目前在欧盟认证或注册医疗器械时,会要求制造商提供医疗器械的EMDN代码。
EMDN全称为European Medical Device Nomenclature,即欧盟医疗器械术语。
EMDN的第一个版本于2021年5月份发布。目前版本已更新到1.1,在这个更新版本的EMDN中,修正了一些语言和句法,同时,医疗器械软件的新术语和描述(在类别J、W和Z下)也已推出。
此外欧盟指导文件MDCG 2021-12 FAQ on the European Medical Device Nomenclature (EMDN) 描述了EMDN的常见问题。
1、什么是EMDN?
EMDN旨在支持欧洲医疗器械数据库(EUDAMED)的运作。制造商在EUDAMED中注册医疗器械时需要填写器械的EMDN。它与每一个器械的UDI-DI相关联。
EMDN 还在 IVDR技术文档、由公告机构进行的技术文档抽样审核、上市后监督、警戒和上市后数据分析等中也起着关键作用。
2、EMDN的结构是怎样的?
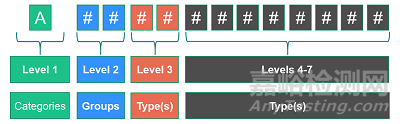
EMDN 的特点是其字母数字结构,建立在七级层级树中。它将医疗器械分为三个主要层级:
Categories类别:第一层级
Groups组:第二层级
Types类型:第三层级(必要时可扩展为几个更细的层级(1、2、3、4和5)
每个代码以一个大写英文字母开头,表示器械所属的“类别”,如W代表体外诊断器械。后面是两个数字,表示“组”和一系列数字,表示“类型”。最大位数设置为13。
3、 该如何查询器械的EMDN?
线上查找方式:
European Medical Device Nomenclature (EMDN) (europa.eu)
https://webgate.ec.europa.eu/dyna2/emdn/(点击文末阅读原文即可访问)
可以通过器械名称的关键词来搜索。
当然也可以在该界面上点击Download EMDN (download full list) 来下载最新的EMDN进行搜索。
4、应该用EMDN的哪一级来给我的器械分配术语?
用EMDN的树状层次结构时,用户必须始终为他们的器械分配最细微的、可用的终端术语(树中的最低层)。
5、 EMDN的应用
前面还提到了EMDN在技术文档的抽样审核中起到了关键作用。IVDR下,C类IVD器械需要使用EMDN和IVP代码给器械进行分组,然后公告机构对每个器械组至少评审1个代表器械的技术文档。







