今日头条
石药RANKL单抗获批上市。石药集团旗下津曼特生物开发的RANKL单抗纳鲁索拜单抗注射液(JMT103,纳乐舒单抗)获国家药监局批准上市,用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。JMT103可通过阻断RANKL与破骨细胞前体细胞、破骨细胞、破骨细胞样巨细胞等细胞的膜上受体RANK结合,进而抑制RANKL-RANK信号通路介导的上述细胞分化成熟与功能活性。在关键临床中,纳乐舒单抗治疗达到93.5%的肿瘤反应率。
国内药讯
1.默沙东九价HPV疫苗报男性NDA。默沙东九价人乳头瘤病毒(HPV)疫苗(酿酒酵母)Gardasil 9的新适应症上市申请获CDE受理,推测申报的适应症为“预防9-45岁男性HPV感染”。这是一款使用重组酿酒酵母CANADE3C-5(菌株1895)分别表达重组人乳头瘤病毒(HPV)6、11、16、18、31、33、45、 52和58型L1蛋白的病毒样颗粒(VLP)的铝佐剂疫苗。该疫苗目前已在中国获批用于9-45岁适龄女性接种预防HPV感染。
2.恒瑞HER2 ADC拟纳入突破性疗法。恒瑞医药HER2-ADC新药注射用SHR-A1811获CDE拟纳入突破性治疗品种,用于治疗HER2阳性晚期结直肠癌。SHR-A1811可通过与HER2表达的肿瘤细胞结合并内吞,在肿瘤细胞溶酶体内通过蛋白酶剪切释放毒素,诱导细胞周期阻滞从而诱导肿瘤细胞凋亡。此前,该新药已有三项适应症被CDE纳入突破性治疗品种,分别用于:HER2低表达的复发或转移性乳腺癌,HER2阳性的复发或转移性乳腺癌,以及HER2突变的晚期非小细胞肺癌(NSCLC)。
3.森朗CD7靶向CAR-T获孤儿药资格。森朗生物自主开发的靶向CD7的CAR-T产品“SENL101自体T细胞注射液”获FDA孤儿药资格,用于治疗复发或难治性T淋巴母细胞淋巴瘤/白血病(T-LBL/ALL)。公布于ASH2022年会上的一项I/II期试验数据显示,SENL101治疗第28天,有95.8%患者的骨髓/外周血实现最小残留病灶(MRD)阴性的完全缓解(CR)。
4.华津溶瘤细菌国内批实体瘤临床。广州华津医药1类生物药SGN1注射液获国家药监局批准,即将开展静脉给药和瘤内给药用于治疗晚期实体瘤的两项临床试验。SGN1是一款广谱溶瘤产品,通过减毒沙门氏菌载体搭载特异的甲硫氨酸水解酶,剥夺肿瘤生长所需的必须氨基酸,从而杀伤肿瘤并阻止肿瘤扩散。此前,该产品已获得FDA授予用于治疗骨肉瘤、肝细胞(HCC)癌和小细胞肺癌(SCLC)三项孤儿药资格。
5.安进双抗多肽偶联药国内报降重IND。安进1类生物制品AMG 133的临床试验申请获CDE受理。AMG133是一款GIPR/GLP-1R双抗多肽偶联药物,可同时发挥抑制GIPR、激活GLP-1R的效应。I期临床数据显示,与安慰剂相比,AMG 133(140mg和420mg)每四周给药一次可使患者体重显著下降(-7.2%和-14.5%,vs1.49%)。今年3月,该产品已启动减重Ⅱ期临床开发。
国际药讯
1.罗氏新型C5补体抑制剂美国报BLA。罗氏旗下基因泰克新一代补体C5抗体crovalimab(珂罗利单抗)的生物制品许可申请(BLA)获FDA受理,用于治疗突阵发性睡眠性血红蛋白尿(PNH)。在Ⅲ期COMMODORE 2研究中,与标准治疗相比,crovalimab在既往未接受补体抑制剂治疗的PNH患者中实现疾病控制,达到避免输血和控制溶血的共同主要疗效终点。目前,该新药已被CDE纳入优先审评,有望在中国获得全球首批。
2.TF靶向ADC宫颈癌Ⅲ期临床成功。Genmab公司与Seagen公司联合开发的靶向组织因子(TF)的ADC药物Tivdak(tisotumab vedotin),在用于治疗复发性或转移性宫颈癌的国际Ⅲ期临床(innovaTV 301)达到主要终点。独立数据监查委员会评估的中期分析显示,Tivdak治疗较单独化疗显著改善患者的总生存期(OS)。研究者评估的无进展生存期(PFS)和客观缓解率(ORR)等关键次要终点也达到统计学显著性。临床中未发现新的安全性信号。
3.Beam公司碱基编辑CAR-T疗法上临床。Beam公司基于胞嘧啶碱基编辑(CBE)的针对CD7、TRAC、PDCD1和CD52四重靶点的同种异体CAR-T疗法BEAM-201,在用于治疗复发/难治性T细胞急性淋巴细胞白血病/T细胞淋巴母细胞淋巴瘤(T-ALL/T-LL)的Ⅰ/Ⅱ期临床完成首例患者给药。这是首次进入临床的碱基编辑疗法,旨在消除CD7、TRAC、PDCD1和CD52基因的表达,具有减少对健康细胞的损伤、移植物抗宿主病和CAR-T细胞耗竭的潜力。
4. AATD寡核苷酸疗法报IND。Wave Life Sciences公司宣布其潜在“first-in-class”寡核苷酸疗法WVE-006已递交了首个临床试验申请(CTA),用以治疗α-1抗胰蛋白酶缺乏症(AATD)。这是一种由突变型AAT蛋白积累导致的可影响肺和肝脏功能的遗传疾病。WVE-006经PN化学修饰、GalNAc偶联的设计,旨在纠正SERPINA1 Z等位基因编码mRNA中的单个碱基突变,恢复AAT正常功能,以改善此疾病在肝脏与肺脏的病征。
5.CD45表位碱基编辑疗法临床前研究积极。宾夕法尼亚大学研究团队使用腺嘌呤碱基编辑器(ABE)开发出的“表位编辑”策略,对造血干细胞和CAR-T细胞进行改造,以改变CAR-T细胞与CD45蛋白结合的“表位”,输入体内后,这些靶向CD45的CAR-T细胞不会自相残杀,也不会杀死输入的表位编辑的造血干细胞,但能够杀死表达正常CD45的血液癌细胞。研究成果发表于Science子刊Science Translational Medicine上。
6.BMS引进泽纳仕CD19抗体。百时美施贵宝与Zenas BioPharma(泽纳仕)就后者一款临床后期潜在“first-in-class”人源化CD19双功能抗体Obexelimab签订合作许可协议,获得Obexelimab在日本、韩国、台湾、新加坡、香港和澳大利亚开发和商业化权益,用于治疗自身免疫性疾病。根据协议,Zenas将获得5,000万美元的预付现金和股权投资,开发、监管和商业里程碑后期付款,以及产品的销售分成。
医药热点
1.李利出任国家药监局局长。国务院发布任免国家工作人员通知,任命李利为国家药品监督管理局局长,免去焦红(女)的国家药品监督管理局局长职务。根据公开信息,李利,男,汉族,1962年9月出生,江西信丰人,1985年8月加入中国共产党,1981年11月参加工作,中央党校研究生,副主任医师。现任国家市场监督管理总局党组成员,国家药品监督管理局党组书记、副局长。
2.国家医保局明确纳入医保支付耗材范围。9月5日,国家医保局发布《国家医疗保障局关于做好基本医疗保险医用耗材支付管理有关工作的通知》,明确纳入医保支付的耗材范围。要适应医疗服务价格改革“技术劳务与物耗分开”的原则, 加强医疗服务价格项目与医用耗材支付管理联动,逐步将未被纳入医疗服务项目价格构成的一次性医用耗材按规定纳入医保支付管理范围。
3.南丁格尔奖颁奖大会在京举行。9月5日,第49届南丁格尔奖颁奖大会在北京人民大会堂举行。我国共有7名护理工作者获奖,分别为海军军医大学第二附属医院急诊重症医学科副主任护师兼血透室护士长陈静,海南省第五人民医院麻风病区护士长邢少云,首都医科大学附属北京朝阳医院内科原科护士长刘小娟,重庆医科大学附属第二医院护理部主任甘秀妮,浙江大学医学院附属第一医院护理部副主任赵雪红,四川大学华西医院护理部主任蒋艳,山西医科大学第二医院护理部副主任张颖惠。
评审动态
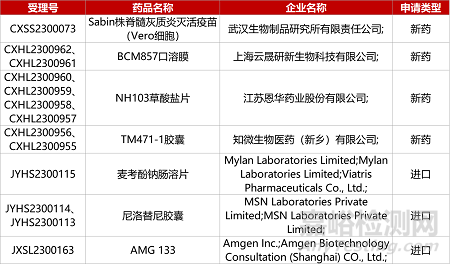
1. CDE新药受理情况(09月06日)
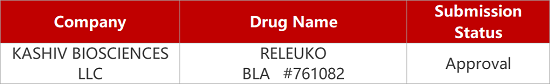
2. FDA新药获批情况(北美09月01日)