人工血管又叫做人造血管,通常是用涤纶、聚四氟乙烯、聚氨酯等物质通过针织、编织或者机织的方式制作而成,一般用于严重狭窄或者闭塞性血管疾病,作为血管替代物或支架,用于恢复血液流动,并维持身体组织的供氧和养分供应。人工血管仿真度比较高,并且长时间使用并不会发生退化、破裂、膨胀等现象,并且人工血管与人体血液相容性比较好,并不会出现排斥的反应。目前,许多材料已被用于制备人工血管。
人工血管(来源:网络)
按照口径大小,人工血管被分为大口径、中口径、小口径。其中,10毫米以上为大口径,6-10毫米为中口径,小于6毫米为小口径。现如今,广泛应用于临床的人工血管均为中口径及大口径,主要用于主动脉置换或搭桥、外周血管旁路移植术、血管创伤修复、血液透析血管通路、冠脉旁路移植术等。
人工血管的发展历史
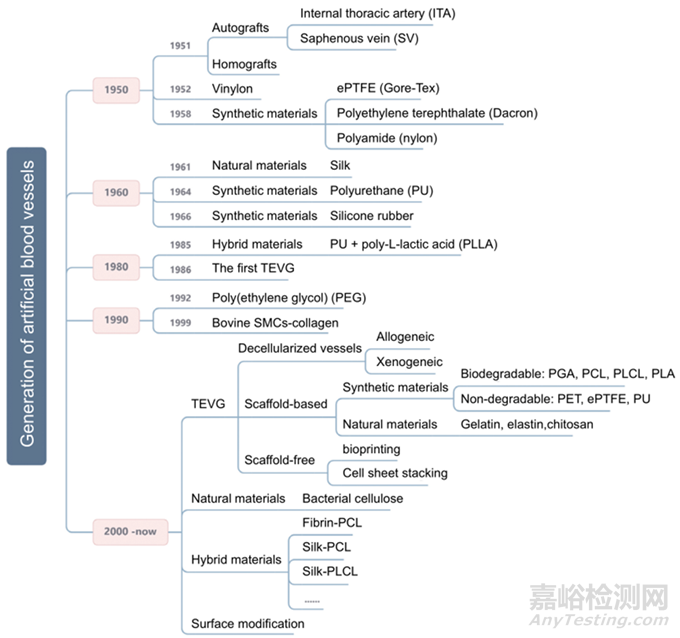
如下图所示,研究人员始终在尝试改善对人工血管移植物的需求。早在1900年左右,奥地利-德国外科医生Payr用可吸收镁制成的细管进行了实验,标志着人工血管首次用于人类。然而,由于镁诱导的纤维化组织的形成,患者在3天后死于肺炎。1951年3月,Dubost等利用尸源主动脉同种异体移植物进行了第一次成功的动脉瘤切除和移植物植入。1954年,Blakemore和Voorhees首次用合成动脉替代品治疗了10名患者,为后来人造血管的快速发展奠定了基础。然后,在1958年,De Bakey等人提出了Dacron人造血管作为尸源同种异体移植物的替代物,后者易于出现晚期并发症。随后,大多数研究人员将注意力集中在各种其他合成材料上,其中涤纶、聚氨酯和膨体聚四氟乙烯(ePTFE)已被证明是血管外科手术中最可行的,但这种材料不适合血管直径<6 mm的情况。
人工血管的发展历史
1986年,Weinberg和Bell用涤纶和胶原复合材料生产了第一个组织工程血管,从此开启了组织过程血管时代。1990年,一种不锈钢和涤纶管移植物制成的支架成功应用于人类血管内动脉瘤修复术。1999年,首次将完全自体工程动脉植入猪受体体内,表现出良好的通畅性和机械耐久性。
在过去的二十年里,各种类型的组织工程血管替代物的开发取得了重大进展。组织工程技术将细胞、组织支架和工程相结合,以生成血管移植物。特别是,在通过不同方法使用组织工程技术方面,小直径人工血管的进展良好,例如使用可生物降解聚合物作为支架或由脱细胞血管组织组成的人工血管。
临床研究进展
人工血管在血管外科以及心血管外科均有应用,其中包括冠状动脉搭桥血管、外周血管补充血管、血液透析血管等。相关产品众多,本文仅以我国首个获批上市的国产人工血管VASOLINE为例,根据其临床试验情况看国产人工血管的有效性和安全性。
VASOLINE人工血管于2019年启动全国多中心临床试验,共入组248例受试者,其中四分叉人工血管采用前瞻性、多中心、随机对照、非劣效性试验设计,共入组188例,试验组和对照组各94例;直线型和侧分叉人工血管采用单组设计,各30例。
该临床试验的主要评价指标为术后12个月生存率。次要安全性评价指标包括术后30天、3 个月、6个月生存率,术后至出院、术后30天、3个月、6个月、12个月、2-5年主要心脑血管不良事件(MACCE)发生率。次要有效性评价指标包括术后12个月人工血管通畅率、术后即刻器械成功率、术后3个月人工血管通畅率、术后12个月人工血管结构完整性、术中出血量、住院时间等。
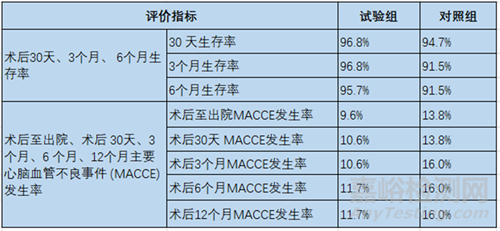
四分叉人工血管试验中,试验组和对照组术后12个月生存率分别为95.7%、90.4%,生存率差值的95%置信区间(-1.9%, 13.0%),达到非劣效性。次要安全性评价指标见表1,次要有效性评价指标见表2。
表1. 次要安全性评价结果
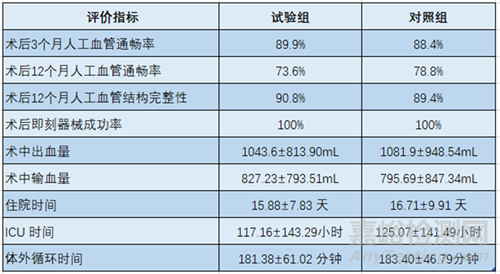
表2. 次要有效性评价指标结果
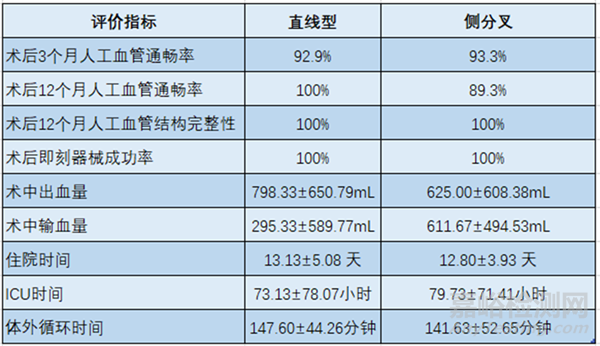
直线型和侧分叉人工血管试验中,术后12个月生存率分别为100%、96.7%。次要安全性评价指标见表3,次要有效性评价指标见表4。
表3. 次要安全性评价结果
表4. 次要有效性评价结果
不良事件发生情况为:随机对照研究中,试验组和对照组分别发生83例、87例不良事件,与研究器械有关的不良事件分别占1.1%、2.1%,两组间无统计学差异。严重不良事件发生亦无无统计学差异。未发生与研究器械有关的严重不良事件。单组研究中,直线型组和侧分叉型组均发生6例严重不良事件,且均与器械无关。
医疗器械行业是一个多学科交叉的高速发展的行业,产品研发周期长,上市后监管严厉。为了保证一款可以造福人民的医疗器械诞生,创新的材料、精密部件和精密加工工艺不可或缺。
人工血管的评价
体外评估
人工血管移植物的体外评估主要包括2个方面:力学性能和生物相容性。
人工血管应该具有足够的机械性能,以支撑正常的血液流动和承受血流压力。同时,要展现出与自然血管相似的弹性特性,以避免狭窄、扩张或破裂等问题。机械性能方面,核心问题在于保持柔顺性的同时,实现高强度。
生物材料的生物相容性也是设计人工血管时应考虑的最基本特性,要确保该材料具有良好的血液相容性,并且由于过敏反应等问题而产生免疫排斥的可能性较低。
体内动物试验
为了满足合理测试各种类型人工血管性能的需求,要建立一个可行且稳定的动物模型。目前,常用的体内血管动物模型是猪、绵羊、狗、兔子和大鼠。根据动物的大小和血管的直径,动脉模型的选择不同。大鼠腹主动脉置换术和兔颈动脉置换术是小口径血管体内验证的可行动物模型。
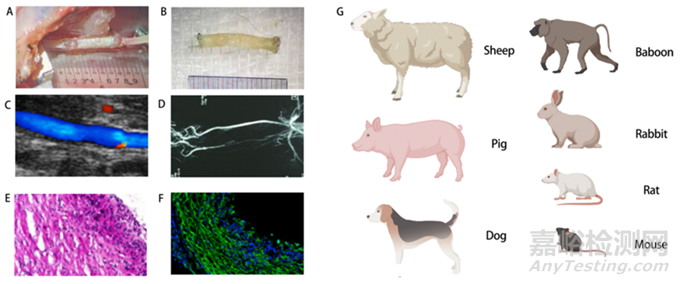
可以使用高分辨率超声来评估移植物的功效,例如平坦度、血管管腔、管腔中的血流速度以及植入后人工血管移植物的频谱波形,通过与手术前拍摄的超声图像进行对比,最终也可用于评估植入后的血管通畅性。此外,微型计算机断层摄影血管造影术还可用于评估人工血管的通畅性和体内人工血管的具体情况。
人工血管的体内评估。(A)植入时移植物的大体视图。(B)移植术后大体视图。(C)移植到大鼠颈总动脉的超声图像。(D)显示移植物通畅性的血管造影记录代表性图像。(E)苏木精和伊红横截面图。(F)血管移植物中段的免疫荧光图像。(G)用于体内评估的常见动物模型。
4、人工血管的未来挑战
目前,采用涤纶、聚四氟乙烯、天然真丝等人造材料制备的大、中口径人工血管已广泛应用于临床,主要用于大血管置换术、血管旁路移植术、血液透析血管通路的建立等。小口径人工血管可用于外周血管替换、动静脉瘘建立以及心脏搭桥术等领域,临床应用范围较广。但迄今为止,尚无小口径人工血管上市,其未能实现商业化的主要是受材料等因素的限制。
许多国内企业及科研院所逐渐将研发目光聚焦于小口径人工血管产品及其材料。该领域研发重点及难点主要在于,用于制备小口径人工血管的材料(如聚氨酯材料、组织工程材料等)性能仍有待提高,血液相容性及抗凝血性能不佳,与血液接触后会不同程度地产生纤维蛋白和血小板沉积,从而导致血管管腔狭窄,甚至造成血管闭塞。同时,由于小口径人工血管中血流速度慢、血压低,且现有材料无法较好支持血管内皮细胞黏附和生长,人工血管植入体内后不能尽快内皮化,容易造成血管管腔狭窄、栓塞,小口径人工血管的远期通畅率问题仍难以解决。
文章整合来源:
1. Hu K, Li Y, Ke Z, et al. History, progress and future challenges of artificial blood vessels: a narrative review. Biomater Transl. 2022 Mar 28;3(1):81-98. doi: 10.12336/biomatertransl.2022.01.008. PMID: 35837341; PMCID: PMC9255792.
2. 关注 | 首个国产人工血管获批上市. 中国食品药品监管杂志, 2022-11-21.
3. 一文了解:“以假乱真”的人工血管. 思宇MedTech, 2023-08-10.
4. Hu K, Li Y, Ke Z, et al. History, progress and future challenges of artificial blood vessels: a narrative review. Biomater Transl. 2022 Mar 28;3(1):81-98. doi: 10.12336/biomatertransl.2022.01.008. PMID: 35837341; PMCID: PMC9255792.
5. 医疗器械产品注册技术审评报告
6. 浅析 | 人工血管市场需求广阔,高端材料国产化仍面临挑战. 翔康医学, 2022-09-12.