今日头条
华东医药引进罕见自免病新药报产。华东医药与Kiniksa公司合作开发的3.1类生物药注射用利纳西普(Arcalyst,rilonacept)的上市申请获CDE受理,用于治疗冷吡啉相关的周期性综合征(CAPS)患者。Rilonacept是重组二聚体融合蛋白,可阻断白细胞介素-1α(IL-1α)和白细胞介素-1β(IL-1β)的信号传导。在美国,该产品已获批用于治疗CAPS,以及IL-1受体拮抗剂缺乏症(DIRA)。
国内药讯
1.君实PCSK9单抗降脂Ⅲ期临床积极。君实生物PCSK9单抗昂戈瑞西单抗治疗原发性高胆固醇血症和混合型血脂异常的Ⅲ期临床详细结果公布于AHA2023年会上。治疗24周时,昂戈瑞西单抗(150mg Q2W和300mg Q4W)两队列LDL-C较基线变化百分比与安慰剂组差异的最小二乘均值分别为-67.74%和-61.2%;在52周治疗期间,两个治疗组LDL-C水平可以维持较基线67.8%~72.9%和51.4%~56.9%的稳定降幅。药物整体安全性良好。
2.恒瑞EZH2抑制剂启动Ⅲ期临床。恒瑞医药EZH2抑制剂SHR2554登记启动一项Ⅲ期临床,评价SHR2554对照西达本胺治疗T细胞淋巴瘤患者的有效性和安全性。该项试验主要研究者由北京肿瘤医院医学博士后宋玉琴担任。今年2月,恒瑞医药已宣布与Treeline公司达成一项超7亿美元的合作协议,将SHR2554在除大中华区以外的全球范围内开发、生产和商业化的独占权利授予Treeline公司。
3.星汉德TCR-T肝癌最新临床数据积极。星汉德生物乙型肝炎病毒(HBV)特异性TCR-T细胞疗法SCG101治疗晚期HBV相关肝细胞癌(HCC)的最新临床数据公布于AASLD年会上。SCG101(5.0×107~1.0×108/kg)单次输注在所有患者中均观察到血清HBsAg下降,其中4例患者血清HBsAg显著降低,疗效维持长达90周;这4例患者均观察到肿瘤缩小,且无进展生存期(PFS)显著延长至25.8周。
4.广州达博人脐带间充质干细胞疗法报IND。广州达博生物“人脐带间充质干细胞注射液”的临床试验申请(IND)获CDE受理。人脐带间充质干细胞注射液(E10I)是由脐带组织经体外分离、筛选、大规模三维扩增后制备所得,临床拟用于治疗II型糖尿病。值得一提的是,今年四月,达博生物实体瘤基因疗法E10A(安达诺欣®)获批临床,为国内首款进入III期开发的基因治疗药物。
5.诺华引进传奇生物DLL3靶向CAR-T。传奇生物与诺华就其特定靶向DLL3的嵌合抗原受体T细胞(CAR-T)疗法以及自体CAR-T候选药物LB2102签订独家全球许可协议,诺华将获得开发、制造和商业化这些细胞疗法的全球独家权利,并可将其T-Charge平台应用于LB2102的生产。根据协议,传奇生物将获得1亿美元的预付款,高达10.1亿美元的临床、监管和商业里程碑潜在付款以及分级特许权使用费。
国际药讯
1.创新口服TTR稳定剂将报NDA。BridgeBio Pharma公司新一代转甲状腺素蛋白(TTR)小分子稳定剂acoramidis治疗伴有心肌病的转甲状腺素蛋白介导的(ATTR)淀粉样变性(ATTR-CM)的Ⅲ期临床ATTRibute-CM最新数据公布于AHA2023会议上。30个月随访结果显示,与安慰剂相比,acoramidis治疗使患者全因死亡风险降低35.5%(风险比为0.645,p=0.0008);acoramidis组与安慰剂组生存率分别为81%和74%。该公司预计年底前向FDA递交新药申请。
2.诺华BTK抑制剂荨麻疹Ⅲ期临床成功。诺华BTK抑制剂remibrutinib治疗慢性自发性荨麻疹(CSU)经治患者的Ⅲ期(REMIX-1和REMIX-2)研究达到所有主要和次要终点。与安慰剂相比,remibrutinib治疗组第12周时患者的每周荨麻疹活动(UAS7)、瘙痒(ISS7)和荨麻疹(HSS7)评分较基线改善的统计具统计学显著性;该组约有三分之一的患者达到完全无瘙痒和荨麻疹症状;两组总体不良事件发生率相当。
3.Alnylam公司长效降压RNAi疗法Ⅱ期临床成功。Alnylam公司与罗氏开发的RNAi疗法zilebesiran单剂量治疗轻中度高血压成人患者的Ⅱ期KARDIA-1临床达到主要终点和所有关键次要终点。第6个月时,zilebesiran(150mg、300mg和600 mg)治疗组经动态血压监测(ABPM)测量的24小时平均收缩压(SBP)安慰剂校正降低分别为11.1mmHg、14.5mmHg、和14.2mmHg(所有p值均小于0.0001)。药物安全性和耐受性良好。
4.乙肝功能性治愈组合疗法Ⅱ期临床积极。Vir Biotechnology公司HBV中和抗体VIR-3434联合siRNA疗法VIR-2218治疗慢性乙型肝炎(CHB)的Ⅱ期临床MARCH最新数据公布于AASLD2023会议上。24周时,VIR-3434/VIR-2218组合,以及VIR-2218/VIR-3434组合+长效干扰素α(PEG-IFN-α)治疗的患者分别有15.0%和14.3%实现EOT时HBsAg的丢失;三联方案组有52%的患者在EOT时检测到>10 mIU/mL的抗乙型肝炎表面抗体滴度。数据显示VIR-3434可作为一种免疫刺激剂,在功能性治愈乙肝方面起到重要作用。
5.门诊用BCMA CAR-T治疗AL早期临床积极。Immix Biopharma公司靶向BCMA的CAR-T疗法NXC-201用于治疗复发/难治性轻链淀粉样变性(AL)的Ⅰb/Ⅱa期最新数据公布于ASH2023年会上。该产品CAR结构经过优化设计,旨在提高其转导率,以及降低脱靶的发生率,拟用于门诊治疗。数据显示,NXC-201在先前治疗中位数为6的患者中达到100%的总缓解率(ORR);药物耐受性良好。推荐Ⅱ期剂量确定为8亿CAR-T。
6.礼来RNAi疗法降脂蛋白早期临床积极。礼来RNAi疗法Lepodisiran(LY3819469)用于无心血管疾病且Lp(a)浓度平均为110nmol/L受试者的首个人体研究结果公布在AHA2023年会上。数据显示,lepodisiran(4mg、12mg、32mg、96mg、304mg和608mg)能剂量依赖性降低受试者有害风险因子脂蛋白(a)[Lp(a)]浓度。第48周时,608mg剂量组Lp(a)的中位变化为-94%。详细结果同时发表在《美国医学会杂志》上。
医药热点
1.安徽省试点高血压糖尿病一体化管理。日前,安徽省发布《安徽省高血压、2型糖尿病一体化管理试点项目指导方案》,进一步推动安徽省9个市14个县(市、区)高血压、2型糖尿病一体化管理试点工作,促进医防融合,降低或减缓“两病”引起的相关并发症。项目试点周期3年,预计至2025年底,试点地区一体化管理的“两病”患者占辖区管理的高血压患者、2型糖尿病患者的比例将达到70%左右,“两病”并发症住院人数将降低10%左右。
2.上海市第六人民医院领导班子调整。11月13日下午,上海申康医院发展中心党委在上海市第六人民医院召开干部会议,宣布申康中心党委关于上海市第六人民医院领导班子成员调整的决定:陈梅同志任中共上海市第六人民医院委员会副书记,纪律检查委员会委员、书记,免去陈梅同志的上海市第六人民医院副院长职务;岑珏同志任上海市第六人民医院副院长,免去岑珏同志的中共上海市第六人民医院委员会副书记,纪律检查委员会委员、书记职务;范理宏同志任中共上海市第六人民医院委员会委员、副书记。
3.首儿所通州院区建设项目获批。近日,北京市发改委批复首都儿科研究所附属儿童医院通州院区项目建议书(代可行性研究报告)。儿研所通州院区项目位于通州区宋庄镇,总建筑面积18.64万平方米,其中地上建筑面积11.33万平方米、地下建筑面积7.31万平方米。项目按照800张床位规划建设,主要设置医疗综合楼、教学科研楼、感染楼等。项目建成后,儿研所将实现“一院两址”办医。
评审动态
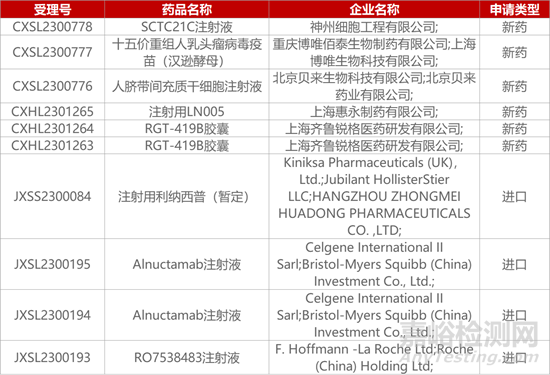
1. CDE新药受理情况(11月14日)
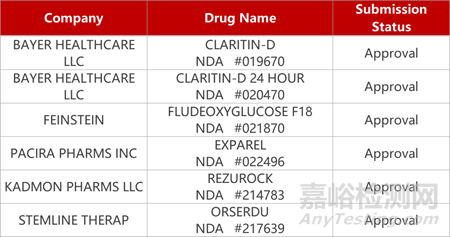
2. FDA新药获批情况(北美11月09日)