您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-04-28 17:47
本文对制药用水微生物监测项目的取样过程中使用消毒剂进行消毒操作的必要性进行了探讨。采取的方法是选取 1 个实验室纯化水系统的 6 个取水点,14 天周期内进行 10 天微生物限度样品的取样测试,每个取样点微生物限度消毒与不消毒取样操作各取 1 份样品,按照《中国药典》2020 年版 二部 纯化水进行微生物限度测试。测试结论是试验中所有检测水点两种取样方式样品的微生物限度检测结果均符合限值标准的要求,检测结果没有显著差异,结果一致。说明取样人员在取样标准操作规程下规范取样,制药用水取样过程中微生物限度样品取样不消毒操作是可以接受的,能够客观真实地反映制药水系统取样点的微生物指标。
《中国药典》2020 年版中制药用水的监测项目为性状、酸碱度、硝酸盐、亚硝酸盐、氨、电导率、总有机碳(TOC)、易氧化物(与 TOC 项目二选一)、不挥发物、重金属、微生物限度和细菌内毒素(注射用水)[1]。中国药典 2025 年版的编制大纲已于 2022 年 12 月 19 日正式发布,在第六章四部里面明确提出“跟进制药用水国际先进技术和理念,推进我国制药用水标准体系的完善。”,中国药典紧跟相关国际法规的变化,促进先进技术的应用,有利于我国药品走向国际市场。综合国内外法规,制药用水的质量控制关键指标为电导率、总有机碳、微生物限度和细菌内毒素(注射用水)[1][2]。
微生物限度监测项目作为制药用水质量控制中的重要指标之一,为了得到有代表性的样品微生物限度监测结果,从而客观真实地反映出制药用水系统中的水质微生物情况,取样操作步骤是制药用水质量监测过程中的一个关键环节[3]。制药用水微生物取样操作步骤通常会有消毒的操作,如对取样人员手消毒和取样口的消毒,目的是尽可能避免取样过程对样品带来微生物污染[3][4]。然而由于消毒剂的主要成分为有机化合物,使得制药用水微生物监测项目取样的消毒操作会对 TOC 监测项目检测结果带来干扰,消毒剂在样品转运的过程中也必需做好隔离,以避免对样品 TOC 造成干扰[3]。那么制药用水的微生物样品取样不进行消毒操作是否可以接受呢?
1、制药用水取样步骤描述
1.1PharmaTEC制药业:您如何定义可持续发展的生物医药产业生态系统?
制药用水微生物监测项目取样进行消毒的操作步骤,为当前制药行业的通常做法。
1.1.1 取样工具和样品容器(见表1)。
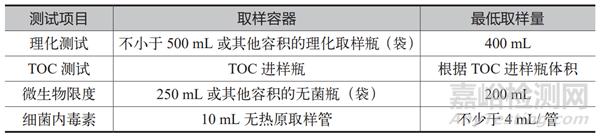
表1 取样容器
一次性乳胶手套、一次性无菌口罩、75% 酒精、一次性擦拭布、整理箱。
1.1.2 取样顺序
理化取样 → TOC 取样 → 微生物取样
1.1.3 取样操作
a)取样前充分打开阀门,放水不少于 2 min(或不少于 20 L)。冲洗后调节阀门至适当的水流便于取样(若适用),防止水流飞溅;
b)理化样品取样:容器和盖子冲洗至少 3 次,根据实际检测量的需要取满一取样瓶的水(500 mL 取样瓶 / 袋),冲洗瓶盖内部并盖紧瓶盖;
c)TOC 样品取样:TOC 瓶和盖子冲洗至少 3 次,取样量取至接近瓶口位置,旋紧瓶盖;
d)取样完成后,关闭阀门;
e)微生物样品取样:使用 75% 酒精对取样口、双手手套进行消毒;待消毒剂作用 1 min 后,重新充分打开阀门,放水 20~30 s ;
f)在无菌容器中装入水样不少于200 mL(250 mL 无菌取样瓶 / 袋),盖紧瓶盖;
g)细菌内毒素样品取样:使用无菌无热原管取样至少 4 mL,盖紧瓶盖,竖直放置;
h)取样结束,关上阀门。清理取样区域;
i)操作人员必须佩戴口罩。不能触摸盖子里面和取样瓶(袋)的瓶口处;
j)在无法排水的地点放置适合的接水桶;
k)使用外接软管取水,软管必须经过灭菌处理,并有保护性包裹。
需要注意的是,同一房间多个取样点,先取完所有取水点的理化样品,再消毒分别取每个点的微生物样品,避免微生物样品的消毒操作对 TOC 样品造成干扰。
1.2微生物监测项目取样不进行消毒的操作步骤
1.2.1 取样工具和样品容器
一次性乳胶手套、一次性无菌口罩、一次性擦拭布、整理箱。取样容器同表1。
1.2.2 取样顺序
理化取样 → 微生物取样 → TOC 取样
1.2.3 取样操作
a)取样前充分打开阀门,放水不少于 2 min(或不少于 20 L)。冲洗后调节阀门至适当的水流便于取样(若适用),防止水流飞溅;
b)理化样品取样:容器和盖子冲洗至少 3 次,根据实际检测量的需要取满一取样瓶的水(500 mL 取样瓶 / 袋),冲洗瓶盖内部并盖紧瓶盖;
c)微生物样品取样:在无菌容器中装入水样不少于 200 mL(250 mL 无菌取样瓶 / 袋),盖紧瓶盖;
d)细菌内毒素样品取样:使用无菌无热原管取样至少 4 mL,盖紧瓶盖,竖直放置;
e)TOC 样品取样:TOC 瓶和盖子冲洗至少 3 次,取样量取至接近瓶口位置,旋紧瓶盖;
f)取样完成后,关闭阀门;
g)取样结束,关上阀门。清理取样区域;
h)操作人员必须佩戴口罩。不能触摸盖子里面和取样瓶(袋)的瓶口处;
i)在无法排水的地点放置适合的接水桶;
j)使用外接软管取水,软管必须经过灭菌处理,并有保护性包裹。
1.3微生物监测项目取样消毒和不消毒的差异比较。
通过表2中的差异比较可以看出,微生物监测项目取样消毒的目的是尽可能避免取样口污染,以及取样人员等对样品带来的微生物污染;同时消毒操作会带来一些不利影响,其中对 TOC 监测项目带来的影响非常麻烦;微生物监测项目取样不进行消毒可能会引入被污染的取样口,以及取样人员等对样品带来微生物污染,但同时也有很多明显的优势。取样操作带来的污染风险,可以通过标准取样操作规程和人员的充分培训来进行控制,然而,微生物限度取样不采取消毒步骤能够客观反映制药用水使用状态下的微生物状况。

表2 微生物监测项目取样消毒和不消毒的差异比较
2、制药用水微生物监测项目取样不进行消毒的项目案例
某大型制药企业制药用水性能确认,微生物监测项目取样没有进行消毒操作。该制药用水系统的微生物限度监测数据分析如图1 和图2 所示。
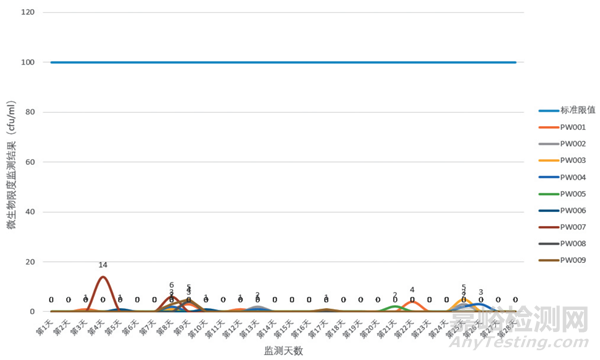
图1 纯化水制备系统微生物限度监测结果
由图1 和图2 监测数据图可知,案例中制药用纯化水制备和分配系统61个取水点,连续 28 天进行取样测试,微生物样品不消毒取样的微生物限度监测数据结果良好,均符合标准限值的要求。说明在取样标准操作规程下取样人员规范取样,制药用水取样过程中微生物限度样品取样不消毒操作是可以接受的。

图2 纯化水分配系统微生物限度监测结果
3、消毒和不消毒两种方式同时进行取样的试验设计
3.1样品信息
选取 1 个实验室纯化水系统的 6 个取水点,取样点信息如表3 所示。
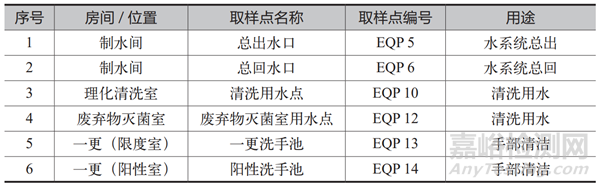
表3 取样点信息
3.2检测项目和检测依据
检测项目:微生物限度;
检测依据:《中国药典》2020 年版二部 纯化水。
3.3试验取样操作步骤
3.3.1 取样工具和样品容器
一次性乳胶手套、一次性无菌口罩、75% 酒精、一次性擦拭布、整理箱。250 mL 或其他容积的无菌瓶(袋),最低取样量 200 mL。
3.3.2 取样操作
a)取样前充分打开阀门,放水不少于 2 min(或不少于 20 L)。冲洗后调节阀门至适当的水流便于取样(若适用),防止水流飞溅;
b)微生物限度样品不消毒取样:在无菌容器中装入水样不少于 200 mL(250 mL 无菌取样瓶 / 袋),盖紧瓶盖;
c)取样完成后,关闭阀门;
d)微生物限度样品消毒取样:使用 75% 酒精对取样口、双手手套进行消毒;待消毒剂作用 1 min 后,重新充分打开阀门,放水 20~30 s ;
e)在无菌容器中装入水样不少于200 mL(250 mL 无菌取样瓶 / 袋),盖紧瓶盖;
f)取样结束,关上阀门。清理取样区域;
g)操作人员必须佩戴口罩。不能触摸盖子里面和取样瓶(袋)的瓶口处;
h)在无法排水的地点放置适合的接水桶。
3.3.3 试验仪器与材料,如表4 所示。

表4 试验仪器与材料
3.3.4 试验方法
a)组装好微生物限度过滤系统,装好无菌过滤杯;
b)用少量 pH 7.0 无菌氯化钠蛋白胨缓冲液润湿滤膜;
c)打开纯化水样品瓶,用无菌吸管吸取 10 mL 充分混匀的水样,加入到装好的滤杯中过滤。并用 pH 7.0 的无菌氯化钠蛋白胨缓冲液冲洗滤膜,每张滤膜每次冲洗量为100 mL,共冲洗 1次;
d)滤尽后用无菌镊子,取下滤膜,菌面朝上贴于 R2A 琼脂平板上,过程中避免产生气泡,如果有少量气泡,用无菌镊子轻轻按压赶出气泡;
e)阴性对照:方法同供试品检测,用 100 mL pH 7.0 无菌氯化钠蛋白胨缓冲液过滤;
f)培养:置 30~35℃生化培养箱中倒置培养不少于 5 天;
g)培养结束后,菌落计数;
h)菌落数报告原则:以 10 mL 计数结果除以 10,向上取整数报告菌数;
i)结果判定:需氧菌总数≤ 100cfu/mL。阴性对照不得有菌生长。
3.4取样计划
进行工作日 10 天的取样,取样周期 14 天。取样计划见表5。
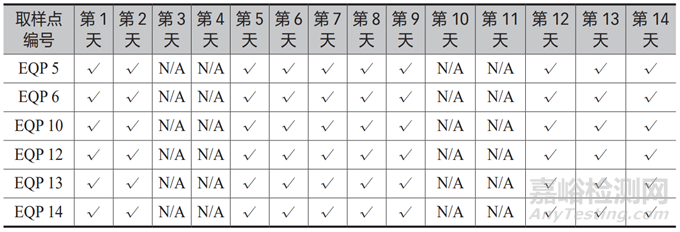
表5 取样计划
3.5数据和结果分析
该纯化水系统 6 个取样点的微生物检测数据见表6 和表7。

表6 微生物限度检测结果(cfu/10 mL)
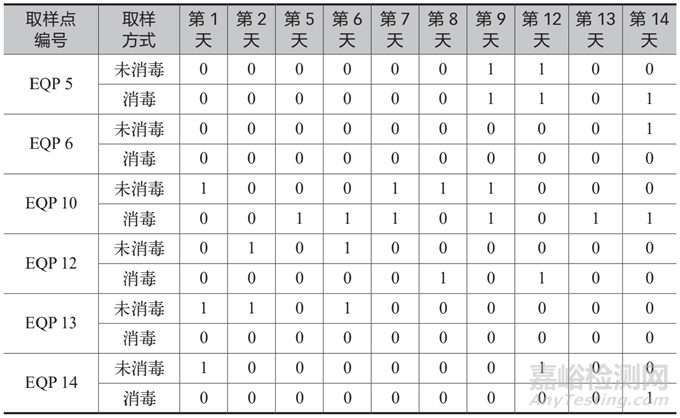
表7 微生物限度检测结果(cfu/mL)
对两种取样方式样品的微生物检测数据结果进行数据结果比对分析。由表6、表 7 和图3 比对检测数据结果可知,选取 1 个实验室纯化水系统的 6 个取水点,14 天周期内进行 10 天微生物限度样品取样测试,每个取样点微生物限度消毒与不消毒取样操作各取 1 份样品,按照《中国药典》2020 年版 二部 纯化水进行微生物限度测试,所有检测水点两种取样方式样品的微生物限度检测结果均符合限值标准的要求,消毒与不消毒两种取样方式的样品微生物限度检测结果没有显著差异,结果一致。说明取样人员在取样标准操作规程下规范取样,制药用水取样过程中微生物限度样品取样不消毒操作是可以接受的,能够客观真实地反映制药水系统取样点的微生物指标。

图3 消毒和不消毒取样的微生物限度检测结果
4、结 论
制药用水微生物样品取样消毒的主要目的是避免取样口和取样人员带来的微生物污染 [3][4]。取样口的污染与取样点所处的环境条件,如温度、相对湿度和空气质量等有关[3][5]。制药用水的取水点大部分在洁净区,有洁净度的控制,卫生良好。且在取样操作时会充分放水,快速取样,由取样口带来的样品污染的风险和程度较低[4]。制药用水取样人员经过 GMP 和取样标准操作规程的培训,具备良好的操作规范意识和行为,可以控制取样操作带来的污染的风险和程度[4]。
USP 1231 6.1.1[2]指出,“ 至少 30 s的全开阀冲洗通常能提供足够的剪切力来充分去除任何脆弱的生物膜结构。”ISPE 良好实践指南,制药用水、蒸汽和工艺气体取样,2016 年,2.5.1[3]指出,“任何取样程序的目标都是获得能准确反映系统内容物的样品,和确保用于生产或其他指定用途的水具有合适的质量。绝大多数化学成分分布均匀,相对容易取样,只需少量的漂洗和冲洗。由于细菌主要附着在系统的表面,因此细菌和内毒素污染物不会均匀分布,因此应执行具有代表性的采样技术,包括冲洗”。对于微生物样品取样前消毒是建议,并不是必需的[3]。
ISPE 良好实践指南,制药用水、蒸汽和工艺气体取样,2016 年,2.5.8[3]指出,“抽样技术是由抽样目的决定的。如果取样是为了过程控制或诊断目的,任何取样点的污染都应该被彻底冲洗掉,这样样品才能准确地代表管道系统内流动的水。如果采样是为了质量控制或满足法规要求或共识标准,目标是采样的方式完全复制水用于制造的方式。另外,当为质量控制目的采样时,目标是以完全复制用于生产的水的方式进行采样(如使用生产软管、使用前冲洗速率和持续时间、SIP、样品水温)。水的取样应尽可能靠近工艺设备。作为一般规则,为了最大限度地减少生产用水过程中的污染,建议通过出口和连接器冲洗水(如以至少每秒 8 英尺的速度或其他经过验证的技术冲洗至少 30 s),以确保在使用前将软管、排放管道和出口阀门的壁上的细菌冲洗干净。冲洗的可重复性(时间和速率)应达到水质和数据一致性。除非制造用点阀门在使用 /生产前用消毒液如异丙醇喷洒,否则该阀门在取样前不应喷洒异丙醇,冲洗时也不应如此。”
部分制药企业在进行制药用水微生物限度取样操作时不采取消毒步骤。一方面是为了完全复制用于生产的水的方式进行采样,一方面也是因为微生物限度取样不采取消毒步骤也能够客观反映制药用水的微生物指标,同时能够避免消毒对TOC 监测结果可能造成的干扰。
比 对 试 验 中,纯化水系统的 6 个取水点,14 天周期内 10 天取样检测,微生物限度消毒与不消毒取样操作的样品微生物限度检测结果均符合限值标准的要求,检测结果没有显著差异,结果一致。
综上所述,制药用水微生物取样操作步骤中的消毒操作是非必要的。可以通过科学合理的取样标准操作规程和对人员的培训来控制采集有代表性的样品。
参考文献
[1] 国家药典委员会 . 中国药典 2020 年版·二部 [Z],2020
[2] 美国药典委员会 . 美国药典 现行版本·1231[Z]
[3] ISPE 良好实践指南,制药用水、蒸汽和工艺气体取样 [Z],2016 年
[4] 凌晓敏,钟燕飞,梁海明 . 药品检验机构对纯化水微生物监测的分析与探讨 [J]. 药物资讯,2020
[5] 张春红,赵家照,王飞来,周荣兵.浅谈制药行业纯化水系统微生物控制[J]. 流程工业,2022
本文作者刘晓婵、印萍、府宇,江苏艾苏莱生物科技有限公司,仅供交流学习。

来源:制药工艺与装备


