您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2020-03-17 10:05
概述
环氧化合物(结构见图1)通常作为原料药或原料药中间体合成中使用非常广泛的起始物料,例如抗凝药物利伐沙班中,利用 (S)-2,3-环氧丙醇来合成其关键中间体,S-环氧氯丙烷则是利奈唑胺原料药合成中用到的一个关键起始物料。由于环氧化物三元环的刚性结构,环张力较大,具有很高的反应活性,在药物合成过程中易与胺基、有机金属试剂、卤代化合物、芳香化合物、氰化物等亲核试剂发生反应而开环,环氧化物的两个亲电性碳原子能够与DNA结构中的亲核中心反应,形成烷基化产物,导致DNA突变而危害人类健康。
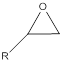
图1.环氧化合物结构图
环氧化物具有警示结构,是已知的潜在基因毒性杂质,其结构种类繁多,是基因毒性杂质中较为常见的一类。药品生产过程中是否有环氧化合物的残留已成为基因毒性杂质是现阶段药物研究过程中重要讨论和控制的内容,也已成为国内外药品注册审评不可缺少的项目。由于环氧化合物在高温下极易容易分解,给分析方法的建立带来了巨大的挑战。
根据参考各国药典及文献,总结了部分含有环氧化合物类基因毒杂质药物的种类,详见表1。
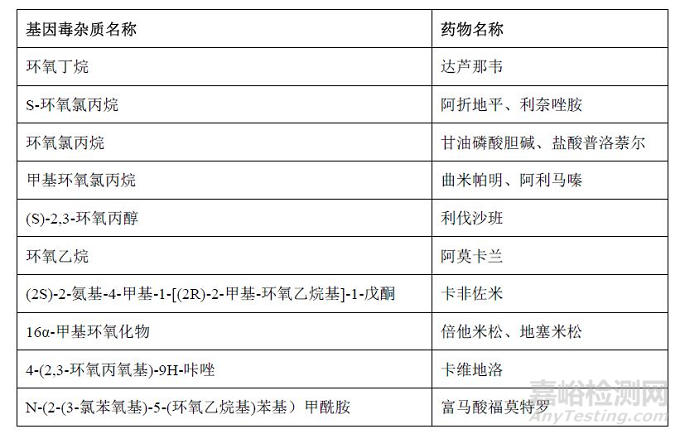
表1. 含有环氧化合物类基因毒杂质药物列表
常用的检测方法:
直接检测法:
对于具有一定挥发性的环氧化合物,如环氧乙烷,因其具有很强的挥发性,所以气相色谱法是此类基因毒杂质的主要检测分析手段。有文献报道,采用GC-FID法直接测定阿莫卡兰中的环氧乙烷的残留量,其LOD为0.09 μg/g,可达到较高的精密度和灵敏度。近年来,对环氧氯丙烷(ECH)杂质检测方法报道也比较多,常用气相色谱法、气相色谱-质谱联用法直接进行检测。
对于非挥发性环氧化物则采用液相色谱法进行检测。文献显示,采用HPLC-UV法分别检测地塞米松中的一对差向异构体16α-甲基环氧化物和16β-甲基环氧化物,两者的分离度大于3,LOQ均为30 ng/mL。
衍生化法:
环氧化合物化学性质不稳定,且有些环氧化物是中性分子,不容易在ESI离子源中质子化和去质子化,因此无法通过MS检测器来直接检测。当样品不能直接进样分析时,为了满足分析方法的要求,通常会选择柱前衍生的方法,将其转化为容易质子化的化合物或具有强紫外吸收的化合物,从而提高环氧化合物的检测灵敏度。据文献报道,采用二甲胺作为衍生化试剂,结合ESI-MS检测方法对原料药中的环氧化物进行了残留量的测定,LOD能够达到1ng /mL。也有不少文献采用3,5-二氟苄胺、N,O-双(三甲基硅烷基)三氟乙酰胺、亚硫酸钠等作为衍生化试剂测定水中或者其他基质中的环氧化合物,通过借鉴这些方法并进行方法优化,则也可以应用于药物中环氧化物基因毒杂质的测定。
其他方法:
衍生化法并不适用于所有环氧化合物,特别是含有多个亲电基团的环氧化合物,如:(2R)-2-[(5-溴-2,3-二氟苯氧基)甲基]环氧乙烷、(R)-对甲苯磺酸缩水甘油酯等,衍生化反应可能会生成多个产物,给检测带来巨大困难与挑战,为了能够有效检出,这类化合物可以采用配位离子喷雾质谱(CIS-MS)法直接法进行测定,在CIS-MS中,环氧化合物中性分子在溶液中或者气相状态下容易转变为带正电或者带负电的化合物,能够有效提高其检测灵敏度。
案例
盐酸普洛萘尔:
盐酸普洛萘尔(Propranolol,化合物1,图2),是β受体阻断类药物中的代表药物,在临床上广泛应用于心律失常、心绞痛等疾病。在盐酸普洛萘尔的合成工艺(图2)中,一般以α-萘酚与环氧氯丙烷(ECH)作为起始原料,得到中间体4,之后中间体4在异丙胺中发生开环反应得到中间体5,最后在加热回流环境中进行盐酸化处理反应制得盐酸普洛萘尔成品。盐酸普洛萘尔的合成工艺中使用到的环氧氯丙烷(化合物3,图2)具有警示结构,为已知的基因毒性杂质,因此必须对其进行严格控制。

图2. 盐酸普洛萘尔的合成工艺
因此,采用GC-FID的方法测定环氧氯丙烷。根据ICH指南要求,对该方法进行了检测限(LOD)、定量限(LOQ)、线性、精密度、准确性等相关验证,环氧氯丙烷在2 ppm~11.25 ppm的范围内成良好的线性关系,相关系数R2=0.9985,环氧氯丙烷的LOD和LOQ分别能够达到0.5 ppm及2 ppm,平均回收率为97.2%,该方法灵敏度非常高、操作简单且无机制干扰,适合在痕量水平下对盐酸普洛萘尔中基因毒杂质环氧氯丙烷进行控制。
卡维地洛:
卡维地洛(Carvedilol,化合物6,图3)是由德国Boehringer Mannheim公司开发的第三代β受体阻滞剂,该药于1991年首次在美国上市。卡地维洛的合成是以4-羟基-9H-咔唑(化合物7,图3)为原料,在强碱催化下,反应形成中间体8,然后中间体8与另一个中间体2-(2-甲氧基苯氧基)乙胺(化合物9,图3)反应得到卡维地洛成品。事实上,该合成工艺的中间体4-(2,3-环氧丙氧基)-9H-咔唑(化合物8,图3)含有环氧化合物的警示结构,具有潜在的遗传毒性和致癌性,因此,依据EMA和FDA相应的指导原则,有必要对卡维地洛中的4-(2,3-环氧丙氧基)-9H-咔唑的残留进行定量分析。根据ICH发布基因毒性杂质的最大摄取量为1.5 μg/d计算,卡维地洛最大日剂用量为100 mg/d,则对应的基因毒性杂质4-(2,3-环氧丙氧基)-9H-咔唑的TTC水平为15ppm。
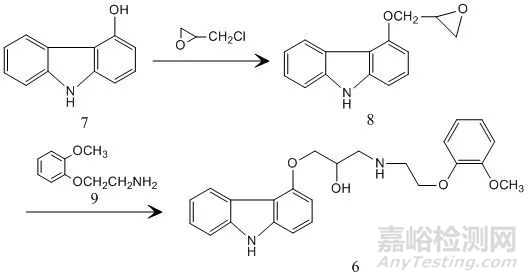
图3. 卡维地洛合成工艺
因此,采用LC-MS直接检测的方法对4-(2,3-环氧丙氧基)-9H-咔唑进行定量,在该方法下LOQ 为2.68 μg/g,LOD 为 0.825 μg/g,在0.2~22.5 μg/g的浓度范围内均成良好的线性关系,相关系数R2=0.9995,回收率为96.7-101.5%。该方法快速、简单、准确且经全面验证后符合检测的需求。
总结
环氧化合物作为潜在的基因毒性杂质,通常作为起始物料或中间体存在于药物合成过程中,这些物料通常会作为杂质存在于终产品中,可能具有遗传毒性和致癌性而危害病人的健康。因此,药品中如果含有上述种类的基因毒性杂质,就需要对其进行严格的控制。由于环氧化合物种类繁多,且化学性质各异,因此需从灵敏度、选择性、待测物稳定性、基质复杂性等进行全方面分析,选择合适的分析检测手段。
值得注意的是,有时采用基因毒性物质作为起始物料或反应试剂是不可避免的,除此之外,还会涉及到合成工艺流程的方方面面以及包括随后的药品的稳定性和可能的降解杂质,这是一个极其复杂的过程问题,因此对基因毒性杂质的有效控制是不可忽视的。不得不承认,基因毒性杂质研究是一件非常富有挑战性的工作,它涉及到工艺化学、毒理学数据采集分析、化学分析方法的建立和有效检测,因此,我们要尽可能地明确药品中存在的各类基因毒杂质的结构、来源以及质控限度,建立一个科学可行的分析方法,从而有效保证药品的质量安全。
本文根据以下文章进行编辑整理,仅用于学习、交流:
1.Shaik J V, Raveendra B.G and Shakil S S. Estimation of epichlorohydrin content in pharmaceutical drug substances by capillary gas chromatography with flame ionisation detection[J]. Journal of Chemical and Pharmaceutical Research, 2011, 3(6):392-399.
2.Rao M. S , Sumathi V. R, Ray U.K., et al. Quantification of 4-Oxiranyl Methoxy 9h-Carbazole a Genotoxic Impurity in Carvedilol Drug Substances by LC-MS[J]. Journal of Bioanalysis & Biomedicine, 2010, 2(4) : 091-095.
3. Kang P X, Yuan X, Fang Z L,et al. Efficient method development strategy for challenging separation of pharmaceutical molecules usingadvanced chromatographic technologies[J]. Journal of Chromatography A, 2007,1163 : 145–156.

来源:Internet


