药品不良反应是指合格的药品在正常的用法用量情况下出现的与用药目的无关的或意外的有害反应,它不包括无意或故意的超剂量用药引起的反应以及用药不当引起的反应。许多药品不良反应是在药品质量检验合格的情况下发生的。
主管部门此前召回相关生产厂家部分批次的产品,大多数是经国家药品检验机构的检验后发现相应药品质量不符合法定质量标准的产品。
查阅资料发现,主管部门2010年至今因质量问题召回产品大多是注射剂且主要是化学药注射剂,召回原因中“‘可见异物项’不符合规定”出现的频次最多。
注射剂是所有剂型中质量要求最高的,因为人体微循环血管的直径为7μm~12μm,仅能通过单个排列的血细胞,若注射剂中存在可见异物,注射进入人体后,可引起静脉血管炎、血栓、变态反应、微循环障碍,可见异物的存在还会引起热原样反应、过敏反应的发生。
“可见异物”项目本身属于《中国药典》规定要检测的内容,可见异物的检测需要使用专用灯检仪,并且要配备特定照度、黑色背景及经过培训的专业人员,一般的基层医院不具备这些条件。往往是患者发生了不良反应之后药品检验机构检查产品质量时才发现“可见异物”项目的不达标,然后主管部门才发公告召回产品,滞后性常常使得注射剂可见异物导致的医疗纠纷屡见不鲜,直接危害患者的身体健康。
可见异物是指存在于注射剂、眼用液体制剂和无菌原料药中,在规定条件下目视可以观测到的不溶性物质,其粒径或长度通常大于50μm。根据2015年版《中国药典》要求,注射剂、眼用液体制剂应在符合药品生产质量管理规范(GMP)的条件下生产,产品在出厂前采用适宜的方法逐一检查并同时剔除不合格产品。临用前,需在自然光下目视检查(避免阳光直射),如有可见异物,不得使用。
我国在注射剂产品检验所有不合格项目中,可见异物检查项始终排在首位。注射剂可见异物的来源有两个方面:一是来源于外源污染,如金属屑、玻璃屑、纤毛和块状物等; 二是来源于内源产生,如药品中存在或产生的不溶物、析出的沉淀物和结晶等,这些形形色色的不溶物不仅直接关系到患者的用药安全,也可间接反映出药品是否严格按 GMP 的要求生产,产品的处方、工艺、药包材的选择是否合理,剂型的选择是否得当。
2005版《中国药典》将注射剂的澄明度检查项目修订为可见异物项目后,其标准大幅度提高。2015年版《中国药典》对于注射剂供试品中不得检出金属屑、玻璃屑、长度超过2mm的纤维、最大粒径超过2mm的块状物以及静置一定时间后轻轻旋转时肉眼可见的烟雾状微粒沉积物、无法计数的微粒群或摇不散的沉淀。
外源性的可见异物一般为生产过程中引入和环境污染所致,主要为生产管理上没有严格按质量管理的标准管理规程SMP、质量管理标准操作规程SOP 的要求管理和操作所致。例如,小容量注射剂一般采用的包装为安瓿。安瓿的生产厂家在进行生产时周围环境控制没有达到标准,就会在生产安瓿的过程中将可见异物引入。另外,如果安瓿的清洗过程中洁净度不达标,有些可见异物会附着在瓶子的内壁。这些都是导致小容量注射剂产生可见异物的原因之一。
针对这种情况,应当在安瓿的生产过程中,对于生产车间的环境质量要严格把关,同时,应当加大对于安瓿的抽查力度,对其质量进行控制。防止因为包装材料的不合格致使小容量注射剂产生可见异物。
从表1可见,玻璃类抗生素瓶作为粉针剂的主要包装材料,国际知名药企的成品也可能产生玻璃屑。从生产工艺风险分析发现,抗生素瓶受温越高,其膨胀量越大,也越容易引起碎瓶。即使有些抗生素瓶生产时没发生碎瓶,但放置一段时间后仍可能析出玻璃屑。国内部分制药企业对抗生素瓶隧道式热风循环灭菌烘箱去热原灭菌的工艺指标还停留在传统的“350℃、5min”水平,国内部分制药企业现设定为“320℃、5min”,欧美制药企业的灭菌工艺指标在“300℃”左右,通过延长灭菌时间,可达到同等灭菌、去热原的效果,从而避免因灭菌温度过高带来可见异物增加的风险。
药品生产管理越来越讲究加强药品医疗器械全生命周期管理的理念,注射剂的可见异物风险识别及控制需要遵循质量源于设计原则、风险管理原则和GMP符合性原则,从质量风险管理的流程着手解决,才能使药品的质量风险降低至一个可以接受的水平。
内源性通常是药物结晶或沉淀物质,这可能需要从产品的处方、工艺、剂型的选择方面分析风险。
原辅料在外观、性状、细菌内毒素、微生物等多个方面存在着较大差异,由于原辅料特性不同,注射剂工艺参数不同,就会导致某些注射剂生产中的药液在灭菌、受热后有白点、白块等异物析出,从而产生可见异物。如质量较差的葡萄糖在配制溶液过滤后,管道内壁会残留乳白色物质,药液在灯检过程中会被发现有白点、白块等,从而影响产品的质量。
活性炭是输液生产中吸附杂质、热原等不可缺少的, 但是它其中含有微量金属离子, 能使药液氧化分解而增加输液中的微粒。
在生产过程中,酸碱度对药物的稳定性有很重要的作用。不同的药物所需的环境不同,酸碱度就不同,应当根据所生产的药物的特点来制定生产环境的酸碱度。尤其是在生产一些中药制剂时,中药的某些成分与溶液的pH值有很大关系,一部分中药成分会溶解于溶液当中,产生沉淀。
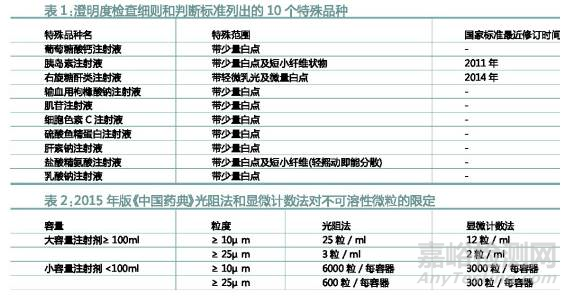
“可见异物”项目在2005版《中国药典》颁布实施之前,称之为“澄明度”项目,采用的是1991年原卫生部国家标准(药典、部颁布件)(91)卫药标字01号《澄明度检查细则和判断标准》,列出10个特殊品种。其中右旋糖酐类注射液进入第3期药品不良反应信息。
2005版注射剂用“可见异物”检查取代了原来的“澄明度”检查,同时注射用无菌粉末也要求进行“不溶性微粒”检查。2015年版《中国药典》要求静脉用注射剂(溶液型注射液、注射用无菌粉末、注射用浓溶液)及供静脉注射用无菌原料药中不可溶性微粒的大小及数量。药典要求的方法有光阻法和显微计数法(见表2)。
《中国药典》对注射剂中微粒的控制仅限于粒径大于等于10μm和25μm的微粒数有所限制,但对粒径10μm的微粒则未作规定。粒径为2μm~10μm的微粒则可能造成潜伏性的更大危害。
《中国药典》对不溶性微粒检查法的规定和叙述越来越翔实,越来越严格。特殊产品在新规之下应该有新的限定与豁免,而不是笼统地“带少量白点”即可逃过检查。
以葡萄糖酸钙注射液为例,作为特殊品种,虽然没有进入药品不良反应信息通报,但是在历年应质量问题召回的产品名单中,可见个别厂家因“可见异物”项目不符合规定导致寒颤、发热症状不良反应而面临召回。
查询国家及各省级药品质量公告情况发现,在国家层面组织的基本药物全国抽验和省级药品监督管理部门组织的监督抽验中,葡萄糖酸钙注射液(10ml:1g)均有报道质量不合格的情况,且自2012年以来抽验不合格的批次数量有上升趋势。
葡萄糖酸钙注射液的不良反应主要和其溶解度有关。葡萄糖酸钙为D-葡萄糖酸钙盐-水合物,因钙离子所带电荷较大,决定了其在沸水中易溶,在水中缓缓溶解,略溶于冷水(3g/100mL,20℃)。1份葡萄糖酸钙完全溶解需要5份沸水或30份冷水。葡萄糖酸钙注射液中葡萄糖酸钙的浓度是其在冷水中溶解度的3.3倍,10%小水针的葡萄糖酸钙注射液很容易受温度影响变成过饱和溶液,从而在储存或生产过程中,非常容易析出白色结晶而检测不合格,最终对用药安全或产品稳定产生严重影响。由此可见,葡萄糖酸钙注射液(10ml:1g)本身在处方的设计上就存在缺陷。
2010 年以来全国各地中标的相关企业有中,部分企业明知产品存在质量和安全风险,却仍然继续生产,有失妥当。而葡萄糖酸钙注射液(10ml:1g) 临床上主要用于钙缺乏,急性血钙过低、碱中毒及甲状旁腺功能低下所致的手足搐搦,过敏性疾患,镁、氟中毒的解救,以及心脏复苏时应用(如高血钾或低血钙、或钙通道阻滞引起的心功能异常的解救)。该品种为国家基本药物目录品种,并且仅有小容量溶液规格10ml:1g进入目录,属矿物质类药。
葡萄糖酸钙注射液(10ml:1g)在制备和贮存过程中析出可见异物的问题,影响因素很多,有原辅料的纯度、助溶剂的种类、溶液的pH值、空气中的二氧化碳、配制及灭菌的温度及时间、金属离子等,其中贮存中的析出物是不可溶的。2015年版《中国药典》中对于葡萄糖酸钙注射液的检查项目中未对“不溶性微粒”检查有所豁免,那么葡萄糖酸钙注射液(10ml:1g)比较难在抽检中检查合格。
绝大多数小容量注射剂和粉针剂在使用时都需要复配或稀释,而复配在操作环境、操作方法和配伍输液等方面均与药典对注射剂中不溶性微粒的检测过程不同,是注射剂在使用过程中引入或形成不溶性微粒的关键环节。
此外,临床应用中,大容量静脉用注射液常是与小容量注射剂配伍使用,药典对配伍后的混合溶液的不溶性微粒限值并没有做出明确限定。而这些注射剂(尤其是中药静脉注射剂)配伍后发生不溶性,微粒超标的情况时往往就比较严重了。
2017年5月,CFDA发布的关于征求《关于鼓励药品医疗器械创新实施药品医疗器械全生命周期管理的相关政策》(征求意见稿)意见的公告(2017年第54号)提到,要完善药品医疗器械不良反应/事件报告制度,以及开展上市注射剂再评价。2017年10月1日,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)提到,力争在5至10年左右完成注射剂再评价。在注射剂再评价工作完成前,为保证安全用药,有关部门可继续适时发出风险警示,指导临床谨慎用药。
此外,在完善药品医疗器械不良反应/事件报告制度方面,将在由过去的医疗机构报告不良反应/事件制度基础上,改为药品上市许可持有人为主体的不良反应/事件报告制度。
药品上市许可持有人将要承担所生产的药品不良反应/事件报告的责任,并根据不良反应/事件提出完善质量控制措施,提出修改说明书及标签申请。
通过再评价的,享受化学仿制药口服固体制剂质量和疗效一致性评价的相关政策。预计常常被药品不良反应信息通报,实际检测常常不达标的注射剂很有可能将是首批要求进行再评价的产品。
鉴于注射剂的用药渠道主要为医疗机构,进入再评价目录的注射剂如果没按期完成再评价,就只能退出市场。相较于没过一致性评价的口服药产品还可以在药店渠道销售而言,注射剂再评价对行业的洗牌效应更大。
过去已批准上市的注射剂的再评价工作,应尽早结合批准上市时的研究情况、上市后持续研究情况等综合分析,开展产品成份、作用机理和临床疗效研究,评估其安全性、有效性和质量可控性。生产企业也需要关注《中国药典》对“不溶性微粒”的要求的提高,特别是成分复杂的中药注射剂。
在上述工作基础上,相关企业还应建立从生产到使用全过程检查责任,从流通管理、运输储存、临床实际应用方面出发设计产品,进一步提高注射剂控制和防范微粒进入人体的措施和技术,从而保证患者使用产品时不会发生二次污染的风险,降低不良反应发生率。





