您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-01-29 16:41
近日,器审中心公布了先健科技(深圳)有限公司的创新产品“髂动脉分叉支架系统”的注册技术审评报告,我们一起来了解一下髂动脉分叉支架在研发阶段做了哪些实验。
一、产品概述
(一)产品结构及组成
该产品由髂动脉分叉支架、髂内覆膜支架以及其各自配套的输送器组成。髂动脉分叉支架由自膨式镍钛合金支架和PET膜组成,通过 PET 缝线缝合,支架连接点钢套采用 316L 不锈钢制成,支架显影点材料为钽;髂内覆膜支架由自膨式镍钛合金支架和 ePTFE 膜组成,支架显影点材料为钽。该产品经环氧乙烷灭菌,一次性使用。
(二)产品适用范围
该产品用于治疗腹髂动脉瘤或髂总动脉瘤。
髂动脉分叉支架通过输送器输送至病变位置后,支架会自膨胀开并与血管壁或已释放的腹主分叉支架分支内壁贴附,通过自身的径向支撑力将覆膜支架固定。通过该分叉支架的短分支可将一髂内覆膜支架植入到髂内动脉内,并与髂动脉分叉支架的短分支相连,这样实现了髂内动脉的重建。并且支架覆膜将血流与病变位置隔绝,消除血压对病变位置的影响,以达到治疗腹髂动脉瘤或髂总动脉瘤的目的。
二、临床前研究概述
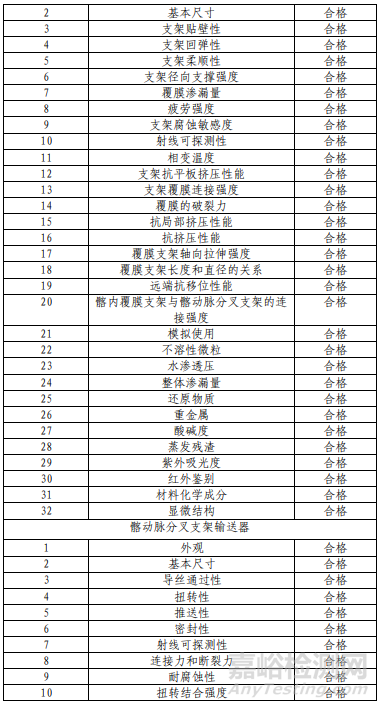
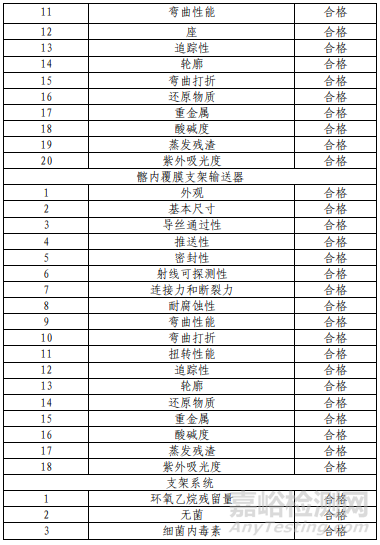
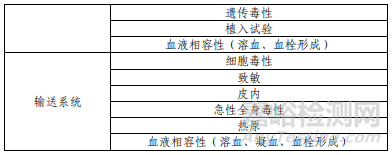
产品性能评价包括支架轴向、弯曲、扭转疲劳耐久性研究、有限元分析、MRI兼容性研究、体外镍离子释放研究、电偶腐蚀研究、ePTFE覆膜化学性能研究、输送器涂层工序 — 14 — 验证确认、灭菌过程确认、无菌检查方法确认等研究,结果表明产品符合设计输入要求。
该产品采用环氧乙烷灭菌,无菌状态提供。申请人提供了灭菌确认报告,证明无菌保证水平为 10-6。
(五)动物研究
申请人开展了以猪和犬为模型的动物实验研究以验证产品的体内安全有效性。通过器械操作、超声、DSA 造影等评估器械可操作性和即刻安全有效性,通过组织病理切片、 DSA 造影等分析支架植入后的长期安全有效性。动物实验结 果表明,产品达到预期设计要求。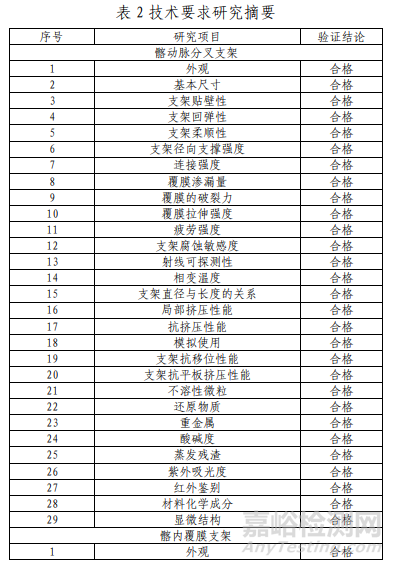


来源:嘉峪检测网


