您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-24 11:15
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.GSK艾滋病复方在华获批上市。葛兰素史克双药HIV疗法多替拉韦利匹韦林片获国家药监局批准上市,用于治疗特定成人人类免疫缺陷病毒1型(HIV-1)感染患者。该产品的美国商品名为Juluca,是全球首个二合一HIV复方药物,最早于2017年11月获FDA批准上市,作为一种长期维持治疗药物,用于已接受至少6个月稳定的抗逆转录病毒方案实现病毒学抑制(HIV-1RNA<50 拷贝/毫升)且无病毒学失败病史、同时对任何NNRTI或INSTI无已知或可疑的耐药突变的HIV-1感染者。
2.艾伯维JAK抑制剂CD适应症报产。艾伯维JAK抑制剂乌帕替尼缓释片(upadacitinib)的第五项适应症上市申请获CDE受理,推测适应症为中重度活动性克罗恩病(CD)的治疗。乌帕替尼是中国首个获批用于治疗特应性皮炎的口服选择性JAK抑制剂,目前在中国已获批用于治疗特应性皮炎、活动性类风湿关节炎和银屑病关节炎。值得一提的是,该新药日前也获得FDA批准第六项适应症,用于治疗成人活动性非放射学中轴型脊柱关节炎(nr-axSpA)。
3.腾盛博药2款长效HIV疗法早期临床积极。腾盛博药将在IDWeek2022会议上公布BRII-732和BRII-778的两项Ⅰ期研究积极结果。BRII-732是一种新化学实体(NCE),口服给药后可代谢为islatravir(强效核苷逆转录酶抑制剂)。BRII-778是一种盐酸利匹韦林缓释制剂。两项研究结果均表明,BRII-732和BRII-778每周一次给药安全且耐受性良好,数据支持该公司在美国针对BRII-732/BRII-778联合疗法用于HIV每周一次给药的临床开发。
4.礼来N3pG淀粉蛋白抗体在华报IND。礼来1类生物药remternetug注射液的临床试验申请获CDE受理。Remternetug(LY3372993)是一款新一代N3pG淀粉样蛋白抗体,目前正在Ⅲ期临床中用于皮下注射或静脉输注评估治疗早期阿尔茨海默病患者的有效性和安全性。此前,LY3372993已在Ⅰb期临床中显示出与淀粉样蛋白降低等级一致的深度斑块清除,并且具有较好的安全性。
5.美杰赛尔PD-1基因编辑T细胞疗法报IND。美杰赛尔1类生物新药PD-1基因编辑T细胞注射液的临床试验申请获CDE受理。此前,这款生物制品已在四川大学华西医院完成研究者发起的Ⅰ期临床,2020年4月发表于《自然-医学》上的数据显示,所有11例晚期难治性肺癌受试者未出现严重不良反应及脱靶问题;部分患者编辑的T细胞可在体内长期存活,TCR免疫组库多样性指标显著改善,且疾病稳定。
国际药讯
1.抗过敏肾上腺素鼻喷雾剂报NDA。FDA受理Silverback公司肾上腺素鼻喷雾剂neffy(2mg)的新药申请,用于紧急治疗≥30kg儿童和成人的I型过敏反应。PDUFA日期为2023年年中。Neffy采用了鼻吸收增强技术Intravail®。这种肾上腺素鼻喷雾给药方法与现有的肾上腺素自动注射器的疗效相当,而且在过敏反应的紧急情况下时,无需打针更易于给药。如果获批,neffy将成为首个用于I型过敏反应的非注射治疗产品。
2.毛果芸香碱配方老花眼Ⅲ期临床积极。Eyenovia公司毛果芸香碱(pilocarpine)配方眼药水MicroLine在治疗老花眼的Ⅲ期临床达到主要终点和所有次要终点。MicroLine与安慰剂相比,在治疗后2小时的低光度情形下,有显著更高的患者比例达到DCNVA视力指标上15个字母或以上的阅读改善,并同时不失去5个字母的远视力;药物总体耐受性良好。该公司计划向FDA递交新药上市申请。极目生物拥有该新药的大中华与韩国地区权益。
3.Opdivo辅助治疗早期黑色素瘤达Ⅲ期主要终点。百时美施贵宝PD-1抑制剂纳武利尤单抗(Opdivo)用于辅助治疗完全切除的IIB/C期黑色素瘤患者的Ⅲ期临床(CheckMate-76K)结果积极。与安慰剂相比,Opdivo可显著降低病患复发或死亡风险达58%(HR:0.42,95% CI:0.30-0.59,p<0.0001);两组12个月无复发生存率分别为89%(95% CI:86-92)与79%(95% CI:74-84);临床中未发现新的药物安全性问题。
4.GSK带状疱疹疫苗保护效力可达10年。葛兰素史克宣布其重组带状疱疹疫苗Shingrix在用于50岁及以上成人的ZOSTER-049扩展研究中获得积极中期结果。该研究对来自ZOE-50和ZOE-70研究的受试者再开展6年的随访,持续评估Shingrix的长期疗效。中期分析显示,从初次接种后的6至10年期间,Shingrix的有效率为81.6%。从第二剂接种1个月到第10年,该疫苗的保护效力为89.0%。Shingrix是GSK的疫苗核心产品,预计今年全年营收超30亿美元。
5.Talaris同种异体细胞疗法III期临床暂停。Talaris公司同种异体细胞疗法FCR001用于抑制活体肾移植(LDKT)患者急性免疫排斥反应的III期FREEDOM-1研究触发了预先指定的试验临时停止要求,并由该研究数据监测委员会(DMC)审查。原因为1例接受治疗的中度慢性移植物抗宿主病(GvHD)患者最近因IV级GvHD住院,并发严重感染最终死亡。在对该事件进行审查后,DMC认为FREEDOM-1研究6月份修订的试验方案足以降低GvHD风险,建议试验继续开展。
6.罗氏近10亿美元引进病毒免疫疗法。罗氏与HookipaPharma公司达成合作和许可协议,共同开发用于KRAS突变癌症的HB-700和第2种未公开的新型沙粒病毒免疫疗法。根据协议,Hookipa将获得2500万美元的预付款,可能达到9.3亿美元的开发和商业化里程碑潜在付款,以及合作产品的销售分成。HOOKIPA将负责HB-700的早期临床开发;罗氏将负责I期试验后的开发和商业化过程。
7.基因编辑公司Editas拟出售肿瘤管线。张锋博士联合创建的CRISPR基因编辑公司Editas Medicine计划出售其临床前肿瘤管线。目前,Editas临床前肿瘤管线共有三款在研产品,其中EDIT-202是Editas与BlueRock联合开发的针对实体瘤的一款NK疗法,其最大的优势是可以通过双重敲入与双重敲除提高疗法的多个治疗特征。此外,肿瘤管线还涵盖与BMS合作开发αβ T细胞疗法以及诱导多能干细胞(iPSC)衍生的自然杀伤细胞(NK)疗法。
医药热点
1.南京鼓楼医院医学美容中心开诊。南京鼓楼医院医学美容中心近日正式开诊。医学美容中心由该院整形烧伤科和皮肤性病科两科室共同组建,主诊医师均在硕士学位及以上,都是专门从事医美行业的专业医生。主要服务内容包括光电类项目(超声炮、超光子、黄金微针、光子嫩肤、调Q激光、冰点脱毛、去痣等)和注射类项目(玻尿酸注射、肉毒素注射等)。
2.上海交大医学院成立医学装备与技术研究院。10月21日,上海交通大学医学院正式成立医学装备与技术研究院,旨在打造具有国际影响力的医学装备和技术研发基地、转化应用基地和人才引育基地,实现医学装备与新技术领域创新链和产业链的深度交叉融合。中国工程院院士王红阳、中国工程院院士程京、中国工程院院士韩德民、中国工程院院士尚红任研究院学术委员会主任,中国工程院院士贾伟平任研究院院长,医学院附属第六人民医院院长殷善开任研究院执行院长。
3.可分解尼古丁肠道细菌或助预防吸烟相关疾病。来自北京大学、复旦大学、浙江大学与美国国立卫生研究院等中美学者合作开展、发表于《自然》的微生物学最新研究显示,研究人员识别出一种可分解尼古丁的肠道细菌——解木聚糖拟杆菌,该种细菌还在小鼠模型中显示出对吸烟相关脂肪肝疾病进展的保护作用。这些发现表明了一种可能的调查路径,以减少一些吸烟相关疾病进展导致的危害。
评审动态
1. CDE新药受理情况(10月22日)
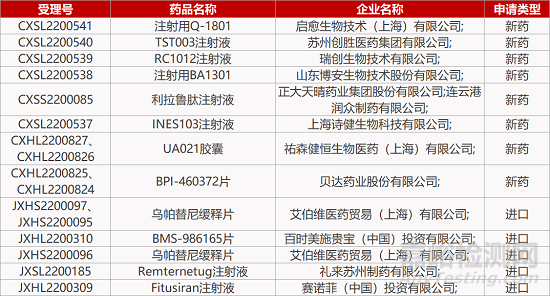
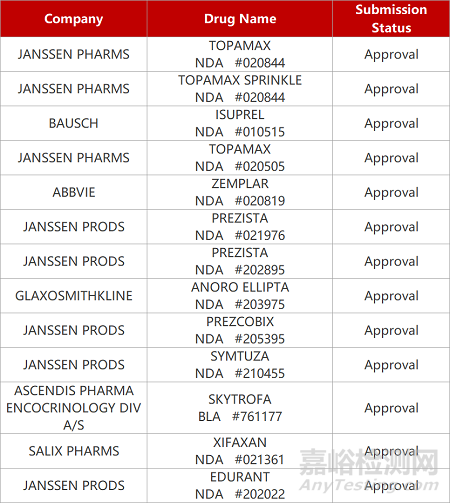

来源:药研发


