生物可吸收支架(Bioresorbable scaffolds,BRS)被认为是心脏介入领域的第四次革命,其诞生旨在解决前代金属支架的缺陷,减少再狭窄和支架内血栓的发生率,并恢复血管的生理机能和完整性。
图1 2012年一篇综述中提到的,当时在研的可降解支架们。(A)AMS(Absorbable metallic stent) 1;(B)AMS 2;(C)DREAMS 1;(D)DREAMS 2;(E)Igaki-Tamai支架;(F)Vascular BRS 1.0;(G)Vascular BRS 1.1和PLLA的化学结构;(H)Reva Medical的BRS版本1;(I)Reva Medical BRS的分子组成和版本2;(K)DeSolve BRS;(L)ART BRS;(M)第一代和第二代IDEAL支架和所使用聚合物的化学结构;(N)Acute BRS;(O)Amaranth PLLA;(P)Xinsorb;(Q)Sahajanand BRS。大家可以看看十年后的现在还剩了几个~
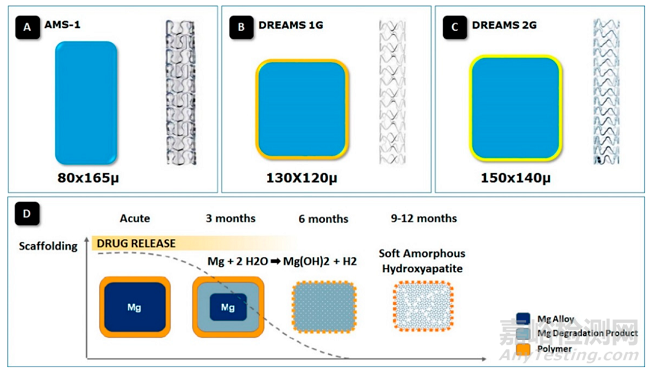
今天想来说说这个上图中Biotronik大厂的镁支架,也是笔者正巧看到了他们在EuroPCR上最新公布的DREAMS 3G支架1年随访结果。Dreams支架是对原始可吸收镁支架AMS系列的改进,因镁合金具有快速的降解/水解速率,必须添加聚合物涂层以减缓其的降解。药物方面,在DREAMS 1G的时候用的还是紫杉醇,到2G开始就都载雷帕霉素了,其浓度为1.4ug/mm2,如下图2。
图2 (A)~(C)几款镁支架的横截面示意图;(D)药物洗脱可吸收镁支架的吸收过程示意图,抗增殖药物的释放在植入后的3月内,整个支架在9个月的随访期间逐渐吸收成软的无定形羟基磷灰石(amorphous hydroxyapatite)
图3 镁基金属支架的比较,可以看到DREAMS 3G和DREAMS 2G相比,小梁更薄了尺寸更多了,但是降解时间还是相似的(笔者曾在哪篇推送里看到说三代改了降解时间,这是不对的,2G到3G的设计应该没有大调整)
图4 各种应用的传统镁合金的组成
我们都知道,镁Mg是人体第四大金属元素,在生理环境中具有生物活性,参与了超过300种有益酶促反应。块状纯镁的密度和杨氏模量约为1.74g/cm3和40GPa,接近人体致密骨的密度和杨氏模量(1.8g/cm3和30GPa),因此可生物降解的镁合金在骨科方面的运用也愈发地受到关注,生物可降解的骨螺钉于2013年即获得CE认证,早于可降解的镁合金支架。上图3中Dream支架的基底WE43镁合金,最初是在1980年代为高强度和高温应用而开发的,主要添加了稀土(RE,rare-earth)元素,包括钇(Y)、钕(Nd)和钆(Gd),稀土元素较高的溶解度、较小的电极电位差和钝化作用,能大大提升镁合金的抗氧化和抗腐蚀能力(此外,大多数稀土合金还有潜在的抗癌特性~)。是故,考虑到血管内植入支架所需的渐进降解持续时间,其需与生物应激环境中病变区域的再生或愈合进程相匹配,在有限的时间内给病变血管提供持久和足够的机械支撑,直至降解;此处,可降解镁合金的优异机械性能和适当的生物相容性,显示出了它相较于生物可降解聚合物(如PLGA)和陶瓷等材料的优势。
但是,镁合金存在两个问题:1)降解速度比预期快得多(表面改性、优化合金成分);2)镁合金的六方晶体结构和有限滑移系统,导致其延展性差(退火、固溶、热处理、优化合金成分),很难进行精确的塑性变形。
图5 镁的六方晶体结构
DREAMS 2G支架就做过BIOSOLVE-II、-III和-IV研究,Magnesium 2000上市后研究,Magmaris Multicenter Italian注册研究,等等。在第一个临床研究PROGRESS中,镁支架的安全性得到了验证,但是4月时临床驱动的靶病变血运重建率(CDTLR)很高(23.8%),并有0.83mm的节段内晚期管腔丢失(In-segment LLL),支架内再狭窄也被认为是支架失效和新生内膜增长所致。到了DREAMS 1G支架,虽然支架的机械性能得到了显著改善,并添加了紫杉醇药物,减少了1年CDTLR的发生,但其晚期管腔内丢失仍不理想(0.52mm)(所以药还是得加啊~)。DREAMS 2G支架则不仅在骨架设计方面进行了改进,还引入了药物-聚合物涂层,西罗莫司与可生物吸收的聚-L-丙交酯酸聚合物(Bioresorbable poly-L-lactide acid polymer)相结合,延长了镁骨架支架的稳定性。
图6 AMS-1和AMS-3.0支架的小梁横截面示意图(上),以及植入猪冠脉动脉模型28天后的光学显微镜下外观(下)。注意一代和三代支架相比,结构由矩形改成了方形,其厚度从165um减少到了120um
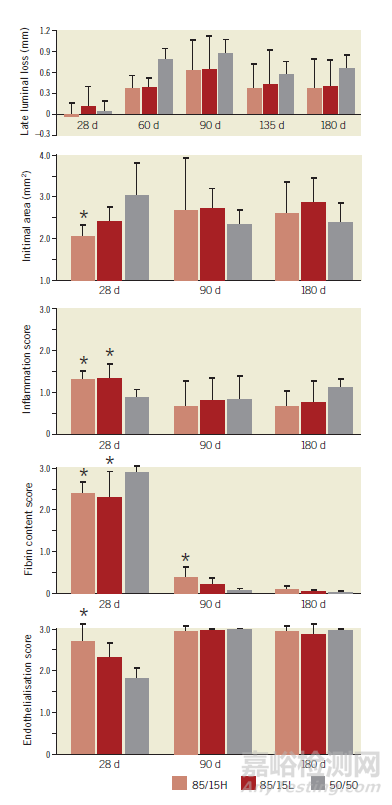
图7 三种AMS-3.0支架在大小上完全相同,但使用了不同的聚合物涂层设计
图8 三种不同设计的AMS-3.0支架猪模型中晚期管腔丢失、内膜面积、炎症评分、内膜纤维蛋白含量和内皮化评分的比较
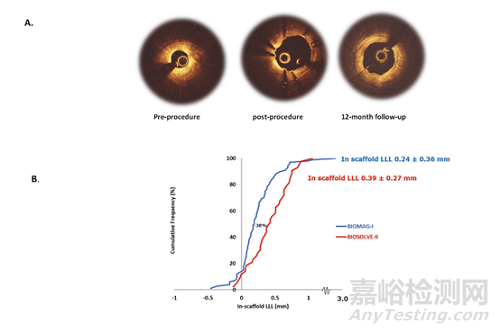
本次的BIOMAG-I是评估新一代DREAMS 3G支架的首个研究,此前瞻性、欧洲多中心、单臂的试验从2020年4月至2022年2月入选了116名患者,97.7%的支架成功释放。初步结果表明,第三代药物洗脱可吸收镁支架DREAMS 3G达到其设计目标,血管内成像显示其在6-12个月之间有良好的管腔保存。
图9 BIOMAG-I研究的OCT和LLL随访结果
那么,今天就写到这吧。人到中年,很容易觉得一事无成,心生颓废,重复劳作,前途无望,与大家共勉。
引用文献:
1. Michael Haude, Adrian Wlodarczak, Rene J. van der Schaaf, et al. A new resorbable magnesium scaffold for de novo coronary lesions, the DREAMS 3G: one-year results of the BIOMAG-1 first-in-human study. EuroIntervention. 2023;19:1-1.
2. To cite this article: Umer Masood Chaudry, Sravya Tekumalla, Manoj Gupta, Tea[1]Sung Jun & Kotiba Hamad (2021): Designing highly ductile magnesium alloys: current status and future challenges, Critical Reviews in Solid State and Materials Sciences, DOI: 10.1080/10408436.2021.1947185.
3. Eric Wittchow, Nina Adden, Johannes Riedmuller, et al. Bioresorbable drug-eluting magnesium-alloy scaffold: design and feasibility in a porcine coronary model. EuroIntervention. 2013;8:1441-1450.