今日头条
信立泰ARNi类降血压新药报产。信立泰自主研发的ARNi类小分子1类新药沙库巴曲阿利沙坦钙片(S086)的上市申请获CDE受理,推测适应症为治疗轻、中度原发性高血压。今年1月,S086已在治疗轻、中度原发性高血压适应症的III期临床中达到主要终点。与奥美沙坦酯(20mg)相比,接受S086(240mg、480mg)治疗12周后患者平均诊室坐位收缩压的降幅均值高1.90、5.04mmHg。
国内药讯
1.复星引进创新型肉毒素报新NDA。复星医药从Revance公司引进的注射用A型肉毒毒素(RT002,DaxibotulinumtoxinA-lanm)的第二个适应症上市申请获CDE受理,用于治疗成人颈部肌张力障碍。RT002是一种长效肽制剂神经调节剂,已获FDA批准上市,用于改善成人中重度皱眉纹。今年4月,RT002也在中国递交了用于改善成人中重度皱眉纹的上市申请。
2.创胜CLDN18.2抗体获批胃癌国际III期临床。创胜集团宣布其Claudin18.2单抗Osemitamab联合PD-1抗体纳武利尤单抗与化疗治疗HER2阴性、CLDN18.2表达、局部晚期或转移性胃或胃食管(G/GEJ)结合部腺癌患者的国际III期临床(TranStar 301)IND申请分别获得CDE和韩国MFDS批准。公布于ESMO GI2023年会的I/II期临床(NCT04495296)最新数据显示,该药联合卡培他滨和奥沙利铂(CAPOX)一线治疗,预计中位无进展生存期达到9.5个月。
3.诺贝仁褪黑素儿童失眠拟纳入优先审评。诺贝仁医药申报的褪黑素颗粒因“符合儿童生理特征的儿童用药品新品种、剂型和规格”被CDE拟纳入优先审评,适应症为儿童期伴随神经发育障碍的入睡困难的改善。这是一款褪黑激素受体激动剂,旨在通过褪黑素来抑制神经的兴奋性,使血压下降,心跳速度减慢,提高睡眠质量,让心脏得到休息,消除疲劳。2020年3月,该新药已在日本获批上市,商品名为Melatobel。
4.罗氏CFB靶向反义疗法获批肾病临床。罗氏从Ionis公司引进的靶向补体因子B(CFB)的反义疗法RO7434656注射液(IONIS-FB-LRx)获国家药监局临床默认许可,拟开发用于IgA肾病的治疗。去年11月,IONIS-FB-LRx已在用于治疗IgA肾病的II期临床达到主要终点,IONIS-FB-LRx治疗29周后,患者的蛋白尿较基线平均减少44%。罗氏拥有该药物在全球范围内的开发和商业化授权。
5.恒瑞3款放射性诊疗产品获批临床。恒瑞医药子公司天津恒瑞医药申报的3款1类新药获批临床。其中,HRS-4357注射液为一款放射性治疗类创新药,拟开发用于既往接受过雄激素受体(AR)通路抑制剂和紫杉烷类化疗的前列腺特异性膜抗原(PSMA)阳性的转移性去势抵抗性前列腺癌(mCRPC)。HRS-9815注射液和HRS-9815注射液制备用药盒则适用于成人前列腺癌患者的PSMA阳性病灶的正电子发射断层扫描(PET)。
6.百济神州DGKζ抑制剂报IND。百济神州1类化药BGB-30813片的临床试验申请获CDE受理。BGB-30813是一种新型DGKζ抑制剂,具有增强DAG下游信号通路的潜力,可以激活T细胞,从而增强肿瘤杀伤作用。今年6月,百济神州在Clinicaltrials.gov网站上登记注册一项BGB-30813单药或与PD-1替雷利珠单抗联用治疗晚期或转移性实体瘤的I期临床试验,拟评估其安全性、耐受性、药动学、药效学和初步抗肿瘤活性。
国际药讯
1.卫材/渤健AD新药获FDA完全批准。卫材与渤健开发的阿尔茨海默病(AD)抗体疗法Leqembi(lecanemab)获FDA批准由加速批准转为完全批准。Leqembi通过与可溶性Aβ聚合体结合,可中和并清除具有毒性的可溶性寡聚体。在Ⅲ期临床(CLARITY AD)中,lecanemab与安慰剂组相比,显著降低AD患者CDR-SB评分的增加速度,能够延缓(大约延缓两到三年)AD患者进展到更严重的疾病阶段。
2.创新HER2/3双抗获肺癌突破性疗法认定。Merus公司创新双抗zenocutuzumab获FDA授予突破性疗法认定,用于治疗晚期不可切除或转移性NRG1融合(NRG1+)非小细胞肺癌。Zenocutuzumab可同时与HER2和HER3受体相结合,阻止HER2和HER3形成二聚体,从而阻断神经调节蛋白的信号传导,对NRG1+癌症具有治疗潜力。一周前,它刚刚获得FDA授予用于治疗NRG1融合阳性胰腺癌的突破性疗法认定。
3.罗氏PD-L1抑制剂肺癌Ⅲ期临床积极。罗氏在《柳叶刀》上发表PD-L1抑制剂Tecentriq(atezolizumab)一线治疗非小细胞肺癌的Ⅲ期临床最新数据。与非铂类化疗相比,atezolizumab显著改善患者的总体生存率【中位总生存期:10.3个月(95% CI 9.4-11.9)vs9.2个月(95% CI 5.9-11.2)】,2年生存率为24%(vs12%),3-4级治疗相关不良事件发生率为16%(vs33%)。
4.默沙东启动癌症疫苗+K药III期临床。默沙东宣布启动癌症疫苗mRNA-4157 (V940)联合PD-1疗法帕博利珠单抗(Keytruda)用于一线治疗II-IV期黑色素瘤的首个III期临床(V940-001)试验。mRNA-4157是针对每个癌症患者的独特肿瘤突变开发的一款个性化肿瘤新抗原疫苗。在IIb期临床KEYNOTE-942/mRNA-4157-P201中,与单独Keytruda相比,mRNA-4157联合辅助治疗使肿瘤产生远处转移或死亡的风险降低65%。
5.罗氏撤回RET抑制剂一项适应症。罗氏旗下基因泰克在美国撤回RET抑制剂Gavreto(普拉替尼)用于治疗晚期RET突变甲状腺髓样癌的加速批准上市许可。基因泰克表示,其撤回适应症的决定并非由于Gavreto的任何新的安全性或有效性数据或产品质量问题,在美国获批的其他适应症不受影响。据悉,罗氏基于战略原因已于今年2月终止与Blueprint公司关于Gavreto的全球合作,将该药物的全球权益归还给Blueprint。
6.Teva计划出售API业务部门。据外媒Endpoints披露,Teva正在考虑出售其原料药(活性药物成分,API)业务。Teva已聘请了顾问来考察是否有买方愿意以约20亿美元的价格收购该业务部门。Teva有着强大的API业务供应链,目前该业务部门已在全球14个生产基地拥有约4000名员工,生产约350种产品。2023年5月,Teva曾宣布了一项“转向增长”战略,为了更好地占领每年增长约6%的API市场,其考虑将API业务独立出来。
医药热点
1.河北省将再建一大型医院。近日,河北省沧州市发改委批复沧州市新华区人民医院建设项目建议书,原则同意沧州市新华区卫生健康局开展沧州市新华区人民医院建设项目前期工作。该项目总投资约106710万元;规划编制床位436张,总建筑面积约115582㎡;其中地上建筑面积约69782㎡, 包括医疗综合楼、住院楼、感染楼、后勤保障楼、附属配套用房、地下车库出入口等。
2.国家级医疗应急工作专家组成立。国家卫健委日前发布《关于成立国家卫生健康委医疗应急工作专家组的通知》,旨在进一步发挥国家级专家在医疗应急工作中的技术支持和业务指导作用,提高医疗应急处置能力和水平,保障和维护人民群众生命安全和身体健康。《通知》明确,国家级医疗应急工作专家组包括急诊医学科、重症医学科、流行病学等22个组。
3.我国严打非法应用人类辅助生殖技术。国家卫健委等14部门联合制定《开展严厉打击非法应用人类辅助生殖技术专项活动工作方案》,强化与人类辅助生殖技术应用相关的全链条管理:要求建立健全准入和退出机制,严格规范人类辅助生殖技术审批和校验管理,加大对医疗机构和医务人员违规开展人类辅助生殖技术的行政处罚力度;严禁辅助生殖技术从业人员在不具备资质或者不具备相应技术类别的机构开展辅助生殖技术服务;严禁互联网医院开具属于药品网络销售禁止清单所列的辅助生殖常用药品处方。
评审动态
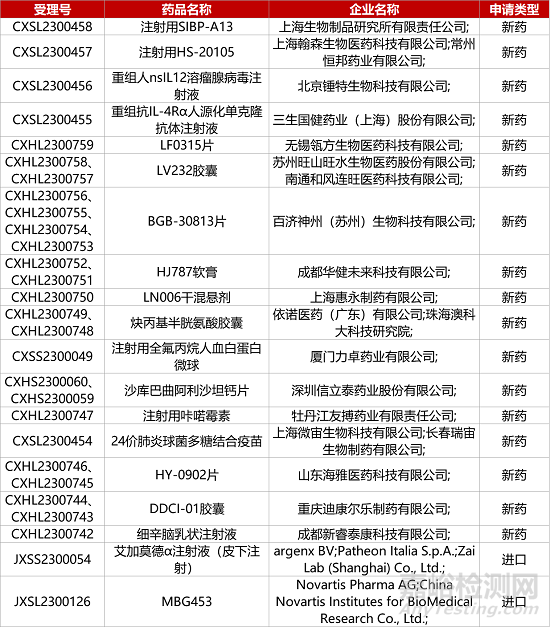
1. CDE新药受理情况(07月09日)
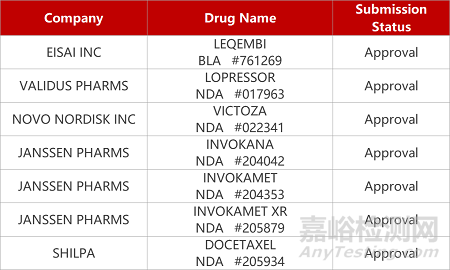
2. FDA新药获批情况(北美07月06日)