今日头条
亚虹DBH抑制剂国内获批UC临床。亚虹医药1类化药APL-1401胶囊获国家药监局批准开展Ib期试验,评估用于中重度活动性溃疡性结肠炎(UC)患者的安全性、耐受性、药代动力学和初步有效性。APL-1401是一种多巴胺β-羟化酶(DBH)抑制剂,能够提高多巴胺(DA)并降低去甲肾上腺素(NE)浓度,恢复肠道免疫稳态正常。去年11月,FDA已批准APL-1401开展用于UC患者的Ib期临床。
国内药讯
1.礼来CDK4/6抑制剂中国获批新适应症。礼来CDK4/6抑制剂阿贝西利片(商品名:唯择)获国家药监局批准拓展适应症,联合内分泌治疗(ET)用于HR+/HER2-、淋巴结阳性、高复发风险的早期乳腺癌成年患者的辅助治疗。在Ⅲ期临床monarchE中,这一联合疗法可将乳腺癌复发的风险降低32%。此前,该新药已被NMPA批准用于治疗HR+/HER2-、局部晚期或转移性乳腺癌;以及联合ET方案,用于辅助治疗HR+/HER2-、淋巴结阳性、高复发风险且Ki-67≥20%早期乳腺癌。
2.诺和诺德凝血因子VIII拟纳入优先审评。诺和诺德长效重组凝血因子VIII(FVIII)注射用培图罗凝血素α(turoctocog alfa pegol,N8-GP)获CDE拟纳入优先审评,用于成人和儿童血友病A患者:按需治疗及控制出血事件;围手术期管理;常规预防治疗以防止或减少出血事件的发生。临床数据显示,每4天一次的预防性注射N8-GP治疗,能够将年出血率维持到每年1.18次的低水平。
3.圣诺实体瘤RNAi疗法早期临床积极。Sirnaomics公司RNAi疗法STP707治疗多种实体瘤的美国Ⅰ期临床结果积极。STP707由靶向TGF-β1和COX-2 mRNA的两个siRNA寡核苷酸组成,并与组氨酸-赖氨酸共聚肽(HKP+H)的载体结合配制成纳米颗粒制剂。最新数据显示,STP707在可评估患者中达到74%的疾病稳定,没有患者表现出剂量限制性毒性。该项试验将继续进行剂量爬坡研究。
4.信诺维HPK1激酶抑制剂获批临床。信诺维自主研发的造血祖细胞激酶1(HPK1)选择性小分子抑制剂XNW21015获国家药监局批准,开展用于晚期/转移性恶性实体瘤治疗的临床试验。XNW21015能有效抑制HPK1驱动的SLP76磷酸化,促进T细胞活化并增加T细胞IL-2的分泌,单用或者与抗PD-1抗体联用具有协同抗肿瘤作用。XNW21015也是信诺维第9款临床阶段产品。
5.未知君生物引进基因工程菌报IND。未知君生物从Aurealis公司引进的1类生物药AUP1602-C(AUP-16)的临床试验申请获CDE受理。AUP-16是一款基因工程化的乳酸乳球菌,其内部搭载多种再生因子的编码基因,可表达人类碱性成纤维细胞生长因子(FGF2、bFGF)、白细胞介素4(IL-4)和巨噬细胞集落刺激因子(CSF1、mCSF)。未知君生物拥有AUP-16在大中华区的独家权利,用于治疗糖尿病足溃疡、其他慢性伤口以及炎症性疾病。
国际药讯
1.罗氏ALK抑制剂早期肺癌III期临床积极。罗氏ALK抑制剂阿来替尼治疗ALK阳性、早期非小细胞肺癌(NSCLC)的III期ALINA研究达到主要终点。与以含铂化疗相比,阿来替尼辅助治疗可以显著降低完全切除的IB(肿瘤≥4cm)至IIIA期ALK阳性NSCLC患者的疾病复发和死亡风险;目前总生存期(OS)数据尚不成熟;未观察到意外的安全性结果。详细结果将在医学会议上公布。
2.CD123靶向药获BPDNC罕用药资格。美纳里尼集团("Menarini")与Nippon Shinyaku公司开发的CD123靶向药物ELZONRIS®(Tagraxofusp)获日本厚生劳动省授予罕用药资格认定,用于母浆细胞样树突状细胞瘤(BPDCN)治疗。Tagraxofusp由人IL-3与截短的白喉毒素(DT)进行重组融合而成,IL-3结构域能够将细胞毒性DT片段引导至表达CD123的肿瘤细胞。在美国和欧洲,ELZONRIS®是首款且是唯一一款获批用于BPDCN治疗的靶向药。
3.AZ/第一三共HER2-ADC获BTD认定。阿斯利康与第一三共开发的HER2-ADC新药Enhertu(trastuzumab deruxtecan)获FDA授予两项突破性疗法认定(BTD),用于治疗不可切除或转移性HER2阳性(IHC 3+)实体瘤成人患者,以及用于治疗HER2阳性(IHC 3+)转移性结直肠癌经治患者。今年7月,Enhertu已在治疗多种HER2表达晚期实体瘤经治患者的II期DESTINY-PanTumor02研究中达到无进展生存期(PFS)和总生存期(OS)改善两个疗效终点;且未发现新的安全性问题。
4.BMS分子胶早期临床见刊NEJM。百时美施贵宝新型E3泛素连接酶cereblon调节剂mezigdomide用于多发性骨髓瘤(MM)患者的Ⅰ/Ⅱ期临床数据发布于《新英格兰医学杂志》。数据显示,mezigdomide联合地塞米松治疗达到41%的总缓解(95% CI:31-51),中位缓解持续时间为7.6个月(95% CI:5.4-9.5;数据尚不成熟),中位无进展生存期为4.4个月(95% CI,3.0-5.5),中位随访7.5个月(0.5-21.9)。未观察到非预期毒性作用。
5.罗氏KRAS G12C抑制剂早期临床积极。罗氏旗下基因泰克KRAS G12C抑制剂divarasib(GDC-6036)在《新英格兰医学杂志》发表用于治疗KRAS G12C突变实体瘤的Ⅰ期试验研究结果。在非小细胞肺癌(NSCLC)患者中,divarasib达到53.4%(95% CI:39.9-66.7)的确认缓解率(ORR),中位无进展生存期(PFS)为13.1个月;在结直肠癌患者中,确认ORR为29.1%(95% CI,17.6-42.9),中位PFS为5.6个月;治疗相关不良事件发生率93%,3级和4级事件发生率分别为11%和1%。
6.FDA拒绝批准贝伐珠单抗眼用制剂上市。Outlook公司贝伐珠单抗眼用制剂ONS-5010用于治疗湿性年龄相关性黄斑变性(wAMD)的上市申请收到FDA完整回复函(CRL)。FDA给出的原因是“与化学、生产和控制(CMC)”有关。在III期临床NORSE ONE中,ONS-5010组患者达到BCVA评分增加15个字母以上的比例显著高于雷珠单抗组(意向性治疗人群:41.7%vs23.1%,P=0.0052;符合方案人群:41.0%vs24.7%,P=0.0409)。
医药热点
1.姜勇出任郑大一附院院长。9月1日,郑州大学第一附属医院院长聘任仪式在该院郑东院区举行。姜勇受聘担任郑州大学第一附属医院院长。公开资料显示,姜勇为教授、博士生导师,长江学者特聘教授,国家“杰青”,原南方医科大学基础医学院病理生理学教研室主任。长期从事炎症相关的细胞信号调控及其分子机制的研究,对于炎症信号转导机制及其相关信号分子的鉴定和功能研究作出了重要贡献。
2.广东省开设首个核辐射健康门诊。为方便市民对辐射类疾病的咨询及就诊,广州市第十二人民医院日前于健康管理中心开设了“核与辐射健康门诊”。这也是广东省首家系统性、专业化的辐射类疾患咨询及诊疗门诊。该门诊目前面向有排查核辐射风险的人群,无论大人小孩均可检测。需要做的检查主要有两项:淋巴细胞染色体畸变分析与淋巴细胞微核检测,相关筛查检测费用目前为自费,花费约在一千元左右。
3.2家中国企业上榜全球医疗器械百强榜。近日,国外知名医疗器械行业媒体Medical Design & Outsourcing发布了最新的2023年全球医疗器械公司百强榜单,该榜单排名以百强公司2022财年的营收进行排名。榜单显示,美敦力、强生医疗、西门子医疗、麦朗、飞利浦、史赛克、GE医疗、嘉德诺、百特、雅培位列前十。在本次百强榜名单中,有两家中国企业上榜,即迈瑞医疗(27)和微创医疗(77)。
评审动态
1. CDE新药受理情况(08月2日)
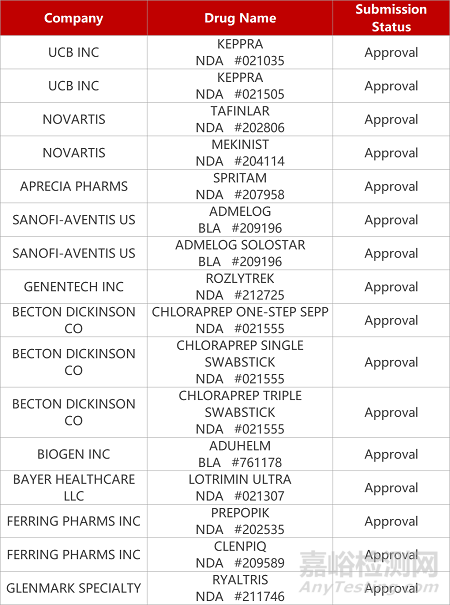
2. FDA新药获批情况(北美08月31日)