您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-05-12 18:49
近日,美敦力(纽约证券交易所代码:MDT)宣布其 PulseSelect 脉冲消融(PFA) 系统获得日本监管批准。日本厚生劳动省是在关键的 PULSED AF 试验之后批准的,该试验是一项全球多中心 IDE 研究,日本的研究中心也参与其中。
该产品于2023年12月获得美国FDA批准用于治疗阵发性和持续性心房颤动,成为第一款FDA批准的PFA系统。
据美敦力称,全球已有250多名医生使用 PulseSelect 成功治疗了3000多名患者,与公司的双向 10F FlexCath Contour 鞘管一起使用。
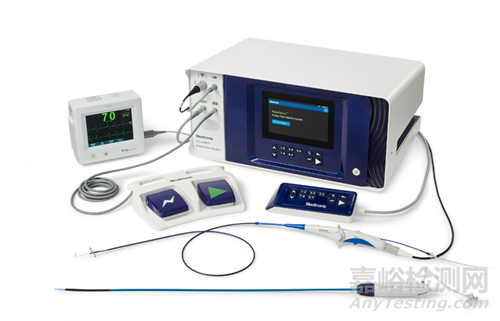
PulseSelect 脉冲消融系统
PulseSelect 脉冲电场消融系统由可操纵的多电极环状消融导管、自定义FPA生成器、心电图、桌边控件、直径10Fr的FlexCath Contour 双向鞘管等组成。图片
优先对肺静脉进行消融,依靠脉冲电场而非热效应,避免损害消融部位周围的组织。

消融导管采用专有的双向波形和独特的内导线设计。导管头部有多个电极,可以通过伸缩变成“圆盘状”(直径25毫米),因操作便利的考虑设计为前倾20°。
产品特点:
即插即用:可以和任何标测系统搭配使用,可以直接和X射线透视成像搭配使用。
内置安全功能:搭载膈神经测试脉冲,膈神经测试脉冲电压很低,在开始正式进行消融前可使用这种测试电压评估消融导管是否靠近膈神经。

固定间距的九个电极:由于导管头部的九个电极形成圆盘状后彼此之间的间距是固定的,因此产生的电场一致,方便进行连续消融。
此外,这九个电极还可以用于起搏和感知。
导管直径小:消融导管的直径小,只有9Fr(外面套着一个直径10Fr的鞘管),有利于导管轻松进入各种解剖结构。
软件升级
美敦力还表示,PulseSelect 有了新的软件升级,其中包括自动给药模式,进一步简化工作流程,为医生在手术过程中控制 PFA 提供更多选择。

美敦力已经完成了欧洲、加拿大现有系统的升级,美国的系统升级已经启动,并将在获得批准后推广到包括日本在内的更多国家。
真实世界数据
2023美国ACC年会上,PulseSelect 系统公布了其PULSED AF Pivotal 临床研究数据,均超出了安全性能目标预期。
数据显示,应用 PulseSelec实行房颤消融术,不良事件发生率仅 0.7%,是目前递交给 FDA 的 PFA 临床试验及其他 PFA 临床研究中最低的。
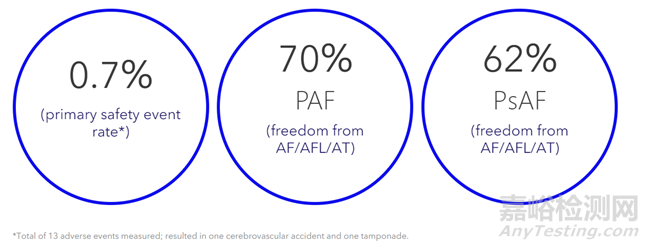
12个月内,阵发性组的房性心律失常无复发率为70%,持续性组的无复发率为62%。
此外,临床成功率在每个患者群中都至少达到了80%(阵发性组为80%,持续性组为81%)。
Pulsed AF 研究结果显示出PulseSelect系统的安全性和有效性。
此外,PulseSelect系统在两组中都超过了12个月的疗效阈值,在阵发性房颤患者中表现出的疗效总计为66%,在持续性房颤患者中为55%。
高管评价
美敦力心脏消融解决方案业务总裁Rebecca Seidel在一份新闻稿中说:
“我们在美国、欧洲和加拿大等各个市场都看到了对 PulseSelect 的极大热情和应用。许多PulseSelect的用户都对它的安全性、易操作性及其灵活性给予了一致的好评。现在,PulseSelect 扩展到日本市场,这对医生和他们所服务的患者来说都是一个好消息,他们应该得到最先进、安全和高效的房颤治疗。”
PFA的巨头之争
脉冲电场消融(PFA)也被称为不可逆电穿孔,是指在短时间内将高电压电脉冲作用于细胞膜的磷脂双分子层,导致跨膜电位形成,产生不稳定的电势,使细胞膜形成不可逆的穿透性损伤,产生纳米级孔隙,进而引起细胞膜渗透率变化,破坏细胞内环境稳态,最终导致细胞凋亡,达到非热消融的目的。
FMI数据显示,从2021年到2022年,全球脉冲场消融市场经历了48.6%的复合年增长率,到2023年市场规模达到130万美元。从2023年到2033年,全球脉冲场消融行业预计将以24.2%的复合年增长率增长。
正是由于脉冲消融的高成长性,它也被认为是下一代颠覆性消融技术,美敦力、强生、波士顿科学等跨国械企均已开始布局相关产品管线。
2023年12月,美敦力脉冲电场消融设备PulseSelect获得FDA批准,成为首个获得FDA批准的脉冲场消融技术。此前11月,PulseSelect PFA获得CE标志。
同月,国内PFA也取得突破,锦江电子“一次性使用心脏脉冲电场消融导管PulsedFA”和“心脏脉冲电场消融仪LEAD PFA”创新产品正式获得NMPA批准,是国内首个获批的心脏PFA类产品。
随后,波士顿科学的脉冲电场消融设备Farapulse在2024年1月获得FDA批准;2021年初,Farapulse PFA 系统获 CE 批准上市。
强生的脉冲电场消融设备 Varipulse 在2024年1月获得日本厚生劳动省(MHLW)批准上市,适用于治疗症状性药物难治性复发性阵发性房颤。这是日本批准的首款PFA产品。公司计划在2024年提交FDA申请。

▲参考Medtrend医趋势
值得一提的是,美敦力、强生、波士顿科等三家巨头的PFA产品均已进入NMPA创新医疗器械特别审查程序。
国内目前有近50家企业正在研发PFA心脏消融系统,德诺电生理、北芯医疗的PFA产品也已进入NMPA特别审查程序。惠泰医疗、玄宇医疗、艾科脉医疗、迈微医疗、鑫律通、洲瓴医疗、远山医疗、心航路医学等企业也纷纷布局PFA。
然而,对于一个正在开启商业化落地的蓝海赛道,随着国内外诸多厂商PFA产品获批,蓝海变红海下如何突围的问题值得各个入局者仔细考量。
关于美敦力

美敦力 (Medtronic,NYSE:MDT) 成立于1949年,总部位于美国明尼苏达州明尼阿波利斯市,是全球领先的医疗科技公司,拥有超过95000名员工。
美敦力的创新解决方案已拓展至70余种重点疾病领域,致力于为慢性疾病患者提供终身的治疗方案,每一秒钟,全球就有2位患者受益于美敦力的医疗技术或疗法。
美敦力主要业务有心血管、医疗外科、神经科学和糖尿病业务四块,其中心血管占比最高。美敦力卖什么?心血管产品线超全盘点
以2023年财报为例,公司整体收入312.27亿美元,在全球医疗器械企业营收中排名第一。其中心血管业务营收115.73亿美元,占比37.06%,包括心脏节律和心力衰竭(CRHF)、结构性心脏和主动脉(SHA)以及冠状动脉和外周血管(CPV)三个部门。

▲2023年财报(源自公司官网)

来源:心未来


