您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-03-01 12:43
摘 要: 建立超高效液相色谱-串联质谱联用法测定丹桂香颗粒中马兜铃酸I的含量。采用ACQUITY UPLC® BHE C18柱(50 mm×2.1 mm,1.7 μm)色谱柱分离,以0.1%(体积分数)甲酸水溶液(含5 mmol/L甲酸铵)-乙腈作为流动相进行梯度洗脱,柱温为30 ℃,流量为0.3 mL/min。在电喷雾离子源正离子模式,多反应监测模式下进行扫描检测,以外标法定量。马兜铃酸I的质量浓度在0.1~40 ng/mL范围内与色谱峰面积线性关系良好,相关系数为0.999 6。无糖型、含糖型样品的平均回收率分别为89.4%、91.3%,测定结果的相对标准偏差分别为3.2%、1.2%(n=9)。该方法操作简单、专属性强、准确度高,可实现对丹桂香颗粒中马兜铃酸Ⅰ的定量检测。
关键词: 超高效液相色谱-串联质谱法; 丹桂香颗粒; 马兜铃酸I
丹桂香颗粒是由炙黄芪、桂枝、吴茱萸、肉桂、细辛等二十三种药材通过挥发油提取、乙醇提取和水煎煮工艺浓缩,后加入蔗糖(或不加蔗糖)与糊精喷雾而成。该颗粒具有益气温胃、散寒行气、活血止痛之功效,临床常用于脾胃虚寒、滞血瘀所致的胃脘痞满疼痛、食欲减退、嗳气、腹胀以及慢性萎缩性胃炎等相关症状[1]。丹桂香颗粒处方中包含属于马兜铃科的细辛植物。马兜铃科植物普遍含有马兜铃酸I成分。已有研究表明[2‒15],马兜铃酸I具有高度的肾毒性和致癌性,能够诱导腺嘌呤和胸腺嘧啶交换,导致基因突变,从而引起肝癌,因此近年来,含马兜铃酸中药的安全性问题引起广泛关注。2003年,原国家食品药品监督管理局要求将龙胆泻肝丸处方中的关木通替换为木通,以避免关木通中的马兜铃酸对人体造成伤害。2012年,马兜铃酸被国际癌症研究机构确定为I类致癌物[8‒9]。此外,《中华人民共和国药典》2015年版开始收载了细辛药材及饮片的马兜铃酸I的限量检查,以实现细辛中药材及饮片的毒性成分质量管控。《中国药典》2020年版对九味羌活丸中马兜铃酸I限量进行控制,但并未对其他含细辛中成药马兜铃酸I成分进行规范。目前马兜铃酸I限量的检测方法主要为液相色谱法[10‒12]、高效液相色谱-串联质谱法等[13‒17],因中成药处方、工艺差异较大,上述方法无法直接应用至丹桂香颗粒中马兜铃酸I的成分测定。
笔者建立了超高效液相色谱-串联质谱联用法测定丹桂香颗粒中马兜铃酸I的含量,以丹桂香颗粒为研究对象,通过优化提取条件并研究基质对测试的干扰,对马兜铃酸I的含量进行了定量分析。该方法操作简单、专属性强、定性定量准确,为开发其他含细辛类中成药中马兜铃酸I含量测定提供思路,确保药品安全使用。
1. 实验部分
1.1 主要仪器与试剂
超高效液相色谱-三重四极杆质谱联用仪:ACQUITY XEVO TQ-S型,美国沃特世公司。
电子天平:XPE205型,感量为0.01 mg,瑞士梅特勒-托利多仪器有限公司。
数控超声清洗器:KQ-500DE型,昆山超声仪器有限公司。
马兜铃酸I对照品:质量分数为99.1%,批号为110746-201912,中国食品药品检定研究院。
甲酸:色谱纯,山东西亚化学股份有限公司。
甲酸铵:质谱纯,美国ACS恩科化学公司。
乙腈:质谱纯,美国赛默飞世尔公司。
丹桂香颗粒样品:含糖型12批,编号分别为S1~S12,无糖型10批,编号分别为S13~S22,均来源于Z公司。
阴性样品:按照中国药典中丹桂香颗粒标准中的处方,不加细辛,其余按标准中的制法进行炮制,得到不含细辛的阴性样品(含糖型/无糖型)。
实验用水为超纯水。
1.2 仪器工作条件
1.2.1 色谱条件
色谱柱:ACQUITY UPLC® BHE C18柱(50 mm×2.1 mm,1.7 μm,美国沃特世科技有限公司);流动相:A相为乙腈,B相为0.1%(体积分数)甲酸溶液(含5 mmol/L的甲酸铵),流量为0.3 mL/min;洗脱方式:梯度洗脱;洗脱程序:0~10 min时,流动相B的体积分数由65%逐渐减少到62%,10~10.5 min时,流动相B的体积分数由62%逐渐增加到65%,10.5~12 min时,流动相B的体积分数保持为65%;柱温:30 ℃;进样体积:1 μL。
1.2.2 质谱条件
离子源:电喷雾离子源(ESI);扫描模式:正离子模式;监测模式:多反应监测扫描(MRM);离子源温度:110 ℃;脱溶剂气温度:4 50 ℃;锥孔气:氮气,流量为50 L/h;毛细管电压:2.80 kV;碰撞电压:10 V。定性离子对为m/z 359.0,296.0,定量离子对为m/z 359.0,297.9。
1.3 样品处理
取丹桂香颗粒,研细,精密称取2.7 g (含糖型)或3.6 g (无糖型),置于具塞锥形瓶中,精密加入70%甲醇25 mL,称定质量,超声处理(功率240 W,频率40 kHz) 30 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,即得样品溶液(含糖型/无糖型)。
1.4 溶液配制
标准储备溶液:精密称取马兜铃酸I对照品约10 mg,置于100 mL容量瓶中,加入70%甲醇溶解并定容至标线,摇匀;精密量取2.5 mL,置于50 mL容量瓶中,用70%甲醇稀释至标线,摇匀;精密量取10 mL,置于200 mL容量瓶中,用70%甲醇稀释至标线,摇匀,制得标准储备溶液。
系列标准工作溶液:精密吸取标准储备溶液0.04、0.08、0.2、0.4、0.8、2、4、8、16 mL分别置于100 mL容量瓶中,用70%甲醇作溶剂稀释至标线,摇匀,得质量浓度分别为0.1、0.2、0.5、1、2、5、10、20、40 ng/mL的系列标准工作溶液。
阴性样品溶液:取阴性样品,研细,取2.7 g (含糖型)或3.6 g (无糖型),精密称定,按1.3样品处理方法,制成阴性样品溶液。
阴性加标溶液:取阴性样品,研细,取2.7 g (含糖型)或3.6 g (无糖型),精密称定,置具塞锥形瓶中,精密加入20 ng/mL的马兜铃酸I标准储备溶液25 mL,称定质量,超声处理(功率240 W,频率40 kHz)30 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,即得阴性加标溶液(含糖型/无糖型)。
1.5 实验步骤
分别取系列标准工作溶液,阴性样品溶液和样品溶液,注入液相色谱-质谱联用仪中测定。分别以马兜铃酸I的质量浓度为横坐标,对应的峰面积为纵坐标,进行线性回归分析,以标准曲线法计算样品中马兜铃酸I的含量。
2. 结果与讨论
2.1 样品提取条件优化
2.1.1 提取方式
取丹桂香颗粒,研细,按1.3样品处理方式,分别采用加热回流30 min和超声提取30 min两种提取方式,考察不同的提取方式对提取效率的影响,测定结果见表1。由表1可知,两种方式的提取效率差异较小,鉴于超声提取方法更加简便,因此提取方法选取超声提取法。
表1 不同提取方式的提取效率
Tab. 1 Examination of Extraction Methods

2.1.2 提取溶剂
按1.3样品处理方式,分别采用50%甲醇、70%甲醇、甲醇作为提取溶剂,考察不同溶剂的提取效率,测定结果如图1所示。从图1中可以看出,70%甲醇溶液的提取效率最好,因此选择70%甲醇作为提取溶剂。

图1 不同提取溶剂的提取效率
Fig. 1 Extraction efficiency of different extraction solvents
2.1.3 提取时间
选择70%甲醇作为提取溶剂,考察不同超声提取时间对提取效率的影响,测定结果如图2所示。从图2中可以看出,超声提取30 min时提取效率即达最高,因此选择超声提取时间为30 min。

图2 不同提取时间的提取效率
Fig. 2 Extraction efficiency at different extraction times
2.1.4 提取溶剂体积
选择70%甲醇作为提取溶剂,超声提取30 min,考察不同提取溶剂体积提取溶剂对提取效率的影响,测定结果如图3所示。从图3中可以看出,25 mL 70%甲醇提取效率最高,因此选择提取溶剂的体积为25 mL。
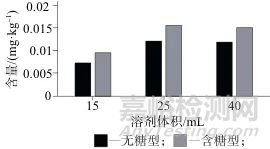
图3 不同提取溶剂体积的提取效率
Fig. 3 Extraction efficiency of different extraction solvent volumes
2.2 流动相的选择
以0.1%甲酸水溶液-乙腈体系作为流动相,结果发现离子对359.0,297.9和359.0,296.0的响应灵敏度较低,在0.1%甲酸水溶液中加入甲酸铵,增加了体系中铵离子浓度,电离强度增强,相应离子对灵敏度增加了4~5倍,因此最终选择0.1%甲酸水溶液(含5 mmol/L甲酸铵)-乙腈体系作为流动相。
2.3 基质效应考察
采用Matuszewski等[18]报道的方法对基质效应进行评估。取标准溶液和阴性加标样品溶液,在1.2仪器工作条件下分析检测,得到阴性加标溶液和标准溶液的峰面积的相对偏差分别为0.4%(含糖型)和2.5%(无糖型),基质效应为100.8%(含糖型)和95.3%(无糖型),表明基质效应影响较小。
2.4 专属性试验
分别取标准溶液、阴性样品溶液和样品溶液,注入液相色谱-质谱联用仪,记录色谱图,所得总离子流色谱图如图4所示。从图4中可以看出,阴性样品溶液谱图中,在与马兜铃酸Ⅰ对照品色谱保留时间相同的位置上无相应离子流,表明处方中其它药味对马兜铃酸Ⅰ的测定影响较小。

图4 阴性样品溶液、标准溶液、样品溶液总离子流色谱图
Fig. 4 Total ion flow chromatography of standard solution,sample solution and negative sample solution
2.5 线性方程与检出限
分别精密量取系列混合标准工作溶液,在1.2仪器工作条件下进样测定,以马兜铃酸I的质量浓度为横坐标,对应的色谱峰面积为纵坐标,进行线性回归分析,计算线性方程及相关系数。取质量浓度为1 ng/mL标准工作溶液,用70%甲醇逐级稀释,在1.2仪器工作条件下测定,以3倍信噪比对应的质量浓度作为检出限,以10倍信噪比对应的质量浓度作为定量限。结果表明,马兜铃酸的线性方程为y=1 151.3x-49.4,质量浓度的线性范围在0.1~40 ng/mL之间与色谱峰面积线性关系良好,相关系数为0.999 6,方法检出限为0.03 ng/mL,方法定量限为0.1 ng/mL。
2.6 加标回收与精密度试验
精密称取丹桂香颗粒细粉约3.6 g (无糖型,马兜铃酸I质量分数为0.015 9 mg/kg)和约2.7 g (含糖型,马兜铃酸I质量分数为0.020 0 mg/kg),各平行称取9份,分别精密加入低、中、高水平(5、10、20 ng/mL)的对照品溶液各3份,加标回收与精密度试验结果见表2。
表2 加标回收与精密度试验结果
Tab. 2 Results of spiked recoveries and precision test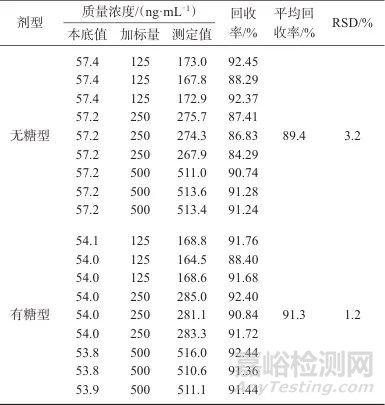
由表2可知,在无糖型和含糖型丹桂香颗粒中马兜铃酸I的平均回收率分别为89.4%、91.3%,测定结果的相对标准偏差分别为3.2%、1.2%(n=9),表明该方法具有较高的准确度和精密度,可准确测定丹桂香颗粒中的马兜铃酸I含量。
2.6 稳定性试验
取马兜铃酸Ⅰ标准溶液和样品溶液(无糖型/有糖型),于室温下分别放置0、2、4、8、12、16、20、24 h,精密量取不同放置时间的上述溶液,在1.2仪器工作条件下测定,稳定性试验结果见表3。
表3 稳定性试验结果
Tab. 3 Results of stability test
由表3可知,标准溶液中马兜铃酸Ⅰ色谱峰面积的RSD为2.6%,样品溶液中马兜铃酸Ⅰ色谱峰面积的相对标准偏差分别为2.6%(无糖型)、2.3%(含糖型),表明标准溶液和样品溶液均在24 h内稳定性良好。
3. 结语
建立了超高液相色谱-串联质谱测定丹桂香颗粒中马兜铃酸Ⅰ的方法。该方法专属性好、灵敏度高、准确度高、操作便利,可作为控制丹桂香颗粒中马兜铃酸Ⅰ限度的检测方法,为丹桂香颗粒的安全使用提供保证。
参考文献:
1 国家药典委员会.中华人民共和国药典(2020年版)[M].北京:中国医药科技出版社,2020.
Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China(2020 Edition)[M].Beijing:China Medical Science Press,2020.
2 XIAN Zhong,TIAN Jingzhuo,ZHAO Yong,et al. Differences in p38-STAT3-S100 A11 signaling after the administration of aristolochic acid I and IVa may account for the disparity in their nephrotoxicity[J]. Phytomedicine,2023,114:154 815.
3 汪毅.基于REV-ERBα和铁死亡的马兜铃酸I肾毒性机制研究[D].广州:暨南大学,2022.
WANG Yi. REV-ERBα and ferroptosis based mechanistic studies on aristolochic acid Ⅰ-induced renal injury[D]. Guangzhou:Jinan University,2022.
4 MENG Xiao,ZHANG Mengping,LIU Lingfei,et al. Rapid and robust analysis of aristolochic acid I in Chinese medicinal herbal preparations by surface enhanced raman spectroscopy[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2023,285:121 880.
5 曹雅静,温家欣,胡佳哲,等. HPLC-MS/MS法同时测定龙胆泻肝丸中高毒成分马兜铃酸I与鬼臼毒素[J].药物流行病学杂志,2023,32(5):522.
CAO Yajing,WEN Jiaxin,HU Jiazhe,et al. Simultaneous determination of aristolochic acid I and podophyllotoxin in Longdan Xiegan pills by HPLC-MS/MS[J]. Chinese Journal of Pharmacoepidemiology,2023,32(5):522.
6 谌晶晶,唐旭霞,徐慧芳,等.马兜铃酸对斑马鱼的耳毒性及肾毒性研究[J].听力学及言语疾病杂志,2020,28(1):57.
CHEN Jingjing,TANG Xuxia,XU Huifang,et al. The ototoxicity and nephrotoxicity of aristolochic acid in zebrafish[J]. Journal of Audiology and Speech Pathology,2020,28(1):57.
7 朱哿瑞,王静,黄恺,等.马兜铃酸Ⅰ致小鼠急性肝毒性的转录组学分析[J].临床肝胆病杂志,2021,37(10):2 389.
ZHU Gerui,WANG Jing,Huang Kai,et al. A transcriptomic analysis of acute hepatotoxicity induced by aristolochic acid I in mice[J]. Journal of Clinical Hepatology ,2021,37(10):2 389.
8 宗时宇,刘洋,孙婷婷,等.细辛毒性及其控制方法研究进展[J].中国药师,2020,23(5):154.
ZONG Shiyu,LIU Yang,SUN Tingting,et al. Research progress in the toxicity and control methods of Asari Radix et Rhizoma[J]. China Pharmacist,2020,23(5):154.
9 张翠英,俞捷,刘广学,等.3种马兜铃酸和2种马兜铃内酰胺在北细辛、华细辛及汉城细辛不同部位的分布及含量分析[J].世界科学技术-中医药现代化,2019,21(7):1 295.
ZHANG Cuiying,YU Jie,LIU Guangxue,et al. Distribution and content of 3 aristolochic acids and 2 aristololactams in different parts of Asarum heterotropoides var. mandshuricum,A. sieboldii and A. sieboldiivar. seoulense[J]. World Science and Technology Modernization of Traditional Chinese Medicine and Materia Medica,2019,21(7):1 301.
10 刘静,戴忠,程显隆,等.马兜铃酸类成分检测与分析研究进展[J].药物评价研究,2019,42(8):1 644.
LIU Jing,DAI Zhong,CHENG Xianlong,et al. Research progress on detection and analysis of aristolochic acids[J]. Drug Evaluation Research,2019,42(8):1 644.
11 庞逸辉,李岳,张宪.高效液相色谱法测定杜仲壮骨丸中马兜铃酸A[J].化学分析计量.2022,31(6):50.
PANG Yihui,LI Yue,ZHANG Xian. Determination of aristolochic acid A in Eucommia Ulmoides Strong Bone Pill by high performance liquid chromatography[J]. Chemical Analysis and Meterage, 2022,31(6):50.
12 黄晓燕,李荣玮,曾蒲军,等.十三味疏肝胶囊中马兜铃酸A的检测方法研究[J].药品评价,2021,18(23):1 421.
HUANG Xiaoyan,LI Rongwei,ZENG Pujun,et al. Determination of Aristolochic Acid A in Shisanwei Shugan Capsules[J]. Drug Evaluation,2021,18(23):1 421.
13 李靖云,孙辉,丁野,等. UPLC-MS/MS同时测定京制咳嗽痰喘丸中马兜铃酸Ⅰ、Ⅱ的含量[J].亚太传统医药,2024,20(4):16.
LI Jingyun,SUN Hui,DING Ye,et al. Simultaneous determination of aristolochic acid Ⅰand Ⅱin Jingzhi Kesou Tanchuan Pills by UPLC-MS/MS[J]. Asia-Pacific Traditional Medicine,2024,20(4):16.
14 王颖,刘繁红,杨燕丽,等. UPLC-MS/MS测定追风透骨丸中马兜铃酸类成分含量[J].中国现代中药,2023,25(10):2 207.
WANG Ying,LIU Fanhong,YANG Yanli,et al. Determination of aristolochic acids and their derivates in Zhuifeng Tougu Pills by UPLC-MS/MS[J]. Modern Chinese Medicine,2023,25(10):2 207.
15 毕武,梁晟,孙辉,等.超高效液相色谱-串联质谱法测定止咳化痰丸中马兜铃酸I和马兜铃酸Ⅱ的含量[J].中兽医医药杂志,2023,42(6):21.
BI Wu,LIANG Sheng,SUN Hui,et al. Determination of aristolochic acid Ⅰ and aristolochic Ⅱ in Zhisou Huatan pills by ultra-high performance liquid chromatography tandem mass spectrometry[J]. Journal of Traditional Chinese Veterinary Medicine,2023,42(6):21.
16 周颖,郑成,戴忠,等.超高效液相-串联质谱法测定镇脑宁胶囊中7种马兜铃酸类成分[J].中国药学杂志,2023,58(21):1 955.
ZHOU Ying,ZHENG Cheng,DAI Zhong,et al. Simultaneous Determination of seven aristolochic acid analogues in zhennaoning capsules by ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Chinese Pharmaceutical Journal,2023,58(21):1 955.
17 郭宁,赵雍,孙奕,等.朱砂莲中马兜铃酸类成分的UPLC-QTOF-MS/MS定性与定量分析[J].中国实验方剂学杂志,2021,7(11):162.
GUO Ning,ZHAO Yong,SUN Yi,et al. Qualitative and quantitative analysis of aristolochic acids in aristolochia cinnabarina dried root tubers by UPLC-QTOF-MS/MS[J]. Chinese Journal of Experimental Traditional Medical Formulae,2021,27(11):162.
18 WASIK A,MCOURT J,BUCHGRABER M. Simultaneous determination of nine intense sweeteners in foodstuffs by high performance liquid chromatography and evaporative light scattering detection development and single laboratory validation[J]. Journal of Chromatography A,2007,1 157(1-2):187.
引用本文: 程庆兵,汪海宣,郑正,等 . 超高效液相色谱-串联质谱法测定丹桂香颗粒中痕量马兜铃酸I[J]. 化学分析计量,2024,33(11):52. (CHENG Qingbing, WANG Haixuan, ZHENG Zheng, et al. Determination of trace aristolochic acid I in Danguixiang Granules by ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Chemical Analysis and Meterage, 2024, 33(11): 52.)

来源:化学分析计量


