您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-17 07:14
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
百利药业全球领先的又一四抗药物启动临床。百利药业在clinicaltrials.gov网站上登记了四特异性抗体GNC-039的一项Ⅰ期临床,用于治疗复发难治转移性神经胶质瘤/实体瘤。GNC-039靶向PD-L1/4-1BB/CD3/EGFRvIII,是该公司进入临床的第二款四抗。去年9月,该公司第一款四抗(PD-L1/4-1BB/CD3/CD19)GNC-038已在中国获得一项临床默示许可,适应症为复发或难治性非霍奇金淋巴瘤、复发或难治性急性淋巴细胞白血病和难治性/转移性实体瘤。据悉,GNC-038是全球首个获批临床的四特异性抗体。
国内药讯
1.智飞新冠疫苗在中国获紧急使用授权。中科院微生所与智飞龙科马生物联合开发的重组新冠疫苗(CHO细胞)获国家药监局紧急使用授权。这款疫苗去年11月起陆续在中国及乌兹别克斯坦、巴基斯坦、厄瓜多尔、印度尼西亚多国启动了Ⅲ期临床,计划接种人数29000例。目前III期临床进展顺利。该疫苗是国内第四款获批紧急使用的新冠疫苗,也是国际上首个获批临床使用的新冠病毒重组亚单位蛋白疫苗。
2.东阳光「恩他卡朋片」即将获批上市。东阳光恩他卡朋片4类仿制上市申请进入“在审批”阶段,有望近期获批上市。恩他卡朋是一种COMT抑制剂,由Orion Pharma 原研,作为标准药物左旋多巴/苄丝肼或左旋多巴/卡比多巴的辅助用药,用于治疗以上药物不能控制的帕金森病及剂末现象(症状波动)。恩他卡朋片原研药于2003年获批进口中国,商品名为珂丹。目前该品种国内仅原研上市。
3.上海凯茂「注射用人干扰素γ」拟纳入优先审评。凯茂生物按生物制品2.2类、3.2类申报的注射用人干扰素γ上市申请获CDE纳入拟优先审评公示名单,拟用于治疗类风湿性关节炎;肝纤维化;慢性肉芽肿病;孟德尔遗传分枝杆菌易感性疾病。注射用人干扰素γ成份为重组人干扰素γ,系由含有高效表达人干扰素γ基因的大肠杆菌,经发酵、分离和高度纯化后冻干制成;目前该品种国内仅凯茂生物获批上市。
4.第二批国家鼓励仿制药品目录发布。国家卫健委公布了 6 部门联合印发的《关于印发第二批鼓励仿制药品目录的通知》,17 个原研药进入第二批鼓励仿制药品目录。这 17 个原研药包括葛兰素史克的万瑞舒(糠酸氟替卡松维兰特罗吸入粉雾剂)、全再乐(氟替美维吸入粉雾剂),安斯泰来的贝坦利(米拉贝隆缓释片),杨森制药的他喷他多,赛诺菲的卡巴他赛,辉瑞的去甲文拉法辛等。
5.石药2020年业绩:净利润增长38.9%。石药集团发布2020年财报,全年营收249.42亿元(+12.8%),股东应占溢利51.60 亿元(+38.9%);成药业务销售收入204.05亿元,较去年增加13.8%,其中恩必普销售额约65.74亿元,增长17.4%;各领域产品中,增速最高的是心血管疾病领域,共获得销售收入23.59亿元,同比增加61.9%;研发费用方面,2020年研发投入28.9亿元,占到营收的11.59%。
国际药讯
1.Moderna第二代新冠疫苗首例志愿者给药。Moderna公司宣布其第二代候选新冠疫苗mRNA-1283已完成Ⅰ期临床首位志愿者给药。该疫苗编码新冠病毒刺突蛋白的受体结合域和N端结构域(NTD),这一设计旨在解决疫苗在冷藏温度下的稳定性,促进疫苗的分发和使用。Ⅰ期临床将评估3个剂量(10 µg,30 µg,100 µg)的mRNA-1283在健康人中接种两剂后的安全性和免疫原性。上周,该公司针对最初在南非发现的病毒株B.1.351的增强疫苗mRNA-1273.351也完成了Ⅱ期临床首位志愿者给药。
2.宫颈癌创新疗法提前终止Ⅲ期临床。赛诺菲和再生元(Regeneron)联合开发的PD-1抑制剂Libtayo(cemiplimab),在单药治疗经治复发/转移性宫颈癌的Ⅲ期临床中获积极结果。与化疗相比,Libtayo显著改善患者的总生存期,两组中位生存期分别为12个月和8.5个月(HR=0.69,p<0.001);在鳞状细胞癌亚组中,Libtayo将死亡风险减少27%,而在腺癌亚组中,Libtayo将患者死亡风险减少44%。独立数据监察委员会(IDMC)建议提前终止临床试验。两家公司预计2021年递交其监管申请。
3.改良型创新制剂BXCL501获FDA突破性疗法认定。BioXcel Therapeutics口服溶解性右美托咪定舌下薄膜制剂BXCL501获FDA突破性疗法认定,这是一种选择性α2a受体激动剂,拟用于老年痴呆症患者激越症状的急性治疗。在一项Ⅰb/Ⅱ期TRANQUILITY试验中,两种剂量(30mg和60mg)BXCL501在用药2小时后,能显著减少患者激越行为发生;试验中观察到的剂量依赖性反应。去年7月,BXCL501用于精神分裂症和双相情感障碍的2项关键III期研究也获得积极结果。
4.蓝鸟生物慢病毒基因疗法调查结果出炉。在经过了近一个月的调查后,蓝鸟生物日前宣布其基因疗法LentiGlobin “极不可能”导致接受治疗的镰状细胞病患者出现急性髓细胞白血病;对于接受LentiGlobin治疗后出现骨髓增生异常综合征(MDS)的患者,蓝鸟生物还在调查当中。另外,受上述原因影响,该公司还暂停了使用同样慢病毒载体BB305已在欧洲上市的地中海贫血细胞疗法Zynteglo的销售。目前Zynteglo仍处于暂停销售状态。欧洲药品管理局将于本周开始审查Zynteglo的收益风险情况。
5.吉利德联手默沙东开发长效HIV组合疗法。吉利德衣壳抑制剂lenacapavir将联合默沙东创新核苷逆转录酶易位抑制剂(NRTTI)islatravir,在HIV患者中开展联合用药研究,评估为HIV患者提供完整的口服或注射型长效治疗方案的潜力。这两款创新疗法均为潜在“first-in-class”药物,并且都处于后期临床开发阶段。预计在今年下半年将启动临床试验,首先检验口服组合疗法的效力和安全性。
6.欧洲药监局将就阿斯利康新冠疫苗召开会议。欧洲药监局宣布,其安全委员会将于16日就阿斯利康新冠疫苗问题相关信息展开研讨,并在18日举行特别会议,以决定如何采取下一步的行动。近期,该疫苗由于存在严重不良反应可能性,在全球十多个国家被暂停接种。其严重不良反应包括凝血、血栓和血小板严重减少。目前调查还在进行当中。
7.靶向药物开发公司insitro完成C轮融资。致力于通过利用机器学习驱动药物发现和开发的insitro公司完成4亿美元的C轮融资。该公司曾于2019年与吉利德达成合作,通过机器学习发现治疗非酒精性脂肪性肝炎(NASH)的新靶点;与百时美施贵宝达成合作,为其发现治疗神经退行性疾病的靶点。本轮融资将用于提升该公司平台的技术能力,扩展数据库,以及收购通过该公司的独特策略去风险化(de-risked)的潜在候选药物。
医药热点
1.上海加快培养“医学+X”人才。上海市日前印发《关于本市加快医学教育创新发展的实施意见》,明确适度扩大研究生尤其是博士生招生规模,加快推进“医学+X”高层次复合型人才培养。以培养医学科学家、医学工程师等高端医学人才为目标,促进医工、医理、医文学科专业的深度融合,推进基础与临床融通的整合式八年制临床医学教育改革。到2030年,建成具有中国特色、上海特点的更高水平医学人才培养体系。
2.辐照技术有望“杀”灭新冠病毒。中核集团旗下中国同辐与中科院微生物研究所日前确定并开始执行实验方案:利用小型辐照装置开展新冠病毒灭活。研究成果将应用于进口冷链食品新冠病毒的消杀处理等。病毒辐照灭活主要是将钴-60和电子加速器等作为辐照源,利用γ射线、电子束及X射线产生的电离作用,直接或间接作用于病毒,使病毒的蛋白质和核酸等生物大分子发生断裂或变性等,从而失去感染性。中国同辐负责设计和提供专用辐照设备。
3.全国首家“子宫内膜异位症诊疗一体化管理示范中心”成立。无锡市妇幼保健院日前正式启动了子宫内膜异位症诊疗一体化管理示范中心。该院成立子宫内膜异位症诊疗一体化管理示范中心,通过中心固定场所、固定人员、固定时间,服务诊疗流程得到进一步优化,更有利于建立集“临床诊疗、随访管理、科普教育”于一体的内异症诊疗随访路径和立体化管理模式。
审评动向
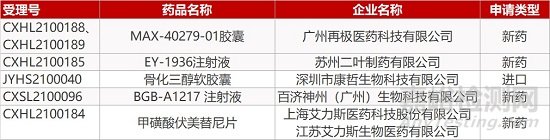
1. CDE新药受理情况(03月1日)
申请临床:
广州再极的MAX-40279-01胶囊(2个规格)、苏州二叶的EY-1936注射液、百济神州的BGB-A1217 注射液、艾力斯医药的甲磺酸伏美替尼片。
申请生产:
深圳康哲的骨化三醇软胶囊。
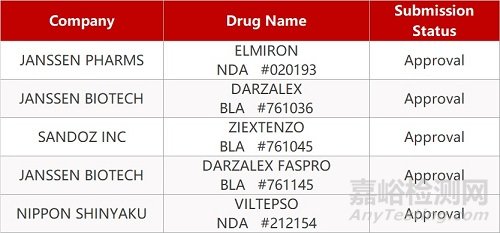
2. FDA新药获批情况(北美03月15日)
股市资讯
【恒瑞医药】公司及子公司成都盛迪医药有限公司的氟唑帕利胶囊及醋酸阿比特龙片(Ⅰ)获得药物临床试验批准通知书。
【柳药股份】公司回购注销限制性股票涉及8人,合计拟回购注销限制性股票22.232万股。
【步长制药】(1)公司拟与天津弗盈恒先健康科技合伙企业(有限合伙)共同设立控股子公司涛医云健康科技(杭州)数字医疗有限公司,拟由控股子公司步长健康科技有限公司的全资子公司天津步长医疗科技有限公司出资设立全资子公司江西省步长移动医疗设备有限公司、尚志市步长移动医疗设备有限公司;(2)全资子公司陕西步长高新制药有限公司拟对经营范围进行变更,增加经营范围:租赁。

来源:药研发


