您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-06-24 11:04
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.翰森治疗乙肝新药获批上市。翰森制药自主研发的1类新药恒沐®(富马酸艾米替诺福韦片)获国家药监局批准上市,用于治疗慢性乙型肝炎成人患者。恒沐®是翰森制药自主研发的第5个1类创新药,也是中国首个原研口服抗乙型肝炎病毒(HBV)药物。临床研究结果显示,与富马酸替诺福韦酯(Viread, TDF)相比,富马酸艾米替诺福韦只需要约十分之一的剂量即可获得相似的抗病毒疗效。
2.和黄医药赛沃替尼获批上市。和黄医药c-Met抑制剂赛沃替尼获国家药监局批准上市,用于治疗MET14跳变的局部晚期或转移性的非小细胞肺癌。这是和黄医药获批上市的第3款新药,也是中国首款获批的Met抑制剂。在一项II期研究中,中位随访17.6个月时,在可评估患者中ORR达到49.2%,疾病控制率(DCR)为93.4%,产生应答的中位时间为1.4个月,中位缓解持续时间(DoR)为8.3个月。
3.罗氏PD-L1抗体联合化疗治疗肺癌国内获批。NMPA批准罗氏PD-L1抗体阿替利珠单抗(Tecentriq,泰圣奇)联合培美曲塞和铂类化疗用于一线治疗EGFR/ALK阴性的转移性非鳞状非小细胞肺癌(NSCLC)。值得一提的是,Tecentriq刚于4月在华获批单药一线治疗PD-L1阳性、EGFR/ALK阴性的转移性NSCLC患者。在一项国际临床IMpower132中,Tecentriq联合化疗与化疗相比改善了无进展生存期(PFS)(中位PFS:7.6vs5.2个月;HR=0.60,95%CI [0.49, 0.72]);而且中国队列的PFS获益与全球人群保持一致。
4. 康泰新冠疫苗在马来西亚启动III期临床。深圳康泰生物自主研发的新冠灭活疫苗(Vero细胞)在马来西亚开展的III期临床完成首批入组受试者接种。今年2月,康泰生物已与马来西亚永大集团就该疫苗在马来西亚当地进行Ⅲ期临床和商业化达成合作。在国内,这款疫苗已于5月获国家药监局授予紧急使用授权,用于预防由新冠病毒感染引起的流行性疾病。
5.信迪利单抗联合化疗治疗食管鳞癌III期临床积极。信达生物与礼来联合开发的PD-1抑制剂信迪利单抗联合化疗(顺铂+紫杉醇/顺铂+5-氟尿嘧啶)一线治疗晚期或转移性食管鳞癌的国际III期临床(ORIENT-15)达主要终点。不论PD-L1表达如何,这一组合对比安慰剂组显著延长患者的总生存期(OS),达到优效性标准,安全性特征与已知研究一致,无新的安全性信号。详细结果将在学术会议上公布。
国际药讯
1.阿斯利康/默沙东Koselugo获欧盟批准上市。欧盟有条件批准阿斯利康和默沙东联合开发的MEK1/2抑制剂Koselugo (selumetinib)上市,用于治疗3岁及以上患有1型神经纤维瘤(NF1)的儿童患者的症状性、不可手术性丛状神经纤维瘤(PN)。在一项II期临床SPRINT Stratum 1中,Koselugo在这类患者中的客观反应率(ORR)达到66%;Koselugo不仅缩小了一些儿童的肿瘤,还减轻了疼痛,改善了他们的生活质量。
2.欧盟批准首个IL-13抗体疗法上市。欧盟委员会(EC)批准LEO Pharma公司抗体新药Adtralza(tralokinumab)上市,用于治疗适用于接受全身治疗的中重度特应性皮炎患者。Adtralza也是首个获批的IL-13单抗。在两项Ⅲ期临床(ECZTRA 1和ECZTRA 2)中,与安慰剂相比,Adtralza治疗组患者达到EASI 75或IGA评分达到0或1的患者比例显著增加;并且在长达52周的治疗期间显示出良好的耐受性和安全性。
3.GSK/Vir中和抗体治疗新冠临床积极。葛兰素史克(GSK)与Vir公司联合开发的中和抗体sotrovimab(VIR-7831,GSK4182136),在住院高风险成人中作为早期COVID-19单药治疗的Ⅲ期COMET-ICE研究结果积极。与安慰剂相比,sotrovimab静脉输注治疗使这类患者的住院或死亡风险显著降低79%(调整后的相对风险降低;p<0.001)。sotrovimab此前已获FDA授予紧急使用授权。目前,两家公司启动了评估肌内(IM)注射sotrovimab用于COVID-19早期患者的Ⅲ期研究。
4.Keytruda组合一线治疗宫颈癌Ⅲ期临床积极。默沙东PD-1抑制剂Keytruda,与含铂化疗联用(加或不加贝伐珠单抗),在一线治疗复发性或转移性宫颈癌患者的关键Ⅲ期临床中达到主要终点指标。中期分析显示,无论PD-L1状态如何,相比同类含铂化疗(加或不加贝伐珠单抗),这种组合疗法显著提高患者的总生存期(OS)和无进展生存期(PFS)。详细结果将于医学会议上公布。
5.创新ADC关键性临床试验中期结果积极。ADC Therapeutics靶向CD25的新型抗体偶联药物(ADC)camidanlumab tesirine(Cami,ADCT-301)在治疗复发/难治性霍奇金淋巴瘤的关键性Ⅱ期临床中获积极中期分析结果。在既往接受过≥3种治疗的患者中,Cami达到66.3%的总缓解率与27.7%的完全缓解率;临床中无新的安全性信号出现;中位缓解时间在中期分析时尚未达到。
6.mRNA疫苗预防季节性流感Ⅰ期临床启动。赛诺菲巴斯德与Translate Bio公司联合开发的下一代mRNA季节性流感疫苗启动Ⅰ期临床。该试验将评估两款单价候选疫苗(MRT5400和MRT5401)的安全性和免疫原性,这两款疫苗使用不同脂质纳米颗粒(LNP)成分,编码了甲型H3N2(A/H3N2)流感病毒株的血凝素蛋白。试验的中期数据预计将在今年年底公布。
7.Horizon购入治疗痛风RNAi品种。Arrowhead Pharmaceuticals宣布与Horizon Therapeutics就其在研RNA干扰(RNAi)疗法ARO-XDH达成全球合作和许可协议。ARO-XDH是一款靶向黄嘌呤脱氢酶的siRNA,拟用于治疗对当前疗法没有应答,症状失控的痛风患者。根据协议,Arrowhead将获得4000万美元的预付款,6.6亿美元的潜在开发、监管和商业里程碑付款;Arrowhead将负责siRNA疗法临床前研究。Horizon将获得该疗法的全球独家许可,并将全权负责其临床开发和商业化。
医药热点
1.河南下达1.1亿元发展中医药。河南省财政下达2021年中医药事业传承与发展补助资金1.1亿元,主要用于支持469名中医药专业人才培养培训、8个全国基层名老中医药专家传承工作室建设、443个基层中医馆建设、2家国家中医临床研究基地能力提升、国家中医疫病防治队和国家中医紧急医学救援队建设、道地药材生态种植示范基地建设、中医药文化传播行动、中医药古籍保护与传统知识收集等项目。
2.默克尔第二针接种莫德纳疫苗。22日,德国政府发言人表示,德国总理默克尔在首剂接种阿斯利康新冠疫苗后,第二剂接种了莫德纳疫苗。德国当局目前推行"混合接种"计划,决定为那些接种过第一剂阿斯利康疫苗的人接种第二剂mRNA疫苗,即辉瑞/BioNtech或Moderna的疫苗。有专家认为,第二针疫苗改用不同公司的产品,可以增强免疫力,目前已有多个相关研究正在进行。
3.世卫拟在南非建新冠疫苗技术转让中心。世卫组织总干事谭德塞21日透露,拟在南非建立新冠疫苗生产技术转让中心,以帮助非洲国家生产疫苗。目前,两家南非制药企业南非生物疫苗公司和埃弗里根生物制剂与疫苗公司加入这一项目。世卫组织正在与美国辉瑞公司和莫德纳公司商谈,希望他们能加入项目,分享他们的mRNA疫苗技术。
审评动向
1. CDE新药受理情况(06月22日)
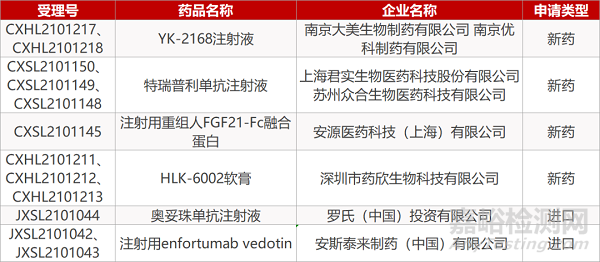


来源:药研发


