您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-07-16 10:36
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
圣诺双靶点RNAi新药上Ⅱ期临床。圣诺制药候选药物STP705在用于预防瘢痕疙瘩(Keloid scar)的Ⅱ期临床中完成首例患者给药。STP705是一种siRNA治疗药物,利用双靶向抑制特性和多肽纳米颗粒(PNP)增强递送直接敲低TGF-β1和COX-2的表达,降低组织的异常纤维化。该新药已获得FDA和NMPA的多个IND批准,包括治疗胆管癌、非黑色素瘤皮肤癌和增生性瘢痕。FDA已授予STP705用于治疗胆管癌的孤儿药资格。
国内药讯
1.荣昌「维迪西妥单抗」新适应症报上市。荣昌生物HER2-ADC新药“注射用维迪西妥单抗”的新适应症上市申请获CDE受理,推测这一适应症为单药治疗HER2过表达局部晚期或转移性尿路上皮癌(UC)。维迪西妥单抗(RC48)是首款由中国公司自主研发并获批上市的抗体偶联药物(ADC),国家药监局已于今年6月附条件批准该新药上市,用于治疗HER2过表达、既往接受过2种系统化疗的局部晚期或转移性胃癌。
2.复星新冠mRNA疫苗即将国内获批。复星医药董事长兼CEO吴以芳在股东大会上透露,国家药监局对mRNA新冠疫苗“复必泰”的审定工作已基本完成,目前已进入行政审批阶段。复星医药mRNA新冠疫苗来自与德国BioNtech合作获得大中华区权益,该疫苗已在香港和澳门批准上市。复星已与BioNTech公司提前启动生产准备工作,一旦疫苗国内获批,第一时间即可供应上市。据悉,复必泰很可能作为加强针免费接种。
3.中国医科院新冠疫苗上Ⅲ期临床。中国医科院生物所自主研发的新冠灭活疫苗科维福获巴西卫生监督局(ANVISA)批准,即将在巴西开展Ⅲ期临床试验,评估间隔14天接种两剂科维福疫苗用于18岁及以上成年人预防新冠病毒感染的的有效性和安全性。这是一项国际临床,全球共计约3.4万人参与该项试验,其中巴西参与试验的志愿者人数将为7992人。
4.欧康维视OT-101滴眼液上Ⅲ期临床。欧康维视核心产品OT-101(0.01%硫酸阿托品滴眼液)获国家药监局临床试验默示许可,即将开展用于治疗儿童受试者近视进展的Ⅲ期临床。这是一项国际临床,将在美国、欧洲和中国等多中心评估OT-101用于延缓或减慢儿童和青少年近视进度的安全性和有效性。目前,OT-101的Ⅲ期临床已在美国完成首例受试者入组,在英国及欧盟递交的Ⅲ期临床申请也获得监管机构的受理。
5.贝达药业CTLA-4单抗获批临床。贝达药业与Agenus联合开发的1类新药「泽弗利单抗」注射液获国家药监局临床试验默示许可(受理号:JXSL2101015)。泽弗利单抗是一款CTLA-4靶向抗体新药,是该公司从Agenus引进的两款新药之一。目前,这两款引进新药(PD-1抗体巴替利单抗和泽弗利单抗)联用治疗晚期实体瘤,以及联合治疗晚期宫颈癌的两项临床试验申请已获CDE受理,根据受理号,此次获批的临床为联合PD-1 治疗晚期实体瘤。
6.开拓PROTAC品种在美获批临床。开拓药业基于蛋白降解嵌合体(PROTAC)技术开发的AR靶向新药GT20029获FDA临床批准,即将开展用于治疗雄激素性脱发和痤疮的研究。该项研究是一项随机、双盲、安慰剂对照、平行分组、剂量递增研究,评估局部单次和多次剂量递增用药后GT20029的安全性、耐受性和药代动力学。据悉,GT20029是全球首款进入临床阶段的外用PROTAC化合物, 今年4月已在国内获批开展I期临床试验。
7.亚盛医药与信达生物达成战略合作。信达生物旗下信达苏州,与亚盛医药及其子公司顺健生物签订一份合作及授权协议,在中国大陆、香港、澳门及台湾地区联合开发及商业化第三代BCR-ABL抑制剂HQP1351。亚盛实体将获得3000万美元的首付款、股权投资和不超过1.15亿美元的里程碑付款。同时,双方同意就Bcl-2抑制剂APG-2575与抗CD20单抗达伯华(利妥昔单抗注射液)、抗CD47单抗letaplimab(IBI188)就某些适应症探索展开临床合作和联合开发。
国际药讯
1.改良维生素A获FDA突破性疗法认定。Alkeus Pharmaceuticals公司维生素A衍生药物ALK-001获FDA授予突破性疗法认定,用于治疗眼底黄色斑点症(又名Stargardt病,STGD1)。在一项Ⅱ期临床中,ALK-001达到研究的主要终点,显示出ALK-001在人体中具有统计学意义的显著疗效,具体数据将在今年晚些时候公布。FDA之前已授予ALK-001治疗该病的孤儿药资格。
2.活体生物治疗产品即将启动临床。希望之城(City of Hope)国家医学中心宣布已与Osel公司达成一项全球独家许可协议。根据协议,Osel公司将从希望之城获得活体生物治疗产品(LBP)CBM588用于癌症治疗的全球独家许可。CBM588是一种酪酸梭菌(Clostridium butyricum)菌株,已在Ⅰb期临床中显示出治疗转移性肾细胞癌患者的潜力。希望之城计划7月启动一项在晚期转移性肾细胞癌患者中评估CBM588与nivolumab/cabozantinib联合治疗的临床试验。
3.礼来收购胰岛素公司Protomer。礼来宣布将斥资高达10亿美元收购生物技术公司Protomer Technologies,并获得Protomer实验性葡萄糖反应性胰岛素的药物资产。Protomer成立于2015年,总部位于美国加利福尼亚州,其开发的药物可对葡萄糖等“分子激活剂”产生反应,从而改善糖尿病患者葡萄糖水平过高的问题。两家公司没有透露预付款和里程碑付款的具体细节。
4.FDA拟对“女性伟哥”Addyi采取监管措施。FDA日前在一份关于已获批产品的潜在新安全问题的报告中指出,Sprout公司的“女性伟哥”Addyi(flibanserin,氟立班丝氨)可能存在药物过敏的风险,FDA正在评估针对Addyi采取监管行动的必要性。Addyi是一款粉红色的小药丸,已于2015年获FDA批准上市,用于治疗绝经前女性非疾病原因的性功能障碍——机能减退性欲障碍(HSDD)。
5.基因编辑公司Prime Medicine融资逾3亿美元。基因编辑领域先驱刘如谦博士联合创建的Prime Medicine公司完成数额为3.15亿美元的融资,拟用于推进其独有的先导编辑(prime editing)技术为患者带来终身性的治愈疗法。该公司的先导编辑技术将Cas9蛋白与逆转录酶(reverse transcriptase)融合形成一种特殊蛋白,这种Cas9-逆转录酶融合蛋白会在其pegRNA模板的引导下,精准地切开一条DNA链,并合成含有正确序列的DNA。该技术可以将任何碱基转化为任何其它碱基(包含所有的12种可能性),还能够插入或删除特定的DNA序列。
6.Ribon公司完成B1轮融资。Ribon公司宣布完成一项6500万美元的B1轮融资,将用于推进其主打候选药物RBN-2397和RBN-3143的临床开发。RBN-2397是一款PARP7抑制剂,能够通过抑制肿瘤细胞中的PARP7,直接抑制细胞增殖并恢复I型干扰素信号,以刺激先天性或适应性抗肿瘤免疫应答,该药拟用于治疗实体瘤,目前处于Ⅰ期临床阶段。RBN-3143是一款PARP14抑制剂,用于治疗炎症,目前处于临床前开发阶段。
医药热点
1.2021全国医院门诊量100榜单出炉。看医界传媒统计编制的《2021中国医院门诊量100排行榜》日前发布。根据榜单,医院门诊量TOP10分别为郑大一附院(776万人次)、广东省中医院(772万人次)、华中科大同济医学院附属协和医院(670万人次)、华中科大同济医学院附属同济医院(632.81万人次)、青岛大学附属医院(600万人次)、江苏省中医院(585万人次)、吉林大学白求恩第一医院(554万人次)、武汉大学人民医院(539.6万人次)、江苏省人民医院(525万人次)、佛山市中医院(522.44万人次)。
2.福布斯中国最佳CEO榜单发布。福布斯中国发布最佳CEO榜单,共计50位CEO上榜。其中医药健康领域上榜10人,分别是复星医药-吴以芳、欧普康视-陶悦群、新和成-胡柏剡、健帆生物-董凡、智飞生物-蒋仁生、长春高新-安吉祥、康泰生物-杜伟民、华兰生物-安康、药明康德-李革、凯莱英-洪浩。医药健康领域占比最高,达到20%。
3.我国人均基本公卫补助增至79元。7月12日,国家卫健委、财政部、国家中医药管理局联合印发《关于做好2021年基本公共卫生服务项目工作的通知》,明确2021年人均基本公共卫生服务经费补助标准为79元。2020年增加的5元全部落实到乡村和城市社区,统筹用于常态化疫情防控;2021年新增5元统筹用于基本公共卫生服务和基层医疗卫生机构疫情防控工作。
审评动向
凯信远达的注射用塞替派。
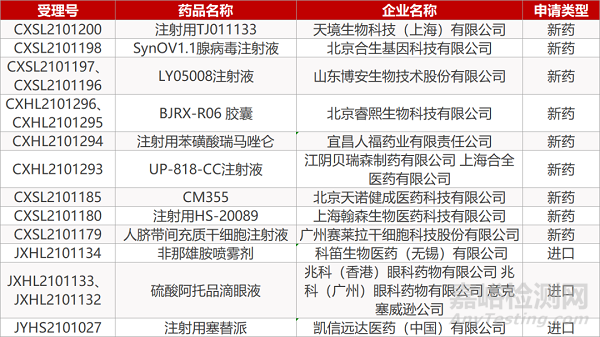
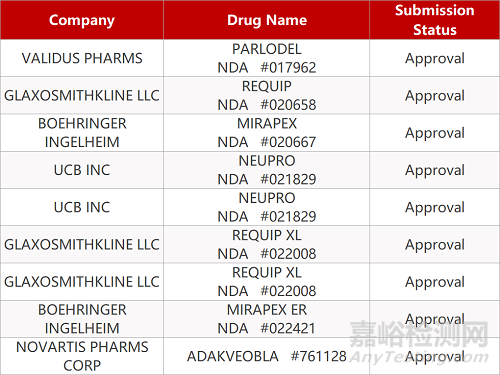

来源:未知


