您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-03-19 18:20
摘要
本文论述了一个仿制药研发项目前期分析调研需要关注哪些内容,以及如何写出一份对研发分析工作有指导意义的调研报告。
前言
《礼记·中庸》告诉我们:“凡事预则立,不预则废。”在做一件事情之前,做好前期准备工作的意义无论如何强调都不为过,调研也是其中之一。仿制药的研发如果前期有了充分的调研,很多工作如何开展就有了清晰的思路,可以省略很多探索的过程。本人根据自己的工作经历阐述对于研发分析调研的理解,个人浅见,作抛砖引玉之用。
鉴于篇幅有限,具体内容检索方法本文不作论述,只是说明应当调研哪些内容,具体检索方法读者可以查阅公众号相关文献资料或者通过其他途径学习。
仿制药研发分析调研内容
仿制药研发分析需要调研的内容个人认为应当至少包含以下内容:参比制剂信息、欧美日审评报告、各国药典标准、对照品、色谱柱和其他相关文献资料。详细内容请见下文的模板。
分析调研报告模板
封面、目录、页眉、页脚等内容读者请按照各自公司的要求撰写。
1. 参比制剂
1.1 原研制剂
说明原研制剂的相应信息,如生产企业、上市情况等,这些信息可以通过在网上查找相关新闻、查询欧美日药政部门官网或者原研企业网站等渠道获得。示例如下:
厄洛替尼是一种分子靶向治疗药物,用于晚期非小细胞肺癌的治疗。该药分别于2004年11月和2005年9月在美国和欧洲通过审批,并于2007年3月由罗氏制药在我国正式上市,商品名为特罗凯。
1.2 参比制剂备案信息
可以在药智数据库查询仿制药的参比制剂备案信息,这些信息可以作为参考。
2. 欧美日审评报告
2.1 审评报告检索
在FDA、EMA、PMDA官网上分别查询chemical reviews、scientific discussion与IF文件,这三份文件有许多与分析有关的内容。将查询到的文件以嵌入文件的形式复制到报告中,示例如下:

2.2 审评报告总结
将上述查询到的审评报告中对于将来工作有意义的内容摘录入报告。
3 药典收载情况
查询该品种在欧美日中四方最新版药典中的收载情况,将查询到的文件以嵌入文件的形式复制到报告中,示例如下:

3.1 原料药标准比对
将查询到的各方药典标准进行对比,可分别对比限度、有关物质检测方法、含量测定检测方法等内容。
限度对比
列出查询到的药典标准的检测项目与限度要求,并初步评估内控标准的检测项与限度。示例如下:

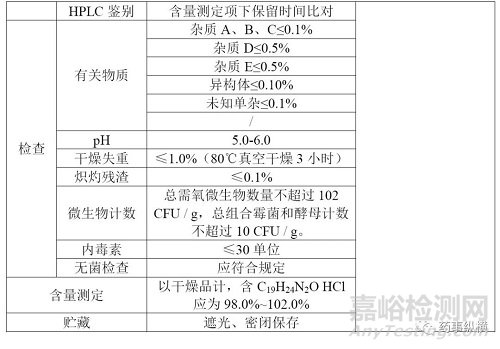
有关物质方法比对
将各方药典标准的有关物质检测方法进行对比,并初步确定主要选择哪一个方法进行研究。
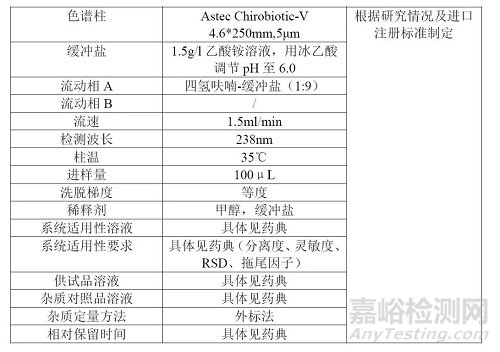
含量测定方法对比
具体操作参考有关物质方法对比。
其他
其他检测方法的对比也可以参考有关物质方法对比。
3.2 制剂质量标准比对
参考原料药标准比对
4.文献查询
根据前期初步评估,将查询到的其他相关文献信息录入报告中。比如头孢类抗生素项目的聚合物检测方法,API为甲磺酸盐相应的遗传毒性物资甲磺酸酯检测方法或者相关专利文献等。
5.对照品
在各国官方对照品或其他来源对照品信息列出,便于将来开展采购。示例如下:
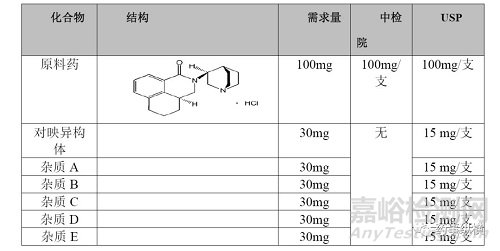
6.色谱柱
将查询到的各国药典用到的色谱柱(主要是USP与EP)与预期会用到的色谱柱列出,便于将来开展采购。示例如下:
含量测定:Agilent ZORBAX SB C8, 4.6*250mm,5μm
有关物质:Astec Chirobiotic-V 4.6*250mm,5μm
7.风险评估
根据相应的经验与上述查询到的信息综合评估项目可能遇到的风险因素,包括技术、管理、设备等各个方面,列出对项目推进可能产生影响的环节,并提出应对措施。示例如下:
本项目为头孢类抗生素,聚合物是药物过敏的主要因素,因此对产品中的聚合物进行研究。各国药典均未收载相应检测方法,需要开发检测方法。聚合物检测一般采用分子排阻色谱法,色谱柱一般为凝胶柱,价格较贵且寿命较短,需要制定相关预算。
本项目可能需要研究甲磺酸甲酯、甲磺酸乙酯、甲磺酸异丙酯,FID检测器的灵敏度可能不足,需要用到质谱检测器,目前实验室尚无该类设备,需尽快进行相应的评估确定是否需要采购。
后言
仿制药研发分析在开展工作之前,如果进行了上述的系统的调研工作,就能对项目有一个较为全面清晰的了解,能够准确找到工作的重点,并能根据这些调研信息制定一个系统的研究计划,避免因为仓促上马而导致顾此失彼。
本文只是个人之见,必定有不合理或疏忽之处,欢迎读者批评指正。

来源:Internet


