您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-11 11:33
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
爱科百发抗病毒新药Ⅲ期临床积极。爱科百发开发的RSV融合蛋白小分子抑制剂齐瑞索韦(爱司韦,ziresovir),在用于治疗呼吸道合胞病毒(RSV)感染儿童患者的关键性Ⅲ期临床AirFLO达到主要终点及关键次要终点。与安慰剂相比,ziresovir治疗48小时内症状评分显著改善了30%(p=0.002);用药组第五天的病毒载量较对照组降低了77%(p=0.006);ziresovir总体耐受性良好。该公司计划于2022年年中向NMPA提交新药上市申请。
国内药讯
1.君实PD-1单抗鼻咽癌Ⅲ期临床积极。君实生物在AACR2022年会上公布PD-1特瑞普利单抗联合化疗一线治疗鼻咽癌的Ⅲ期临床JUPITER-02更新结果。根据BIRC评估,与安慰剂联合化疗组相比,这一组合将患者的中位无进展生存期(PFS)延长13.2个月(21.4个月vs8.2个月),将患者疾病进展或死亡风险降低48%;两组的客观缓解率(ORR)分别为78.8%和67.1%,缓解持续时间(DoR)中位数分别为18.0个月和6.0个月;临床中未出现新的安全信号。
2.强生CD3/22双抗在华获批临床。强生1类生物制品JNJ-75348780注射液(JNJ-8780)获国家药监局临床试验默示许可,拟用于治疗B细胞非霍奇金淋巴瘤和慢性淋巴细胞白血病。JNJ-75348780是全球首个且唯一一个进入临床开发阶段的CD3/CD22双特异性抗体,目前正在海外开展首次人体剂量递增的I期临床研究。该研究旨在确定JNJ-75348780的安全性、Ⅱ期临床的推荐剂量(RP2D)以及最佳给药方案。
3.华东医药FIC三靶点降糖药获批临床。华东医药旗下道尔生物开发的代谢领域创新药注射用DR10624获新西兰监管部门批准开展I期临床试验。DR10624是一款潜在“first-in-class”的靶向GLP-1R、GCGR和FGFR1c-Klothoβ(FGF21R)的长效三靶点激动剂,拟用于2型糖尿病、肥胖和代谢综合征的治疗。此次为道尔生物首个在海外获批的临床试验申请。DR10624也是同类药物中全球首款获批进入临床开发。
4.华海药业抗凝血新药获批临床。华海药业旗下上海华汇拓新型抗凝血药HHT120胶囊获国家药监局临床试验默示许可,拟口服用于预防骨科大手术术后的静脉血栓栓塞症(VTE)。HHT120是一款靶向凝血酶的抑制剂,可阻断血液凝固级联反应中纤维蛋白原的激活,从而阻断血栓的形成。在临床前研究中,HHT120可剂量依赖地抑制血栓生成、抑制血流下降及延长凝血指标;而且HHT120与同靶点的达比加群酯相比,在临床上的出血风险可能较小。
5.礼来Aβ单抗Donanemab在华报IND。礼来阿尔茨海默病(AD)候选药物Donanemab注射液的临床试验申请获CDE受理。Donanemab是一款靶向N3pG的修饰化β淀粉样蛋白斑块抗体药物,它通过与AD大脑中淀粉样蛋白沉积中的β淀粉样蛋白结合,从而促进患者大脑中淀粉样蛋白沉积的清除。去年6月,FDA已授予donanemab突破性疗法认定。目前,该新药已在美国滚动提交上市申请,以寻求FDA的加速批准。
国际药讯
1.IL-2受体靶向疗法关键性Ⅲ期临床积极。Citius Pharmaceuticals工程化IL-2白喉毒素融合蛋白I/ONTAK(E7777)治疗持续或复发皮肤T细胞淋巴瘤(CTCL)的关键Ⅲ期临床获积极顶线结果。总计71例患者接受治疗,69例患者纳入主要疗效分析。试验结果显示,I/ONTAK经IRC评估的客观缓解率(ORR )达到36.2%(95% CI,25.0%,48.7%);研究者评估的ORR为42.3%(95% CI,30.6%,54.6%)。Citius预计将在今年下半年向FDA递交生物制品许可申请。
2.杨森FcRn抗体II期临床积极。杨森在AAN2022年会上公布其FcRn抗体尼波卡利单抗(nipocalimab)治疗全身性重症肌无力(gMG)的II期临床积极结果。数据显示,nipocalimab可剂量依赖性地降低患者血清IgG(包括所有IgG亚类)和AChR IgG自身抗体水平,并且与重症肌无力日常活动评分(MG-ADL)的改善相关。研究表明,IgG降低的百分比可以作为gMG患者综合治疗的一个支持性生物标志物。
3.阿斯利康PD-1/CTLA-4双抗早期临床积极。阿斯利康在AACR2022年会上公布其PD-1/CTLA-4双抗MEDI5752用于治疗不适合标准治疗的晚期实体瘤的Ⅰ期临床研究结果。AACR摘要显示,MEDI5752在这类患者中表现出抗癌活性,客观缓解率达到19.8%,中位缓解持续时间为17.5个月。生物标志物分析显示MEDI5752强力阻断PD-1和CTLA-4信号传导,并显示出扩展已有或新T细胞克隆的潜力。
4.Blueprint第四代EGFR抑制剂早期临床积极。Blueprint公司第四代EGFR抑制剂BLU-945在治疗EGFR突变的非小细胞肺癌(NSCLC)的Ⅰ期临床中获得概念验证数据。BLU-945能够剂量依赖性降低循环肿瘤DNA;最高剂量BLU-945治疗的患者有1例获得部分缓解;而且BLU-945表现出良好的安全性。数据支持在EGFR突变的NSCLC患者中进行全面组合疗法的临床开发。再鼎医药拥有这款新药在大中华区的开发权益。
5.武田布局新一代基因疗法。武田与Evozyne公司将利用后者的蛋白工程化技术平台,针对多达4种罕见病靶点,合作开发基于创新蛋白的新一代基因候选疗法。根据协议,Evozyne将为推进基因疗法构建创新蛋白序列;Evozyne将获得上千万美元前期付款和研究经费,以及高达4亿美元的里程碑潜在付款。武田有权获得创新蛋白序列用于基因疗法项目,并拥有基因候选疗法的独家研发权益。
6.辉瑞扩展传染病研发管线。辉瑞拟斥资5.25亿美元收购ReViral公司,并获得ReViral开发的一系列呼吸道合胞病毒(RSV)在研疗法。sisunatovir是一款旨在阻断RSV病毒与宿主细胞融合的小分子口服药物,目前正在婴儿中进行Ⅱ期临床开发。此前,该新药已获得FDA授予的快速通道资格。在中国,联拓生物拥有sisunatovir的开发和商业化授权。
医药热点
1.上海疫情预测5月初基本平复。天津南开大学黄森忠团队发布《关于上海新发新冠疫情的研判简报(2022.4.6)》指出,自2022年2月24日新发的上海疫情4月4日后已转入“受控”状态,预测将于5月初基本平复,感染总规模在133294~166482例之间。3月14日,兰州大学黄建平院士团队也曾发布预测结果,该团队认为在当前政府采取的及时、有效的管控措施下,本轮疫情预计将于4月初得到控制,预计累计感染约3.50万人。
2.英官方新冠症状清单新增九种症状。英国卫生安全局(UKHSA)近期更新了新冠症状清单,将喉咙痛、肌肉疼痛和腹泻等9种症状列入其中。新版的新冠症状包括:呼吸急促;感觉疲劳、筋疲力尽;身体疼痛;头痛;喉咙痛;鼻塞或流鼻涕;味觉丧失;腹泻;感觉不舒服或生病。英国科学家蒂姆·斯佩克特教授此前曾强烈批评政府拒绝承认广泛的症状。他指出,不承认更广泛的感染症状清单,以及放弃隔离建议和取消免费检测的决定,可能会导致病毒的传播率升高。
3.京东健康2021年总收入306.8亿元。京东健康日期发布2021年全年业绩公告。截至去年12月底,京东健康的年度活跃用户数量达到1.23亿,同比增加3356万。报告期内,京东健康总收入为306.8亿元,同比增长58.3%,其中服务收入增长72.7%;非国际财务报告准则指标下(Non-IFRS)净利润达14.0亿元,同比增长91.5%;全国范围内的药品仓库和非药品仓库数量分别增至19个和超过400个,80%的自营药品订单实现次日达;京东健康互联网医院日均咨询量已超过19万。
评审动态
1. CDE新药受理情况(04月08日)
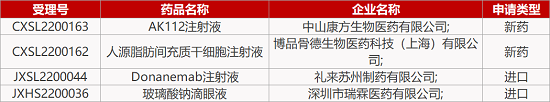
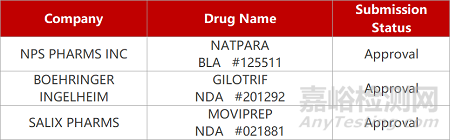

来源:药研发


