您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-06-28 11:19
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.拜耳硫酸拉罗替尼口服液在华获批。拜耳硫酸拉罗替尼口服溶液(larotrectinib)的上市申请获国家药监局批准。Larotrectinib是一款“不限癌种”疗法,是全球首款获批针对NTRK基因融合癌症患者设计的口服TRK抑制剂。今年4月,这款新药的胶囊剂型已获得国家药监局批准上市,此次获批的是larotrectinib的口服溶液剂型,用于治疗NTRK融合基因、局部晚期/转移性实体瘤患者。
2.泰它西普上SLE国际III期临床。荣昌生物宣布全球首款BLyS/APRIL双靶点融合蛋白泰它西普用于治疗系统性红斑狼疮(SLE)的国际Ⅲ期临床在美国完成首例受试者入组给药。该新药通过抑制BLyS和APRIL细胞因子与B细胞表面受体的结合,来阻止B细胞的异常分化和成熟,从而治疗自身免疫性疾病。除SLE外,该新药还在多项Ⅱ/Ⅲ期临床中用于治疗类风湿性关节炎、IgA 肾炎、干燥综合征和重症肌无力。
3.恩沃利单抗慢性乙肝IIb期临床积极。歌礼制药在ILC 20222022大会上口头报告皮下注射PD-L1抗体ASC22(恩沃利单抗)联合核苷酸类似物(NAs)治疗慢性乙型肝炎(慢乙肝)的IIb期临床(NCT04465890)中期结果。在1.0 mg/kg ASC22队列中,有42.9%的患者达到HBsAg持续清除;有21%的患者观察到ALT一过性反跳(安慰剂组患者无此现象),而且这类患者HBsAg下降更显著。临床中未收到药物相关的严重不良事件报告。试验数据显示ALT一过性反跳可作为预测或监测患者对治疗反应的指标。
4.信达改良型IGF-1R抗体获批临床。信达生物IGF-1R抗体改良药IBI311获国家药监局临床试验默示许可,拟用于甲状腺眼病的治疗。全球范围内目前仅有Horizon公司开发的IGF-1R抗体Tepezza获批上市,用于治疗甲状腺眼病,该产品2020年首年上市销售额8.2亿美元,2021年销售额16.6亿美元。Tepezza已上市的为静脉注射剂型,皮下注射剂型正在临床阶段。IBI311推测为皮下注射的Tepezza类似药。
5.礼来Aβ单抗在华获批临床。礼来Aβ单抗donanemab注射液获国家药监局临床试验默示许可,拟开发用于早期症状性阿尔茨海默病(AD),包括AD所致的轻度认知障碍以及轻度AD。Donanemab能够与AD患者大脑中淀粉样蛋白沉积中的β淀粉样蛋白结合,从而促进患者大脑中淀粉样蛋白沉积的清除。在Ⅱ期临床TRAILBLAZER-ALZ中,donanemab较安慰剂使患者iADRS评分降低幅度减少32%。目前,该新药已在美国滚动提交上市申请。
国际药讯
1.儿童软骨发育不全创新疗法获批上市。日本厚生劳动省批准BioMarin公司每日注射一次的C型利钠肽类似物Voxzogo(vosoritide)注射液上市,用于治疗所有年龄段儿童的软骨发育不全。在一项国际Ⅲ期临床中,相较于安慰剂组,vosoritide治疗组患儿平均每年多长1.57cm。而且在开放标签研究的随访时间达到两年的患者中,生长速率的改善得到维持。此前,该新药已获得FDA和EMA批准上市。
2.诺和诺德每周1次胰岛素III期结果积极。诺和诺德icodec胰岛素用于治疗糖尿病的国际IIIa期(ONWARDS 1、2、6)临床均达到主要研究终点。其中ONWARDS 2研究旨在评估每日胰岛素注射的2型糖尿病患者转换为每周注射一次的icodec胰岛素与德谷胰岛素治疗的效果,为期26周的结果显示,与整体基线HbA1c水平8.13%相比,icodec胰岛素实现了0.93%的HbA1c水平降低, 优于德谷胰岛素的0.71%;而且两组的低血糖发生率没有统计学差异。
3.赛诺菲/GSK双价新冠疫苗对奥密克戎有效。赛诺菲与葛兰素史克联合开发的佐剂双价D614/β(B.1.351)加强疫苗在2项临床试验(VAT02 Cohort 2,COVIBOOST VAT013)中获得阳性数据。在接受过mRNA疫苗初级免疫的成年人群中,该疫苗较辉瑞Comirnaty加强针具有更高的免疫应答;也显示出针对广泛新冠变体(包括Omicron BA.1和BA.2)的保护潜力。在既往血清反应阳性人群中,佐剂双价疫苗对Omicron确诊的有症状病例的总体疗效为75.1%(95%可信区间[CI,56.3,86.6]),在Omicron确诊的有症状病例中,总疗效为93.2%(95%可信区间[CI,73.2,99.2])。临床中该疫苗总体耐受性良好。
4.眼科基因疗法获欧盟PRIME认定。Adverum公司一次性基因疗法ADVM-022获欧洲药品管理局(EMA)授予优先药物(PRIME)资格,用于治疗湿性年龄相关性黄斑变性(AMD)。ADVM-022使用Adverum独有的AAV.7m8载体,旨在将携带表达编码aflibercept(阿柏西普,VEGFR-Fc融合蛋白)的转基因递送到眼内治疗湿性AMD。临床试验结果显示,ADVM-022用于一次玻璃体内注射便可提供3年aflibercept持续和一致的表达。
5.渤健终止AD新药一项临床研究。因受限的医保报销政策,渤健日前终止阿尔茨海默病(AD)新药Aduhelm的观察性临床ICARE AD研究,该试验旨在收集Aduhelm在美国使用的真实数据。Aduhelm用于加速批准的验证性III期ENVISION研究目前还在进行当中,预计初步完成日期为2025年底。此外,渤健首席执行官Michel Vounatsos也于近期宣布离职,该公司目前已停止Aduhelm的商业活动并裁减销售团队。
6.Alladapt拟加速“多合一”口服脱敏疗法开发。专注于研发免疫球蛋白(IgE)相关的食物过敏处方疗法的Alladapt公司日前完成了1.19亿美元融资,拟用于推进其主打在研产品ADP101的临床开发,以及生产设施的扩建和后续产品管线的扩大。ADP101是一款口服免疫治疗药物,涵盖引发食物过敏反应的食品类别包括奶,蛋,小麦,鱼类,贝壳类海产,花生,坚果,豆类和芝麻。该公司计划明年年初公布ADP101的Ⅰ/Ⅱ期试验结果,并在2024年启动Ⅲ期临床。
医药热点
1.法国发现首例儿童猴痘病例。当地时间25日晚,法兰西岛大区卫生机构宣布一名儿童感染猴痘病毒,这是法国发现的首例儿童猴痘病例。该病患是一名小学生,病情已得到控制且没有恶化的风险。在法国,迄今已确诊猴痘病例超过300例。世卫组织同日宣布,现阶段猴痘疫情不构成“国际关注的突发公共卫生事件”。
2.吉林:创建中医药“五大中心”。吉林省中医药管理局、卫健委联合印发《吉林省中医药“五大中心”创建实施方案》,计划到2025年年底,在全省各级各类医疗机构中创建一批中医特色突出、基础设施完备、设备技术配套、人才梯队合理、传承创新有力、服务优质精细的中医治未病诊疗中心、中医康复诊疗中心、中医老年病诊疗中心、中医传统诊疗中心、中西医结合诊疗中心。
3.第七批集采开标地点换到南京。6月27日,上海阳光采购网发布公告,企业参与国家第七批药品集采递交材料的地点由上海改为江苏南京,递交相关材料的开始和截至时间均不变。集采开标的具体地址为南京玄武区的紫金山庄会议中心。此前的六批七轮国采均在上海举行。据上海卫健委通报,6月26日上海新增本土新冠确诊病例2例、境外输入性确诊病例6例。
评审动态
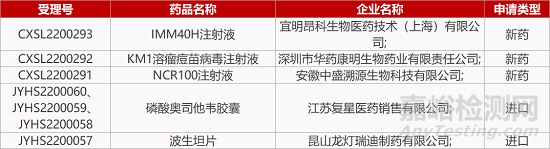
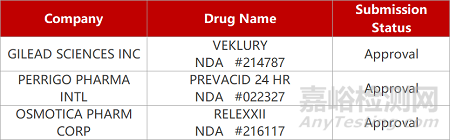

来源:药研发


