您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-05 05:58
本文将高压微射流法与其他纳米制备方法进行比较,概述了高压微射流装备的结构与工作原理及其在药物研究中的应用,重点介绍了在纳米混悬剂和纳米乳制备中的应用。纳米技术作为新兴技术之一,在现代药剂学中 越来越成为研究的热点。在医药领域中,药物颗粒的粒径大小和粒度分布是药物药理药效及使用性能的重要影响因素。与传统的药物制剂相比,纳米化 药物具有粒径小、比表面积大及宏观量子隧道效应等特性,可有效增大药物尤其是难溶性药物的饱和 溶解度和溶出速度、增强疗效及靶向性、提高生物利用度及吸收稳定性、减少药物用量及降低不良反应,在医药领域中具有广阔的应用前景。
1 纳米制剂制备方法及比较
目前纳米制剂制备方法主要分为两大类,即“自上而下( top down) ”和“自下而上( bottom up) ”。
“自上而下”是指通过机械手段将大的药物颗粒粉 碎成小的药物颗粒,常见的有球磨法、超声法、高压 均质法等。“自下而上”是指将药物溶解在一种溶剂中,用另一种含有稳定剂的反溶剂进行沉淀,常见 的有蒸发沉淀法、超临界萃取法等。
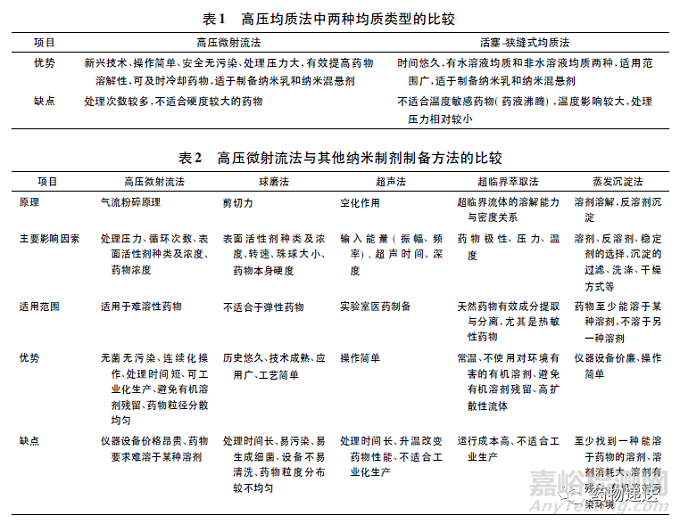
高压均质法有两种均质类型,一种是高压微射 流法,即将大颗粒药物分散于水溶液或其他溶剂(如乙醇)中,在高达4000bar 的压力下悬液先通过 “Z”形腔,通过改变几次液流方向碰撞产生剪切力,后通过通道直径为 75 μm 的“Y”形腔,两股液流高 速( > 1 000 m·s - 1 ) 相向碰撞,通过撞击力、剪切力 及气穴产生粒度均匀的纳米粒。另一种是活塞-狭 缝式均质法,即在 100 ~ 2 000 bar 的压力作用下,含 大颗粒药物的混悬液通过 5 ~ 20 μm 的狭缝,生成均 匀分散的纳米粒。高压微射流法是一种新型的 纳米制剂制备方法,具有能在不破坏药物活性成分情况下降低药物的粒径并使药物的粒度分布均匀等 优点,其处理后的悬浮粒子粒径可达纳米范围。为 了避免纳米药物团聚,需要加入甘露醇等促进纳米 颗粒的分散。将高压均质法的两种均质类型做 了相应比较比较如表 1 所示,将高压微射流法与其 他纳米制剂制备方法进行比较如表 2 所示。
2 高压微射流装备的结构及工作原理
2.1 高压微射流装备的结构
高压微射流装备主 要由进料罐、单向阀、液压泵、增压器、压力表、交互 容腔、辅助容腔、回流过滤器、热交换器和出料口构成。交互容腔和辅助容腔组成物料反应器,对物 料粉碎起关键作用。物料反应器的材质金刚石,其具有坚硬、不易磨损、耐腐蚀等特性,可用于高硬度药物。液压泵内的增压柱塞采用氧化锆陶瓷,具有 耐磨损、耐腐蚀且不易产生静电。高压微射流装备的处理压力可达到30000psi,故工艺流程很稳定,其工艺流程如图 1 所示。

2.2 高压微射流装备的工作原理
高压微射流装备( MicrofluidicsTM Inc.,U.S.A.) 采用的是气流粉碎原理,利用液压泵使流体产生高压,进而推动 装有活塞的增压器,液压驱动增压器内的活塞推动 高压往复活塞产生一个交替的抽吸,使流体加速,高速进入交互容腔内,在交互容腔内的微孔道(75μm)中,流体被分散成两股进行强烈的高速撞击、高速剪切,再进入辅助容腔(200μm) ,在撞击过程中瞬间转化其大部分能量,从而产生巨大的压力降,实现高速撞击、高剪切力、空穴作用、高频振动等综合作用,来达到粉碎的目的,使得液滴或者晶体粒径降低。
3 高压微射流装备的应用
作为新型纳米技术,高压微射流均质技术具有改性药物粒径大小的性能。一般来说,应用微射流仪处理药物颗粒,影响药物粒径大小和粒度分布的因素主要有3个,它们分别是处理压力、循环次数以 及药物本身性质有关。利用高压微射流装备只能制备得到纳米混悬液和纳米乳两种剂型,与其他方法连用可以制得纳米粒、多孔微球等剂型的纳米药物,制得的药物可用于口服、注射、外用、肺部吸收等。
3.1 纳米乳
纳米乳是非平衡体系,形成需要外加能量,通常来自机械设备或化学制剂的结构潜能,粒径通常20~200nm。表面活性剂的种类和用量是纳米乳稳定性的关键。微射流仪能在最短时间内提供所需能量并获得粒径最小的均匀乳液,故在国内外纳米乳剂领域研究中被广泛应用。
Siah等将超声法和高压微射流法比较制备阿司匹林纳米乳,处理压力为200bar,处理10次,载有阿司匹林纳米乳的黏度为3.98cP,平均粒径为(146.1 ± 1.528)nm,粒度分布均匀,适用于制剂领域。Zhao 等将高压微射流法和活塞-狭缝均质法 进行比较制备静脉注射脂肪乳,并研究了影响粒径 大小和粒径分布的因素。所研究的影响因素从主到次依次为处理压力/循环次数、温度、蒸汽灭菌、pH 值,而且制备静脉注射脂肪乳高压微射流法比活塞-狭缝均质法更有效。高压微射流法制备的脂肪乳具有粒径小,粒度分布窄等特点。Kotyl等采用两 种方法制备组分比例相同的 δ-维生素E乳膏。利用高压微射流装备制得的纳米乳的平均粒径为65nm,而用传统方法制得的微米乳的平均粒径为2788nm。将制得的微/纳米乳膏涂抹在已刮掉背毛仓鼠的背部,以2h后微/纳米乳膏的生物利用度为基准,3h后测得纳米乳膏的生物利用度翻了1倍,而微米乳膏只是2h后的1.1倍。Kakumanu等以吐温-80为乳化剂,大豆油为油相,利用高压微射流装备制备达卡巴嗪纳米乳。纳米乳的平均粒径为112nm,ζ电位为-3.2mV,提高其稳定性,有效地减小了异种移植老鼠皮肤癌肿瘤的尺寸。
脂质体,即单层或多层双脂膜结构的球形微粒,也是纳米乳的一种形式。脂质体的制备方法很多,但是多数不适合大规模、连续化生产。高压微射流均质法不仅克服了以上的缺点,而且达到更高的效果。Barnadas-Rodríguez 等利用高压微射流装备制备一系列的磷脂脂质体。压力0.4 MPa下处理9次,得到平均粒径为(39±7)nm、峰宽为(15±4)nm的脂质体; 压力0.2MPa下处理1次,得到平均粒径(319±6)nm,峰宽为(83.2±13.4)nm的脂质体。Saheki 等用高压微射流设备制备蛋卵磷脂和豆油混合的脂质纳米分散体,在 处理压力分别为108MPa和135MPa时,平均粒径均小于100nm,分散稳定性好。Chen等利用高压微射流装备在120MPa下,处理3次,制得粒径为(157.7±2.31)nm 的辅酶Q10 纳米脂质载体,效果是普通乳剂的10倍以上。
3.2 纳米混悬液
纳米混悬液是指用少量表面活性剂为稳定剂将难溶性固体纯药物以微粒状态分散于分散介质中形成的非均相胶体分散体系的液体制剂。与普通混悬剂相比,通常药用纳米混悬剂的平均粒径一般低于1000nm。纳米混悬剂属于热力学 不稳定而动力学稳定的粗分散体系,所以溶剂大多数为水,其稳定性的关键也在于表面活性剂,但制备纳米乳的药物要具有较大的脂溶性,纳米混悬剂则适用于大多数药物。纳米混悬剂制备的主要方法有研磨法、乳化法、蒸发沉降法、超临界流体法等,操作简单,工艺重现性好,易于工业化生产均采用高压微射流法。
Pardeike等利用高压微射流装备制备以吐温-80为润湿剂的不同质量浓度的磷脂酶A2抑制剂PX-18。所得的PX-18的平均粒径均小于1000nm,增加了药物溶解度,重现性好,提高药物的生物利用度,可用于静脉注射。周红玲等利用微射流均质设备在90MPa压力下处理3次制备丝裂霉素纳米混悬剂,经过超速离心机高速离心2h,得到丝裂霉素C-聚氰基丙烯酸丁酯纳米粒,测得平均粒径为113. 5 nm,包封率和载药量分别为( 85.1 ± 3.8) % 和( 7. 0 ± 0.2) % 。Liu 等利用沉淀-超声法和沉 淀-微流化法两种方法制备联苯双酯纳米混悬液,并 对其体外表征进行研究。在压力为23300psi下,处理10次,得到最佳的纳米混悬液。Mschwitzer等利用高压微射流装备在1500bar下循环处理40次制备胃酸分泌抑制剂奥美拉唑纳米混悬剂,在0 ℃下储存1个月仍具有良好的稳定性。
利用高压微射流法与其他方结合可以得到分散 稳定性好的纳米混悬液。Zhao等采用沉淀-高压微射流法结合法制备抗肿瘤药物羟喜树碱纳米混悬液,在压力为9000psi下处理5次,然后在压力为18000psi下处理10次,得到平均粒径为(286.9±6.1)nm,ζ电位为(-32.21±0.92)mV的纳米混悬液,大大增强了其抗肿瘤效果。胡婷婷等将高压微射流法与喷雾干燥法结合制得布地奈德多孔微球,在100MPa和循环60次的最佳条件制得平均粒径为0.64μm、峰宽为0.44 的布地奈德颗粒,经喷雾干燥后制得平均粒径为2.90μm和比表面积为8.71m2·g-1的多孔微球。
4 结论与展望
高压微射流技术是集物理、化学、工程学、微技术和生物技术于一体的多学科交叉的新兴技术。该技术可以与喷雾干燥法、薄膜分散法、乳化法、蒸发 沉淀法等技术联合使用,能制备粒径小且粒度分布窄而均匀的药物粒子。一般来说,随着处理压力增强,处理次数增多,粒径减小,分散稳定性增强。由于高压微射流装备使用简单、工艺重现性好,许多制药公司及其研发机构已经对其产生浓厚兴趣,对未来临床药物上市产品具有很大的应用前景。利用高 压微射流法制备化学小分子药物居多,在生物大分子及其中药领域的研究将备受期待。

来源:药物递送


