您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-19 10:26
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.复宏汉霖GARP单抗获批临床。复宏汉霖1类生物药HLX60获国家药监局临床许可,拟用于实体瘤和淋巴瘤的治疗。HLX60是国内首款获批临床的GARP单抗,可通过特异性结合GARP,阻断GARP介导的TGF-β1的释放,逆转TME中的免疫抑制效应,提高抗肿瘤免疫应答。此外,HLX60还可以通过抗体依赖细胞介导的细胞毒作用(ADCC)清除GARP阳性肿瘤细胞和Tregs等免疫抑制性细胞,从而发挥抗肿瘤作用。
2.海博为可透脑BTK抑制剂获批临床。海博为药业自主研发的1类化药HBW-3210胶囊获国家药监局临床许可。HBW-3210是一款三代BTK抑制剂,是海博为第二款获批临床的BTK抑制剂,其透脑率超过60%(大鼠透脑率>60%VS~10%)。该新药拟开发用于B细胞非霍奇金淋巴瘤,主要开发适应症为原发性/继发性中枢神经系统淋巴瘤或可能累及中枢神经系统的弥漫大B细胞淋巴瘤。
3.远大引进新型PET示踪剂获批临床。远大医药从Telix公司引进的新型PET示踪剂TLX591-CDx(Illuccix)获国家药监局临床试验默示许可。Illuccix是一款基于放射性核素-小分子偶联技术(RDC)的靶向前列腺特异性膜抗原(PSMA)的诊断型正电子发射断层扫描(PET)示踪剂,已获FDA批准上市,用于转移性前列腺癌及复发性前列腺癌的诊断成像。远大医药将在中国人群中开展TLX591-CDx的临床桥接研究。
4.北海康成AAV9基因疗法临床前数据积极。北海康成新型第二代自互补AAV9基因疗法(scAAV9-SMN1P-Co-hSMN1)将在欧洲基因与细胞治疗学会大会上,公布用于脊髓性肌萎缩症(SMA)小鼠模型的临床前研究数据。第二代基因疗法采用了内源性启动子的控制下表达密码子优化的人源SMN1基因的策略。与基准载体scAAV9-CMVEN/CB-hSMN1(该载体与FDA批准用于SMA的基因疗法相似)相比,第二代载体显示出更长的寿命、更好的肌肉功能恢复和更完整的神经肌肉接头神经支配,且安全性更优。
5.百奥赛图OX40单抗授权Syncromune公司。百奥赛图全资子公司祐和医药宣布与Syncromune公司达成协议,共同开发和商业化基于Syncrovax™技术的瘤内免疫疗法。根据协议,Syncromune将获得由祐和医药OX40单抗YH002和其他活性成分组成的瘤内免疫疗法用于Syncrovax™疗法的独家全球开发和商业化权益。祐和医药将保留YH002和其他活性成分除Syncrovax™外的所有全球权益。祐和医药将有望获得数亿美元的付款。
国际药讯
1.GABAA靶向抑郁症新药Ⅲ期临床成功。Sage公司与渤健开发的新一代GABAA变构调节剂zuranolone(SAGE-217/BIIB125)治疗产后抑郁症(PPD)的Ⅲ期临床SKYLARK最新数据积极。该项试验此前已达到主要终点以及所有的关键次要终点,且在服用后第3天便可见到抑郁症状的改善。此次次要终点数据显示,zuranolone(50mg)组较安慰剂在所有时间点达成HAMD-17响应的患者比例更高。两家公司预计今年下半年完成向FDA滚动递交NDA申请。
2.OSA口服复方Ⅱ期临床积极。Apnimed公司口服复方AD109(托莫西汀/aroxybutynin)治疗阻塞性睡眠呼吸暂停(OSA)的Ⅱb期临床MARIPOSA达到主要终点。与安慰剂相比,AD109显著降低患者呼吸暂停低通气指数(AHI)和打呼噜情形,且疗效可持续整晚;患者治疗后每小时睡眠时间内呼吸暂停加低通气次数下降超过50%的患者比例达到44%。药物最常见的不良反应为口干、失眠与恶心。
3.败血性休克靶向新药Ⅱb期临床积极。Inotrem公司选择性靶向TREM-1的抑制剂新药nangibotide在治疗败血性休克的Ⅱb期临床结果积极。在sTREM-1浓度较高的患者中,大剂量nangibotide较安慰剂显著改善患者的SOFA评分,SOFA评分显著改善的患者比例大约50%。该项研究首次证实TREM-1的过度活性与患者严重的免疫失调、器官功能紊乱以及最终死亡相关。除了抗生素和对症治疗之外,目前尚无针对败血性休克的特定疗法获批。
4.吉利德引进CD123/CD3双抗。吉利德和MacroGenics公司就后者临床早期、拟用于急性髓系白血病(AML)治疗的CD123×CD3双抗MGD024达成独家开发和商业化授权协议。根据协议,吉利德将向MacroGenics公司支付6000万美元的预付款和期权费,可能高达17亿美元的开发、监管和商业里程碑潜在付款。两家公司还可能在另外两个早期研究项目中进行合作。目前,吉利德AML在研管线还包括CD47单抗magrolimab和细胞疗法KITE-222。
5.Calico联手AI药物公司开发年龄相关FIC新药。Calico Life Sciences与Terray公司将利用后者专有的AI药物发现平台Terray tNova,针对Calico指定的一组靶点,合作开发抗癌症抗衰老的小分子候选药物。根据协议,Terray公司将负责先导化合物的开发活动;Calico将负责合作品种后续的临床开发和商业化。Calico将向Terray支付预付款,开发、监管和销售里程碑后期付款,以及产品的销售分成。
6.FDA要求IgA肾病新药提交REMS新计划。FDA针对Travere公司内皮素/血管紧张素受体拮抗剂(DEARA)sparsentan用于治疗IgA肾病的上市监管审查提出新的REMS(风险评估缓解策略)要求。FDA要求该公司更新拟议的REMS方案,将sparsentan的肝脏监测纳入其中,从而与内皮素受体拮抗剂类中的某些已批准产品一致。据悉,因肝毒性,辉瑞曾于2010年将内皮素受体拮抗剂sitaxsentan(西他生坦)撤市。
医药热点
1.上海交大医学院生物材料与再生医学研究院成立。10月14日,上海交通大学医学院生物材料与再生医学研究院揭牌成立。新成立的生物材料与再生医学研究院将整合医学院及其附属医院的临床特色资源,实现生物材料与再生医学领域创新链和产业链深度融合,推动交大医学院学科高质量发展。中国工程院院士戴尅戎、中国科学院院士葛均波任研究院学术委员会主任,上海交通大学医学院院长、中国工程院院士范先群任研究院院长,交大医学院附属第九人民医院院长吴皓任研究院执行院长。
2.广州一医院将升级超级传染病医院。10月12日,第四届广州市规划委员会地区规划专业委员会第六次会议召开,《广州市第八人民医院嘉禾院区地块(AB2112规划管理单元)控制性详细规划》在会上获审通过。根据规划,广州市第八人民医院将升级改造,打造规划总床位数3100床的「超级」传染病防治医院。
3.姜保国院士出任深圳大学医学部主任。10月15日,深圳大学医学部官网信息显示,中国工程院院士姜保国已担任深圳大学医学部主任,负责医学部全面工作。根据公开信息,姜保国,中国工程院院士,医学博士,在北京大学人民医院工作近30年,于2016年1月到2022年1月期间担任北京大学人民医院院长。姜保国院士致力于降低创伤致死率和致残率的学术研究,曾任中华医学会创伤学分会第七届主任委员;担任国家创伤医学中心主任、中国创伤救治联盟主席、中国医师协会创伤外科医师分会会长。
评审动态
1. CDE新药受理情况(10月18日)
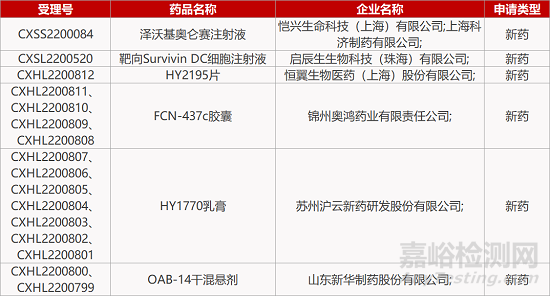
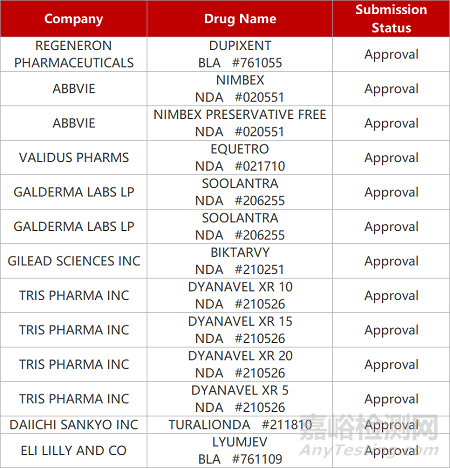

来源:药研发


