您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2022-11-12 03:34
“数字疗法”(Digital Therapeutics,DTx)是指由软件驱动的,为患者(或同时为患者和医疗机构)提供具有循证医学证据的疾病干预措施,用于疾病的预防、管理和治疗。“数字疗法”产品形式以软件为基础,可为独立软件,也可与通用计算设备、其他医疗器械、药物的一种或多种产品联合使用。主要通过信息(如图片、视频、音频等)、物理因子(如光线、声音、振动等)、药物等对患者施加影响,以达到疾病干预目的。
数字疗法主要采用心理学、神经科学、康复医学、药理学等医学理论对患者进行疾病干预,如心理学的认知行为疗法、神经科学的生物反馈疗法、康复医学的运动疗法、药理学的基于药代动力学的个性化用药指导等。主要用于心理、精神、运动-神经系统、感觉器官、慢性病等类疾病的干预,其中基于药代动力学的个性化用药指导主要适用于癌症等恶性疾病以及血友病等罕见病的治疗。
“数字疗法”类产品分类界定
1、管理属性界定
软件类产品的属性界定,应结合其处理对象、核心功能等因素,并基于其预期用途,进行综合判定。
若软件产品的处理对象为医疗器械数据,且核心功能是对医疗器械数据的处理、测量、模型计算、分析等,并用于医疗用途的,符合《医疗器械监督管理条例》有关医疗器械定义,作为医疗器械管理。若产品基于公开的临床指南、文献、公式等,对医疗器械数据进行简单的统计、运算等,不属于上述对医疗器械数据进行处理、测量、模型计算、分析等,亦不作为医疗器械管理。
软件的处理对象若为非客观医疗数据(如患者主诉等信息、病历、检验检查报告结论),或者其核心功能不是对客观医疗数据进行处理、测量、模型计算、分析,或者不用于医疗用途、不具备医疗目的的(如仅具备推送处方视频、播放音乐、缓解心情等功能),不作为医疗器械管理。
注:医疗器械数据是指医疗器械产生的用于医疗用途的客观数据,特殊情形下可包含通用设备产生的用于医疗用途的客观数据,“通用设备”应具有相应的质量控制措施和技术评价要求,以确保其产生的“用于医疗用途的客观数据”能够满足医疗用途。
2、管理类别界定
数字疗法主要涉及《医疗器械分类目录》的药物计算软件(分类编码21-04-01)和康复训练软件(分类编码21-06-01)。
其中,药物计算软件即为基于药代动力学的个性化用药指导软件,按照三类器械管理;康复训练软件所含产品较少,按照二类器械管理。而数字疗法主要用于心理、精神、运动-神经系统、感觉器官、慢性病等类疾病的干预,实际数字疗法产品现状与分类目录产品描述存在较大差距,同时有些数字疗法属于医疗技术而非医疗产品,目前针对“数字疗法”软件类产品管理类别可参考国家标管中心分类界定意见,后续仍需密切关注国家药监局针对此类软件的分类界定原则。
国家药监局近期发布文件
国家药监局为进一步加强软件类医疗产品监督管理,推动产业高质量发展,于2021年7月8日发布《人工智能医用软件产品分类界定指导原则》(2021年第47号)。其中《分类界定原则》明确规定对于属性判定作为医疗器械管理的人工智能医用软件类医疗产品,应当依据产品的预期用途、处理对象、核心功能等等综合判定产品管理类别。人工智能医用软件类产品的管理类别应当不低于二类。”
注册相关技术指导原则还包括:《医疗器械软件注册审查指导原则(2022年修订版)》(2022年第9号)、《医疗器械网络安全注册审查指导原则(2022年修订版)》(2022年第7号)、《人工智能医疗器械注册审查指导原则》(2022年第8号)、《移动医疗器械注册技术审查指导原则》(2017年第222号通告)、《医疗器械生产质量管理规范独立软件现场检查指导原则》(药监综械管[2020]57号)及《医用软件通用名称命名指导原则》(2021年第48号)。
“数字疗法”软件类产品涉及标准
“数字疗法”软件类产品的国行标包括:
1)GB/T25000.51-2016《系统与软件工程 系统与软件质量要求和评价(SQuaRE) 第51部分:就绪可用软件产品(RUSP)的质量要求和测试细则》(2017年5月1日实施);2)YY/T0664-2020《医疗器械软件 软件生存周期过程》(2021年9月1日实施);3)YY/T 1406.1-2016《医疗器械软件 第1部分:YY/T 0316应用于医疗器械软件的指南》(2017年1月1号)等。
国家标管中心分类界定结果汇总
1、作为第三类医疗器械管理的分类界定结果汇总


2、作为第二类医疗器械管理的分类界定结果汇总



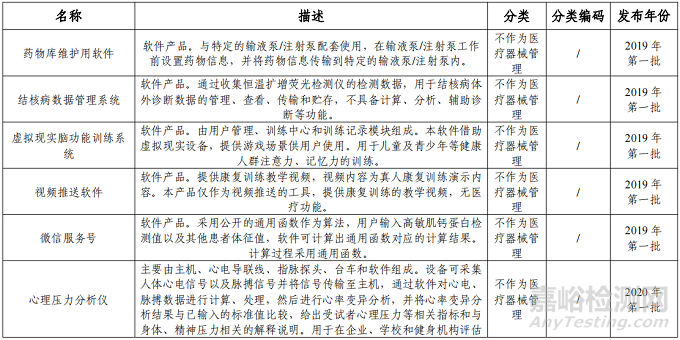
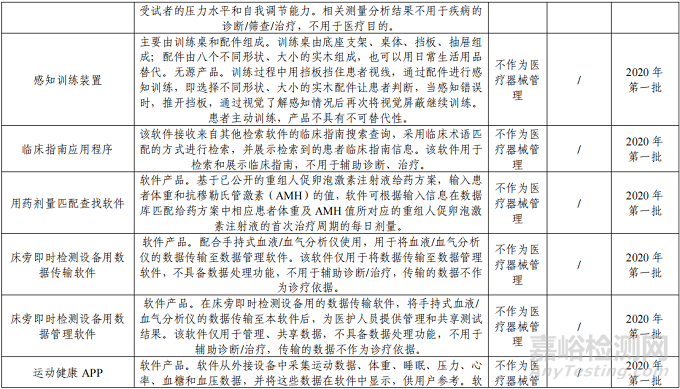
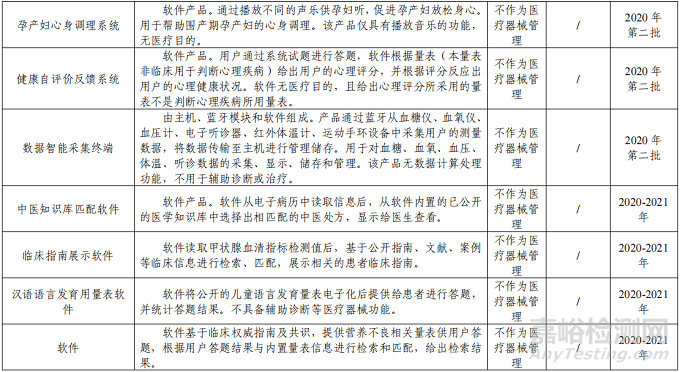
3、建议不作为医疗器械管理的分类界定结果汇总




来源:Internet


