今日头条
新元素医药痛风新药Ⅱa期临床积极。新元素医药尿酸转运蛋白1(URAT1)抑制剂ABP-671治疗痛风或高尿酸血症患者的中国Ⅱa期临床结果积极。在每天一次服用1mg ABP-671剂量组,86%的患者sUA水平低于6mg/dL;在每天一次服用6mg和12mg ABP-671的两个剂量组,100%的患者sUA水平降至5mg/dL以下,且分别有57%和100%的患者sUA水平低于4mg/dL;研究结果与此前在澳大利亚开展的Ⅱa期试验结果一致。
国内药讯
1.恒瑞PDL1单抗获批治疗小细胞肺癌。恒瑞医药1类新药PD-L1单抗SHR-1316(阿得贝利单抗注射液)获国家药监局批准上市,联合化疗一线治疗广泛期小细胞肺癌。发表在《柳叶刀-肿瘤学》上的Ⅲ期研究(CAPSTONE-1)结果显示,与化疗相比,SHR-1316联合化疗一线治疗显著提高患者总生存期(中位OS:15.3个月vs12.8个月)和无疾病进展期,显著降低患者疾病进展风险33%。患者的2年生存率达31.3%(vs17.2%)。
2.默沙东九价HPV疫苗新适应症在华报产。默沙东九价人乳头瘤病毒(HPV)疫苗(酿酒酵母)Gardasil 9新适应症上市申请获CDE受理。Gardasil 9采用三剂免疫程序,适用于预防HPV16、18、31、33、45、52和58型引起的宫颈癌;HPV6、11、16、18、31、33、45、52和58型引起的宫颈上皮内瘤样病变以及宫颈原位腺癌;以及HPV6、11、16、18、31、33、45、52和58型引起的持续感染。2022年8月,国家药监局已批准Gardasil 9由适用人群从19-26岁拓展至9-45岁适龄女性。
3.欧康维视干眼症新药上II期临床。欧康维视I类新药OT202滴眼液正式启动II期临床,评估治疗中重度干眼症的安全性和有效性。OT-202是一款脾酪氨酸激酶(Syk)与血管内皮生长因子受体-2双靶点抑制剂,在治疗干眼症方面可产生协同作用,从而抑制炎症反应。I期临床结果显示,OT-202在健康成人受试者中表现出良好的安全性和耐受性特征。
4.创胜CLDN18.2免疫PET探针见刊JPA。创胜集团开发的用于胃肠道肿瘤无创成像的靶向CLDN18.2免疫PET探针[89Zr]Zr-DFO-TST001的研究成果日前发布于期刊Journal of Pharmaceutical Analysis上。研究显示,探针不仅在细胞水平上表现出良好的特异性,且在24到96小时内呈现出快速而持续的肿瘤蓄积趋势。该研究为实时监测肿瘤患者的抗体治疗疗效提供一种有潜力的无创影像工具。TST001是创胜集团开发的一款CLDN18.2单抗,正在中美两国开展临床试验。
5.联邦RASP抑制剂获批干眼症临床。联邦制药1类新药TUL12101滴眼液获国家药监局临床试验默示许可,拟开发用于干眼的治疗。TUL12101是新一代小分子活性醛(RASP)抑制剂。RASP是炎症的前细胞因子介质,通过与蛋白质上的硫醇和胺残基结合,增强细胞因子释放,激活炎性小体。TUL12101通过可共价结合游离醛并降低过量的RASP水平,降低眼部活性醛的含量和缓解炎症反应。
国际药讯
1.礼来CDK4/6抑制剂获批扩大使用人群。礼来CDK4/6抑制剂阿贝西利获FDA批准扩大适应症,联合内分泌治疗(ET)用于HR+/HER2-、淋巴结阳性、高复发风险的早期乳腺癌成年患者的辅助治疗。阿贝西利是首个获批用于乳腺癌辅助治疗的CDK4/6抑制剂,FDA已于2021年批准阿贝西利联合ET方案,用于辅助治疗HR+/HER2-、淋巴结阳性、高复发风险且Ki-67≥20%早期乳腺癌患者。
2.GSK佐剂RSV疫苗获FDA推荐批准。FDA疫苗与相关生物制品产品咨询委员会(VRBPAC)推荐批准葛兰素史克呼吸道合胞病毒(RSV)疫苗RSVPreF3 OA上市,用于预防60岁及以上成人因RSV引起的下呼吸道疾病。RSVPreF3 OA由RSV融合前F糖蛋白(RSVPreF3)与佐剂组成。在Ⅲ期临床AReSVi-006中,该疫苗在≥60岁老年人中的保护效力达到82.6%(96.95% CI:57.9-94.1)。欧盟和日本监管部门已受理该疫苗的上市申请。
3.Checkpoint公司PD-L1单抗报BLA。Checkpoint公司PD-L1抗体cosibelimab的生物制品许可申请(BLA)获FDA受理,用于治疗转移性或局部晚期皮肤鳞状细胞癌(cSCC)患者。PDUFA日期为2024年1月3日。在临床试验中,cosibelimab在转移性cSCC患者中达到47.4%(95% CI:36.0, 59.1)的客观缓解率(ORR);在晚期cSCC患者中ORR为54.8%(95% CI:36.0, 72. 7)。cSCC是美国第二大常见的皮肤癌类型,每年发病患者达180万例。
4.VMAT2抑制剂治疗TD长期疗效积极。Neurocrine公司VMAT2抑制剂Ingrezza(valbenazine)治疗迟发性运动障碍(TD)年长患者的最新结果积极。Ingrezza旨在通过减少多巴胺量来调节TD患者的神经信号。48周治疗数据显示,在≥65岁的患者中,达成异常不自主运动量表(AIMS)反应改善≥50%的患者比例超过80%。详细数据将公布于2023年美国老年精神病学协会(AAGP)年会当中。
5.HPV DNA疫苗III期临床积极。Inovio公司DNA治疗性疫苗VGX-3100(ABC-3100)治疗成年女性中高危型HPV-16/18感染相关的宫颈高级别鳞状上皮内病变(HSIL)的III期临床(Reveal 2)数据积极。汇总分析显示,在所有研究人群中,VGX-3100组和安慰剂组达到主要终点的患者比例分别为25.0%和9.8%(p<0.001);在生物标志物阳性患者中,两组这一数值分别为54.4%和12.5%(p<0.001)。临床中,没有与治疗相关的严重不良事件。北京东方略拥有该药的中国权益。
6.氨甲蝶呤玻璃体内注射配方报NDA。Aldeyra公司非复合型的氨甲蝶呤玻璃体内注射配方ADX-2191(methotrexate injection)的新药申请(NDA)获FDA受理,用以治疗原发性玻璃体视网膜淋巴瘤。FDA同时授予其优先审评资格。PDUFA日期为今年6月21日。去年10月,ADX-2191在治疗增生性玻璃体视网膜病变的Ⅲ期临床GUARD达到主要终点,与历史对照组(无治疗例行手术治疗)相比,ADX-2191显著降低患者的视网膜脱落情形(P=0.024);且药物总体耐受性良好。
医药热点
1.安徽省首家医疗机构“生物银行”获批。近日,安徽省妇幼保健院(合肥市妇幼保健院)生物样本库顺利获批中国人类遗传资源保藏行政许可,成为安徽省首家获得行政许可的,拥有生物样本库的医疗卫生机构。样本库主要面向母婴自然人群、妊娠高血压、妊娠糖尿病、不良生育史的夫妇,以及儿童罕见病和妇科肿瘤患者等,能为相关疾病的临床研究提供科研材料,为疾病早期的实验技术提供支持。
2.全国政协委员曹菲建议医院设置上门看诊。2023年全国“两会”召开,政协委员曹菲建议“医院设置上门看诊,协助设置家庭病房;社区建立24小时响应体系,搭建护工(每天4-6次)、护士(每周一次)、医生(双休或每月一次)三层级分时不同频度的巡视的体系;制定相应标准,完善居家养老设施”。
3.张文宏呼吁进一步加强社区医卫体系建设。3月4日,全国政协十四届一次会议首场“委员通道”集体采访举行。全国政协委员张文宏教授在接受采访时呼吁,我国目前已进入疫情舒缓阶段,国家应继续强化基层医疗卫生体系。他期待未来三级医院既能赋能基层医疗卫生机构,又能与之相互分级、分层、分流,打造出一个上下联动、平急转换,既有弹性又有韧性的医疗卫生体系。
4.全球药企TOP10名单出炉。随着2022年财报的披露,全球TOP10药企排名正式出炉。按照公司总收入,全球药企TOP10分别为辉瑞、强生、罗氏、默沙东、艾伯维、拜耳、诺华、BMS、赛诺菲和阿斯利康。按照制药业务收入,全球药企TOP10分别为辉瑞、艾伯维、强生、默沙东、诺华、罗氏、BMS、阿斯利康、赛诺菲和GSK。按照公司市值,全球药企TOP10分别为强生、诺和诺德、礼来、默沙东、艾伯维、罗氏、辉瑞、阿斯利康、诺华和BMS。
评审动态
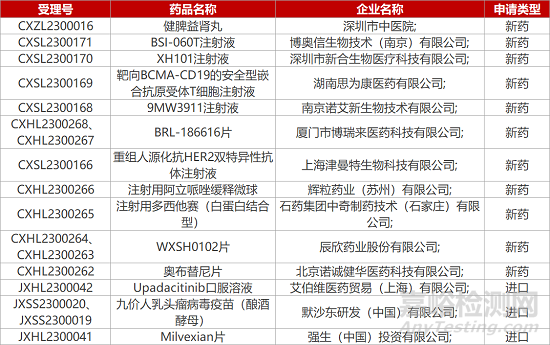
1. CDE新药受理情况(03月04日)
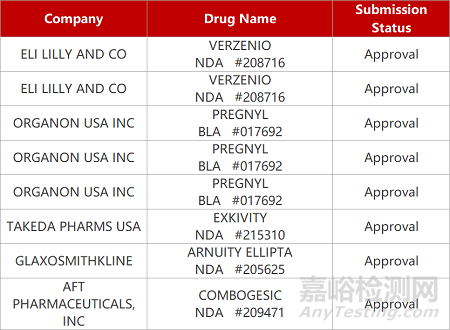
2. FDA新药获批情况(北美03月03日)