生物制药市场正在迅速增长,预计在2018年至2024年之间,复合年增长率为8.6%,到2024年将达到3,900亿美元。单克隆抗体(mAB)是市场上的主要蛋白质类型药物,占总市场的四分之一。单克隆抗体领域始于30年前,批准了用于预防肾脏移植排斥反应的Orthoclone OKT3,此后,每年都有三到五种基于单抗的新产品获批。目前,药品市场以生产生物仿制药为导向,预计蛋白质药物的数量将进一步增长。生物大分子分子量大且不稳定,通常采用肠胃外给药。蛋白质的稳定性是生物制药设计和开发的主要出发点。冻干是制造稳定的生物制药产品的首选方法,目前50%的生物药采用冻干制剂从而保证其使用稳定性。由于生物药的复杂性和敏感性,通常加入药物特异性辅料来优化冻干过程,以使其生物活性成分稳定。例如,皮下注射治疗性蛋白药物由于粘度高导致可注射性降低和复溶时间增长,需要加入降粘剂,以降低溶液粘度。
一、生物制剂处方稳定性
溶液中的蛋白质通常不稳定,冻干是实现稳定生物制药配方的主要方法,但受冻干条件影响,蛋白质分子可能会不稳定。化学不稳定性会导致肽共价键的形成或破坏,从而产生新的化学体。常见的过程包括氧化、脱酰胺和异构化。脱酰胺容易发生在中性和碱性pH值下,碱性条件下的脱酰胺比例是酸性条件下的三倍。异构化通常发生在中性或酸性条件下,可能导致蛋白分子的亲和力降低。物理不稳定会导致蛋白质变性和聚集,影响物理稳定性的因素包括 pH 值、温度、离子强度、冻融、蛋白质浓度和机械应力。糖、聚合物、表面活性剂、多元醇和氨基酸等辅料对于在冻干和储存期间稳定生物蛋白制剂至关重要,但由于肠外制剂的监管要求,其选择十分有限。
二、冻干过程
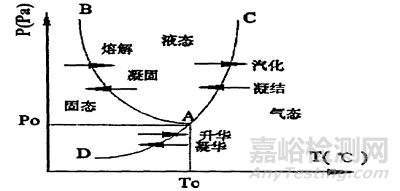
冻干是在冷冻后通过升华从生物制药药物中去除水分的过程,这种技术的时间和经济成本通常较高。冻干过程包括冷冻、初级和次级干燥步骤。
冷冻步骤旨在将大部分水变成冰,形成冻结浓缩溶液。冷冻期间的温度必须设置在最大冻结浓度溶液的玻璃化转变温度和结晶材料的共晶温度以下。退火是冷冻后执行的一步,可形成更大、更均匀的冰晶并使填充剂结晶,从而提高初级干燥的效率。冷冻过程中蛋白质分子所在的体系特性会发生变化,影响产品的稳定性。冷却速度会影响冰晶的大小和形态,进而影响冻干的干燥阶段。蛋白质浓度、类型和退火步骤的加入也会影响产品复溶时间。
初级干燥通过升华去除冷冻的游离水,适当选择板层温度和压力值可以缩短该过程。初级干燥是冻干过程中最耗时和能量的阶段,通常最佳压力为0.1-0.2 mbar,板层温度选择基于玻璃化转变温度Tg'和塌陷温度Tc。通常将产品温度保持在Tg'以下2-3°C以保持蛋白质稳定性,但是适当的处方优化甚至允许产品在Tg'或Tc以上进行干燥。当产品温度Tp等于板层温度时,初级干燥即完成。通常Tg'和Tc可以分别通过差示扫描量热法和冻干显微镜来确定。
二次干燥通过解吸去除未冷冻的结合水,以避免储存期间出现蛋白质稳定性问题。为了避免样品崩溃,应逐渐提高板层温度,一般不超过50°C,时间通常不超过6h。干燥结束后,产品中的残留水分为应符合要求。根据QbD原则,过程分析技术的主要目的是提高过程效率并保证产品的关键质量属性。近年来,已经开发出用于在线和实时测量的新工具,如温度远程监控系统和TrackSense Pro系统,基于对产品温度、板层温度和腔室压力的监控,可以确定一次干燥甚至二次干燥的终点。LyoTrack系统基于光学发射光谱测量干燥室内的水分浓度,从而获得更准确的干燥终点。压力温度测量是一种压力上升测试,当干燥室中的蒸汽压力不再上升时,初级干燥完成。此外,通过使用近红外和拉曼探头,可以监测冻干配方的中间参数,例如过程诱导的转变、结晶、固态化、多晶型转化和残余水分含量。过程分析技术工具以及相应的属性如下表。
三、冻干制剂辅料
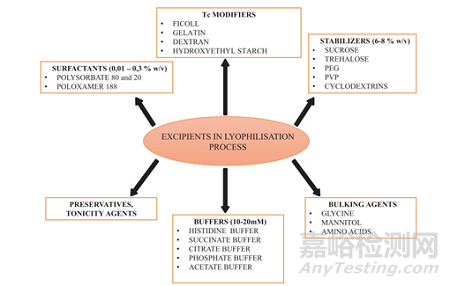
选择合适辅料能有助于产品在冻干过程中获得理想的质量属性和稳定性,并降低生产的时间和经济成本,提高产量。下图为生物药冻干制剂常用辅料选用:
1. 稳定剂
冻干过程中蛋白质的稳定基于两种主要机制:玻璃化和水置换理论。玻璃化定义了蛋白质分子在由无定形稳定剂形成的基质中的固定化,从而降低蛋白质分子之间的相互作用,从而防止其结构的变化。水置换机制是基于稳定剂糖的羟基和蛋白质的极性基团之间氢键的形成,在干燥过程中取代了水和蛋白质之间的氢键,从而允许保留蛋白质分子的天然形式。玻璃化理论代表动力学稳定,而水替代理论代表稳定的热力学方面,动力学稳定与Tg密切相关。Tg的测定对于选择适当的储存和运输条件至关重要。在冻结态下,无定形辅料和蛋白质形成玻璃状基质温度低于该温度Tg。但即使在低于Tg的温度下,蛋白质迁移也可以加速降解反应。蛋白质会增加制剂处方的Tg,需要添加Tg值相对较高的辅料以保持蛋白质稳定性,特别是在高浓度蛋白质制剂中。研究显示,在蔗糖作为稳定剂制剂中添加山梨糖醇而增加的分子迁移率不会影响在Tg温度下储存的蛋白质的稳定性,这表明迁移率(即动力学稳定)对于蛋白质稳定性并不重要。此外,最终产品的水含量应在最佳范围内,过度干燥不利于蛋白质稳定性。不建议以<1% (w/v)为干燥最终水分控制标准,但较高的残留水也会降低储存条件下制剂处方的Tg从而降低蛋白质稳定性。因此,需要选择冻干过程中最佳的二次干燥条件,以保证合适水分量的控制【1】。
临界温度Tg'和Tc也是稳定剂的重要特性,它们决定了冻干过程的温度条件和干燥周期的持续时间。较高Tg'和Tc的稳定剂有助于减少冻干时间,通常为了得到合适的干燥时间,稳定剂的Tg'不应小于-40°C。加入具有较高临界温度的辅料可以在较高的产品温度Tp(高于Tg',甚至高于Tc)下进行初级干燥,从而缩短初级干燥时间而不会发生塌陷。蔗糖和海藻糖在冻干过程和储存过程中对增加蛋白质稳定性都非常明显。主要原因是这两种糖在冻干过程中不易结晶,从而不会与蛋白质相分离。不建议使用结晶性的填充剂作为稳定剂,如甘露醇和甘氨酸。与海藻糖相比,蔗糖更便宜经济。海藻糖作为稳定剂的优势在于其较高Tg为111°C,而蔗糖Tg为65°C【2】。
保证稳定性的重要因素是稳定剂和蛋白质之间的适当比例。糖和蛋白质之间的摩尔比应至少为360:1【3】。添加过量糖会降低Tg'。优化冻干过程的方法是选择具有高稳定性效果和高临界温度Tǵ和Tc的替代辅料,高于蔗糖和海藻糖。包含具有高Tg'和Tc改性剂的辅料,允许产品在更高的干燥温度下进行初级干燥而不会破坏产品结构。此外,Tc改性剂和填充剂通过形成晶格的组合可以在产品温度高于Tc的情况下进行初级干燥,而不影响蛋白质稳定性和不发生塌陷【4】。下表列出的稳定剂辅料(除山梨醇外)Tg'都高于蔗糖(这意味着可能使用更高的干燥温度来缩短干燥过程)。为了确保蛋白质的稳定性并防止相分离,建议将蔗糖和葡聚糖结合使用【2】。
聚乙烯吡咯烷酮PVP也是一种可用于稳定剂的聚合物,它可以抑制缓冲盐的结晶,PVP通常与糖结合使用。对于肠外剂型,由于易在体内积聚不推荐使用高分子量PVP【5】。羟丙基-β-环糊精可以作为稳定剂或表面活性剂,通过水替代理论和增加冻干体系Tg来稳定蛋白质。如果将环糊精用作冻干保护剂,则浓度通常在1-10%(w / v)。环糊精还能限制已经具有结晶倾向的稳定剂结晶,因此其主要帮助在生产和储存过程中蛋白质保持稳定。羟丙基-β-环糊精的两亲性质通过防止蛋白质在界面处展开和聚集,从而在冷冻、干燥和复溶过程中增加蛋白质稳定性,从而起到表面活性剂的作用。除了与蛋白质相互作用外,它还降低了表面张力,从而防止空气/水、冰/水和固体/空气界面的不稳定。研究显示羟丙基-β-环糊精在低浓度(0.1% w/v)下能表现出表面活性剂作用【6】。下表列出生物冻干制剂中的各种稳定剂及其关键参数。
在氨基酸中,最常用作稳定剂的是甘氨酸、组氨酸和精氨酸。组氨酸在保持在无定形状态时作为缓冲液和冷冻/冻干保护剂,以及作为抗氧化剂。在冻干制剂中,甘氨酸通常作为填充剂或缓冲剂添加,而其稳定特性显示出与糖的协同作用。精氨酸稳定作用是基于其与蛋白质表面的弱结合,可以防止蛋白质相互作用和聚集,同时它在冻干期间和之后表现为无定形状态。在用于皮下给药的高浓度蛋白质制剂方面精氨酸使用较多,盐酸精氨酸降低制剂的粘度并有助于增加蛋白质溶解度。此外,脯 氨酸、丙氨酸、丝氨酸、苯丙氨酸、异亮氨酸、亮氨酸、赖氨酸和缬氨酸等氨基酸也可能被用作稳定剂,通常为了增强蛋白质的稳定性而与二糖联合使用。除精氨酸盐酸盐、赖氨酸盐酸盐、组氨酸盐酸盐可作为降粘剂外,不同的盐(NaCl、NaAc、Na2所以4和 NH4Cl)以及将一些辅料改性成疏水盐也可以降低高浓度蛋白的粘度【2】【7】。
2. 填充剂
填充剂能为冻干饼提供适当的结构,有助于冻干饼块的适当形态,形成孔结构,孔隙率是冷冻水升华的先决条件,较大的孔隙可以更快地升华,因此可以减少初级干燥时间。添加填充剂可实现更短的初级干燥(产品温度Tp˃Tg'或Tc)时间,可作为优化生物制药冻干过程的方法。
通常稳定剂与填充剂的比例应至少为1:2,以提供必要的填充剂结晶。形成的晶格为处于无定形状态的成分提供机械支撑。在Tg'上方,制剂体系形成的无定形状态刚性不够,无法支撑其自身重量,并且会坍缩到晶体网络上。由于机械支撑,尽管干燥温度高于Tg'(甚至高于Tc),但仍可以防止塌陷发生。在蛋白质浓度<50 mg/mL的处方中,添加填充剂尤为重要,因为在蛋白质浓度较高的配方中体系的Tg′会增加。但如果填充剂在冻干过程中保持无定形状态,由于储存过程中潜在的结晶,可能会影响蛋白质稳定性,因此,通常加入退火步骤可促进填充剂的结晶。市售产品大多以甘露醇或甘氨酸作为填充剂,因为它们具有高结晶倾向。甘露醇/冰和甘氨酸/冰混合物具有较高的共晶熔融温度,分别为-1.5°C和-4°C。即使甘氨酸的部分结晶(蔗糖与甘氨酸的比例为2:1)也能使体系在更高的干燥条件下进行而不会对冻干饼结构产生影响。与未退火的无定形制剂相比,退火后部分结晶的甘露醇有助于缩短高浓度蛋白质制剂的复溶时间。但是填充剂的物理状态还取决于蛋白质的类型、浓度、pH和缓冲液浓度。研究显示将冻干溶液中的pH值从5.9降低到3.0,并将磷酸盐缓冲液浓度从50mM增加到250mM会降低甘氨酸结晶速率【8】。
填充剂对蛋白质稳定性的影响很小(填充剂的结晶度增加还是会或多或少导致蛋白质物理稳定性降低)或没有影响。因此需要选择合适的填充剂和稳定剂,由于二者的协同作用,含有稳定剂和填充剂的配方有助于提高物理稳定性。但是当使用的稳定剂阻止填充剂结晶导致支撑非晶相的晶格无法形成时,将会影响初级干燥温度。研究发现添加甘露醇作为填充剂几乎不会损害蛋白质稳定性,同时防止在冻干中塌陷【9】。
除了甘露醇和甘氨酸,葡聚糖和PEG,苯丙氨酸、异亮氨酸、亮氨酸、蛋氨酸、精氨酸和组氨酸等氨基酸也可以作为填充剂。研究显示,与甘氨酸和甘露醇相比,其他作为填充剂的氨基酸可以在较低的浓度下结晶,蔗糖与氨基酸的比例为2.5-47.5已被证明足以促进结晶。但为了得到更好的外观和是蛋白质稳定性更好,蔗糖与氨基酸(即亮氨酸、异亮氨酸、苯丙氨酸)的最佳比例为4:1【10】。
3. 缓冲剂
缓冲剂的作用是将溶液的pH值维持在保持蛋白质具有较好稳定性的条件。可根据蛋白质的等电点选择溶液的pH,为了防止使用后的刺激,疼痛和副作用,pH需要在人体生理可接受范围内。结合目前已上市的生物制剂以及相关研究,生物蛋白质药物大多缓冲区间在pH4.6-8.2范围内。蛋白质分子在冻干、复溶和储存过程中暴露于不同的降解条件,因此选择合适的缓冲液至关重要。
对于冻干制剂,最常用的缓冲液是非氨基酸缓冲液,例如磷酸缓冲液、乙酸缓冲液、柠檬酸缓冲液和琥珀酸缓冲液。对于氨基酸缓冲液的使用,组氨酸缓冲液是使用最广泛的。柠檬酸盐缓冲液通常是最先考虑的,因为它的盐组分在冷冻过程中表现出低结晶倾向,并且具有高临界温度Tc,这有助于缩短初级干燥时间。在冷冻过程中需要避免缓冲盐的结晶,因为结晶会改变体系pH值并导致蛋白质不稳定(在磷酸钠溶液的冷冻过程中,二钠盐的结晶会导致pH值降低至3个pH单位)。虽然一些情况下添加填充剂如甘露醇和甘氨酸,可能会促进缓冲盐结晶,但填充剂对缓冲盐的结晶影响主要取决于填充剂的浓度,浓度<50 mM的甘氨酸抑制磷酸盐缓冲液中二钠盐的结晶,而当浓度较高时,结晶速率明显增加,如下图。此外,冷冻过程中磷酸盐缓冲液的急剧pH变化也会导致蛋白质的不稳定,但通常加入稳定剂后处于无定型状态的稳定剂能很大程度缓解缓冲液结晶和pH变化引起的蛋白质不稳定,各辅料起到协同作用【11】。
此外,当缓冲液处于非结晶状态下时,其pH对温度敏感性也值得关注,非结晶状态下,Tris缓冲液比磷酸盐缓冲液更容易受温度影响。当温度降低时,Tris(PKa7.4)缓冲液的缓冲能力会降低,而当温度升高时,pH值也可能会上升,因此尤其是在配制和使用Tris缓冲液时,需要特别注意合适的温度范围。
4. 表面活性剂
表面活性剂在蛋白质制剂中的作用是通过表面活性剂吸附到蛋白质表面的疏水区域或冰/空气和水之间的界面来防止蛋白质表面聚集。表面活性剂增加了蛋白质展开所需的自由能,并降低了冻干和复溶过程中形成界面的表面张力。在复溶过程中,有助于冻干饼块的复溶。
与离子表面活性剂相比,非离子性质不会促进蛋白质变性如聚山梨酯80和20是最常用的。使用聚山梨酯时,必须考虑其对氧化和水解的敏感性。其可能形成的降解产物(例如,过氧化氢,甲酸)会对蛋白质稳定性产生影响。此外,还需要考虑聚山梨酯的成分、等级和来源。药典规定,聚山梨酯80(II)含油酸应不低于98.0%,含肉豆蔻酸、棕榈酸、棕榈油酸、硬脂酸、亚油酸与亚麻酸均不得超过0.5%。而聚山梨酯20含月桂酸应为40.0%~60.0%,含肉豆蔻酸应为14.0%~25.0%,含棕榈酸应为7.0%~15.0%,含己酸、辛酸、癸酸、硬脂酸、油酸与亚油酸分别不得过1.0%、10.0%、10.0%、7.0%、11.0%与3.0%。此外,泊洛沙姆是可以代替聚山梨酯使用的比较有前景的表面活性剂,但是目前它们在市售产品中的使用量很低。
在冻干过程中,药物制剂中的蛋白质分子可能会受到不同因素影响,包括pH,脱水,离子强度增加,水/冰界面的形成和温度变化。通过选用合适的辅料,不仅可以提高生物制药的稳定性,还可以影响冻干过程的参数。因此,这些辅料对于降低成本冻干工艺至关重要,这些工艺可提供具有可接受的冻干饼结构和所需关键质量属性的稳定产品。最重要的辅料是稳定剂。除蔗糖和海藻糖外,具有较高Tǵ和Tc的新型稳定剂如PEG,低分子量PVP和环糊精等能够使产品在相对较高温度下进行初级干燥,从而缩短初级干燥时间,这从工业角度来看尤为重要。稳定剂为蛋白质分子提供稳定性,填充剂负责有助于冻干饼的合适外观和孔隙率,以及无定形材料的机械支撑,从而有助于缩短初级干燥时间。从生物制药皮下应用的当代趋势来看,新型辅料也越来越受到关注,特别是在高浓度蛋白质配方方面。
参考文献:
[1] Liuquan, Lucy, Chang., Deanna, Shepherd., Joanna, Sun., Xiaolin, Charlie, Tang., Michael, J., Pikal. "Effect of sorbitol and residual moisture on the stability of lyophilized antibodies: Implications for the mechanism of protein stabilization in the solid state." Journal of Pharmaceutical Sciences, 94 (2005).:1445-1455. doi: 10.1002/JPS.20363
[2] Valeria, Gervasi., R., Dall, Agnol., S., Cullen., T., McCoy., Sonja, Vucen., Abina, M., Crean. "Parenteral protein formulations: An overview of approved products within the European Union.." European Journal of Pharmaceutics and Biopharmaceutics, 131 (2018).:8-24. doi: 10.1016/J.EJPB.2018.07.011
[3] J.L. Cleland, X. Lam, B. Kendrick, J. Yang, T.H. Yang, D. Overcashier, D. Brooks, C. Hsu, J.F. Carpenter A specific molar ratio of stabilizer to protein is required for storage stability of a lyophilized monoclonal antibodyJ. Pharm. Sci., 90 (2001), pp. 310-321, 10.1016/j.talanta.2017.01.023
[4] E.Y. Shalaev, W. Wang, L.A. Gatlin Rational choice of excipients for use in lyophilized formulations E.J. McNally, J.E. Hastedt (Eds.), Protein Formulation and Delivery, Informa Healthcare (2007), pp. 197-219
[5] S. Pramanick, D. Singodia, V. Chandel Excipient selection in parenteral formulation development, 45 (2013), pp. 65-77
[6] T. Serno, R. Geidobler, G. Winter Protein stabilization by cyclodextrins in the liquid and dried stateAdv. Drug Deliv. Rev., 63 (2011), pp. 1086-1106, 10.1016/j.addr.2011.08.003
[7] S. Wang, N. Zhang, T. Hu, W. Dai, X. Feng, X. Zhang, F. QianViscosity-lowering effect of amino acids and salts on highly concentrated solutions of two IgG1 monoclonal antibodies Mol. Pharm., 12 (2015), pp. 4478-4487, 10.1021/acs.molpharmaceut.5b00643
[8] D.B. Varshney, S. Kumar, E.Y. Shalaev, P. Sundaramurthi, S.-W. Kang, L.A. Gatlin, R. Suryanarayanan Glycine crystallization in frozen and freeze-dried systems: effect of pH and buffer concentrationPharm. Res., 24 (2007), pp. 593-604, 10.1007/s11095-006-9178-z
[9] K. Schersch, O. Betz, P. Garidel, S. Muehlau, S. Bassarab, G. Winter Systematic investigation of the effect of lyophilizate collapse on pharmaceutically relevant proteins I: stability after freeze-dryingJ. Pharm. Sci., 99 (2010), pp. 2256-2278, 10.1002/jps.22000
[10] J. Horn, E. Tolardo, D. Fissore, W. FriessCrystallizing amino acids as bulking agents in freeze-dryingEur. J. Pharm. Biopharm. Off. J. Arbeitsgemeinschaft Pharm. Verfahrenstechnik EV, 132 (2018), pp. 70-82, 10.1016/j.ejpb.2018.09.004
[11] Pikal-Cleland KA, Cleland JL, Anchordoquy TJ, Carpenter JF. Effect of glycine on pH changes and protein stability during freeze-thawing in phosphate buffer systems. J Pharm Sci. 2002 Sep;91(9):1969-79. doi: 10.1002/jps.10184. PMID: 12210044.