今日头条
天广实CD20抗体膜性肾病Ⅱ期临床积极。天广实宣布在ERA大会上公布第三代CD20抗体MIL62治疗膜性肾病患者的Ⅱ期临床积极数据。与对照组相比,MIL62单药治疗24周肾脏总体缓解率显著更高(62.7%vs34.8%);该组患者在抗PLA2R抗体滴度、尿蛋白、血清白蛋白和肾小球滤过率等指标的改善方面均具有显著获益;药物的总体耐受性良好。目前该新药正在Ⅲ期临床中评估治疗原发性膜性肾病的潜力。
国内药讯
1.和黄医药VEGFR抑制剂欧盟报产。和黄医药与武田联合开发的VEGFR抑制剂呋喹替尼的新药上市申请获欧洲药品管理局(EMA)受理,用于治疗经治转移性结直肠癌患者。在III期FRESCO2研究中,与安慰剂相比,呋喹替尼治疗组的mOS延长2.6个月,mPFS延长1.9个月。在中国,该新药已获批用于既往接受过氟嘧啶、奥沙利铂和伊立替康治疗的转移性结直肠癌患者。
2.基石PD-L1单抗肺癌Ⅲ期临床见刊Nature子刊。基石药业PD-L1单抗舒格利单抗一线治疗IV期非小细胞肺癌(NSCLC)的Ⅲ期(GEMSTONE-302)研究在线发表在《自然》子刊Nature Cancer上。舒格利单抗联合化疗治疗的中位OS为25.4个月(vs16.9个月),2年OS率为51.7%(vs35.6%)。在脑转移患者中,舒格利单抗联合化疗治疗的中位OS为22.1(vs9.0个月)。在ITT人群中,舒格利单抗联合化疗的中位PFS为9.0个月(vs4.9个月),2年PFS率为20.8%(vs7.3%)。
3.奥赛康CLDN18.2单抗胃癌早期积极。奥赛康药业子公司AskGene抗CLDN18.2单抗ASKB589用于实体瘤治疗的Ⅰ/Ⅱ期试验最新结果将在IGCC大会上公布。数据显示,在Ⅱ期临床扩组研究中,经研究者确认,ASKB589联合CAPOX(一种包括卡培他滨和奥沙利铂的联合化疗方案)治疗在24例CLDN18.2中高表达的胃癌或胃食管交界处腺癌患者中达到79.2%的客观缓解率(cORR),疾病控制率(DCR)达95.8%。药物总体耐受性良好,无剂量限制性毒性。
4.复宏汉霖LAG-3单抗启动肺癌II期临床。复宏汉霖LAG-3单抗HLX26登记启动一项II期临床,拟评估与PD-1单抗斯鲁利单抗和化疗联用一线治疗晚期非小细胞肺癌(NSCLC)患者中的有效性、安全性和耐受性。该项试验拟入组72人;主要研究者将由复旦大学附属肿瘤医院主任医师王佳雷担任。去年10月,该联合疗法启动了一项针对结直肠癌的II期临床(登记号:NCT05584137)。
5.科伦TROP2-ADC获EMA批准Ⅱ期临床。科伦博泰TROP2-ADC新药SKB264(MK-2870)获欧洲药品管理局(EMA)批准开展II期临床,拟联合默沙东PD-1单抗帕博利珠单抗用于治疗晚期实体瘤患者。这是一项国际多中心临床研究,该组合疗法已分别获得中国、美国、加拿大、澳大利亚等多个欧盟国家的临床批件。SKB264是由科伦博泰采用专有毒素-连接子策略(Kthiol设计策略)研发的一款靶向TROP2的创新ADC。
6.天港医诺FIC双抗获批临床。天港医诺开发的靶向一个全新靶点的双特异性抗体药物TGI-6获FDA批准开展Ⅰ期临床试验。TGI-6可以同时特异性结合肿瘤细胞表面的肿瘤相关抗原和T细胞表面的CD3分子,强烈活化T细胞并杀伤肿瘤细胞。在临床前研究中,TGI-6在结直肠癌动物模型中单次给药已显示出完全清除肿瘤的潜力。该产品拟开发用于治疗结直肠癌及其它肿瘤相关抗原阳性实体瘤。
国际药讯
1.艾伯维IL-23抗体治疗UC的Ⅲ期临床积极。艾伯维IL-23抑制剂Skyrizi(risankizumab)用于维持治疗中重度溃疡性结肠炎(UC)的Ⅲ期COMMAND临床达到主要终点以及关键次要终点。与对照组相比,180 mg、360 mg risankizumab维持治疗在52周时达到临床缓解的患者比例更高(40%和38%,vs25%,p<0.01);达到内镜检查改善的患者比例更多(51%和48%,vs32%,p<0.001);达到组织学内镜检查粘膜改善的患者比例也更高(43%和42%、vs23%,p<0.001)。
2.罗氏TIGIT单抗启动肝癌III期临床。罗氏在clinicaltrials.gov网站上登记启动一项III期临床IMbrave152/SKYSCRAPER-14,拟评估TIGIT单抗tiragolumab联合PD-L1抑制剂阿替利珠单抗+贝伐珠单抗(VEGF)一线治疗局部晚期或转移性肝细胞癌(HCC)的疗效。公布于ASCO2023年会上的Ib/II期Morpheus-Liver临床数据显示,与阿替利珠单抗联合贝伐珠单抗相比,tiragolumab联合治疗显著提高患者的客观缓解率(ORR:42.5%vs11.1%)和无进展生存期(中位PFS:11.1个月vs4.2个月,HR:0.42(95% CI:0.22-0.82)。
3.ITK抑制剂T细胞淋巴瘤早期临床积极。Corvus公司ITK抑制剂CPI-818治疗T细胞淋巴瘤(TCL)的Ⅰ/Ⅰb期临床中期结果积极。数据显示,CPI-818在30例复发性TCL患者中有3例实现完全缓解(CR)、3例实现部分缓解(PR),其中1例PR患者表现出肿瘤持续消退。在淋巴细胞计数(ALC)高于900/立方毫升血液的14例患者中,有6例达到客观缓解(CR、PR),12例达到疾病控制(CR、PR和疾病稳定)。
4.刘如谦团队碱基编辑通用CAR-T研究见刊。刘如谦团队碱基编辑通用CAR-T治疗复发性T细胞白血病患者的首次人体试验最新数据发表在《新英格兰医学杂志》上。结果显示,患有T细胞急性淋巴细胞白血病(T-ALL)的13岁患者在接受治疗四周后,其白血病症状消失,后续成功进行骨髓移植后在将近一年的时间内仍很健康;第2例患者在同样时间内清除了白血病,接受移植后在家中康复;第3例患者由于后续感染真菌死亡。
5.渤健合作开发渐冻症创新组合复方。渤健与NeuroSense公司就后者拟用于肌萎缩侧索硬化(ALS)候选药物PrimeC达成合作协议。PrimeC是由环丙沙星和塞来昔布构成的创新组合配方,通过调节microRNA合成、减少神经炎症和调节铁积累来治疗ALS。根据协议,渤健将在Ⅱb期临床PARADIGM中,评估PrimeC对受试者血浆中神经丝(neurofilament)水平的影响。此外,渤健将资助神经丝生物标志物的研究并进行分析。
6.新型LNP公司完成种子轮融资。波士顿生物技术初创公司Hopewell宣布完成2500万美元的种子轮融资,本轮融资的投资方包括Mass Ave Capital、五源资本、山行资本、Forcefield Ventures(IMO Ventures)、BOPU Capital和WS Investments。本轮融资将用于搭建差异化器官靶向性脂质纳米微粒技术平台(ttLNP)、推进肺部疾病管线,以及开发突破心脑屏障的新一代脂质纳米微粒(LNP)。
医药热点
1.NABR认为食蟹猴不属于濒危物种。美国国家生物医学研究协会(NABR)联合知名独立科学家,于近日向国际自然保护联盟(IUCN)提交了一份请愿书,质疑该机构最近根据IUCN名录标准,将长尾猕猴(食蟹猴)认定为濒危物种。这一认定是由于数据使用不当,不支持将该物种列为濒危。美国国家生物医学研究协会呼吁立即进行审查。
2.国家医保局推出16项医保服务便民措施。日前,国家医保局印发了《国家医疗保障局办公室关于实施医保服务十六项便民措施的通知》,推出首批十六项医保服务便民措施,简化手续、精简材料、压缩时限、创新服务模式,为群众提供更便捷、更优质、更高效的医保服务。下一步,国家医保局将向各地征集医保便民服务典型做法和经验,以持续优化医保便民服务,有效提升医保公共服务能力。
3.世界首个合成人类胚胎引发伦理争议。据外媒6月15日消息,来自美国加州理工学院和英国剑桥大学的一个研究团队表示,他们首次从干细胞中创造出一种不含卵子和精子的合成人类胚胎样结构。这些结构相当于处在人类发育的最早阶段,没有跳动的心脏或大脑,但具有后来可以形成胎盘、卵黄囊和胚胎本身的细胞。研究人员表示,这一成果可能有助于推进对遗传病或流产原因的了解。但同时,这项研究引发了法律和伦理方面的争议,因为实验室培育的实体不在现行立法范围之内。
评审动态
1. CDE新药受理情况(06月20日)
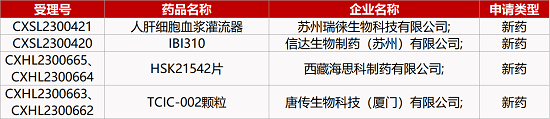
2. FDA新药获批情况(北美06月16日)