今日头条
海思科镇痛药报带疱神经痛NDA。海思科1类化药HSK16149胶囊(crisugabalin)的新适应症上市申请获CDE受理,用于带状疱疹后遗神经痛。HSK16149是一种电压门控钙离子通道类新型镇痛药,属于普瑞巴林的me-better药物,具备高靶点选择性、强效镇痛、长效镇痛、中枢副作用小等特点。去年10月,该新药用于糖尿病周围神经痛治疗的首个上市申请已获得CDE受理。
国内药讯
1.清华PLpro抑制剂获批新冠临床。清华大学与复旦大学合作的木瓜蛋白酶样蛋白酶(PLpro)小分子抑制剂HL-21获国家药监局临床许可。冠状病毒通过其主水解酶(Main Protease,简称Mpro或者3CLpro),RNA依赖的RNA聚合酶(RdRp)和PLpro等关键蛋白协同工作实现病毒复制。HL-21旨在通过PLpro BL2结构域以阻断PLpro对于底物的切割,有望为多种新冠病毒株细胞感染提供新的治疗选择。
2.诺诚健华BTK抑制剂见刊AJH。诺诚健华布鲁顿酪氨酸激酶(BTK)抑制剂奥布替尼在《美国血液学杂志》(American Journal Of Hematology)上发表用于治疗复发/难治性边缘区淋巴瘤(MZL)患者的临床研究结果。中位随访24.3个月时,独立审查委员会(IRC)评估的总缓解率(ORR)为58.9%,92.2%的患者观察到肿瘤缩小。12个月的PFS率和总生存(OS)率分别为82.8%和91.0%。药物的安全性良好。
3.宜明昂科CD24单抗临床前研究积极。宜明昂科CD24单抗IMM47临床前研究成果发表于《Antibody Therapeutics》上。IMM47能够阻断从CD24/Siglec-10通路传递至巨噬细胞、自然杀伤细胞(NK)和T细胞的免疫抑制信号。在临床前动物体内药效研究中,IMM47能够显著提高肿瘤组织中M1巨噬细胞的数量以及下调肿瘤细胞CD24表达,单药或者与PD-1/PD-L1免疫检查点抑制剂联用显示出强大的抗肿瘤疗效。
4.海森生物引进长效PCSK9抑制剂。海森生物与LIB Therapeutics就后者一款临床后期、拟开发用于高胆固醇血症的长效PCSK9抑制剂Lerodalcibep达成合作许可协议,获得该新药在大中华区(包括中国大陆和港澳台地区)开发及商业化独家专有权。根据协议,LIB Therapeutics将获得2000万美元的预付款,最高达3.05亿美元的临床、注册和销售里程碑后期付款,以及产品的销售分成。
5.英矽智能USPI抑制剂授权Exelixis。Exelixis公司与英矽智能达成独家授权协议,获得后者基于其人工智能生成平台Chemistry42开发的一款USP1抑制剂ISM3091,及其他USP1靶向化合物的全球独家开发和商业化权益。根据协议,英矽智能将获得8000万美元的预付款,开发、商业和销售的里程碑潜在付款,以及净销售额的分级版税。今年以来,ISM3091已先后在中美两国获批临床,拟开发治疗晚期实体瘤。
国际药讯
1.PDE3/4抑制剂吸入剂报慢阻肺NDA。FDA受理Verona公司吸入式磷酸二酯酶3/4(PDE3/4)抑制剂ensifentrine(恩塞芬汀)的新药申请(NDA),用于维持治疗慢性阻塞性肺病(COPD),PDUFA日期为明年6月26日。在两项国际III期临床(ENHANCE-1和ENHANCE-2)中,ensifentrine维持治疗使患者的平均1秒平均用力呼气量(FEV1)分别增加87mL和94mL,COPD恶化率分别降低36%和42%。优锐医药拥有ensifentrine的大中华区独家权利。
2.阿斯利康IL-5Rα单抗EGPA临床积极。阿斯利康IL-5Rα单抗benralizumab(本瑞利珠单抗)用于嗜酸性肉芽肿性多血管炎(EGPA)附加维持治疗的III期MANDARA研究达到主要终点。在接受伴或不伴免疫抑制剂的口服糖皮质激素(OCS)治疗基础上,benralizumab附加维持治疗在第36周和第48周达到缓解状态的患者比例的统计非劣效于美泊利珠单抗。详细结果将在医学会议上公布。
3.艾伯维IL-23抗体克罗恩病Ⅲ期临床成功。艾伯维IL-23抑制剂Skyrizi(risankizumab)治疗中重度活动性克罗恩病(CD)的Ⅲ期临床(SEQUENCE)达到双主要终点和所有次要终点。与活性对照组相比,Skyrizi治疗组第24周时临床缓解率的统计达到非劣效性(59%vs40%);第48周达到内窥镜评分[SES-CD]≤4和至少降低2分,且任何单个组分的分项评分均不超过1分的患者比例为32%(vs16%,p<0.0001)。临床中未观察到新的安全性风险。
4.CRF1拮抗剂治疗CAH的Ⅲ期临床积极。Neurocrine公司选择性促肾上腺皮质激素释放因子1型受体(CRF1)拮抗剂crinecerfont,在治疗经典先天性肾上腺皮质增生症(CAH)的Ⅲ期临床CAHtalyst达到主要终点和关键次要终点。在第24周,与安慰剂相比,该新药在维持雄激素控制的同时,还显著降低患者每日所需糖皮质激素剂量百分比;该组约63%的患者所使用的糖皮质激素降低至生理剂量,而安慰剂组这一数值约为18%(p<0.0001)。Crinecerfont总体耐受性良好。
5.慢性鼻窦炎创新疗法Ⅱ期临床积极。Lyra Therapeutics鼻基质创新药物LYR-220治疗慢性鼻窦炎(CRS)的Ⅱ期临床结果积极。LYR-220旨在向鼻窦通道连续递送六个月的抗炎药物糠酸莫米松以达到治疗目的。结果显示,与假性治疗组相比,LYR-220治疗组患者第24周时鼻塞、流鼻涕和面部疼痛/压力的综合改善具统计学意义(-1.50;p=0.02);鼻腔鼻窦结局测试22(SNOT-22)评分也显著改善(-16.8;p=0.007)。联拓生物拥有在大中华区开发和商业化LYR-220的优先权利。
6.百时美施贵宝LPA1拮抗剂Ⅱ期临床积极。百时美施贵宝口服溶血磷脂酸受体1(LPA1)拮抗剂BMS-986278治疗进行性肺纤维化(PPF)的Ⅱ期临床结果积极。与安慰剂组相比,BMS-986278(60mg)治疗组预测用力肺活量百分比(ppFVC)的变化率降低69%(治疗组与安慰剂组的差异为2.9%;95% CI:0.4,5.5),治疗组ppFVC的变化率相对于安慰剂组降低74%(3.2%;95% CI:0.7,5.6)。药物不良事件(AEs)发生率与安慰剂相似。
医药热点
1.重庆九价HPV疫苗接种已纳入补贴。9月8日,重庆沙坪坝区适龄女生HPV疫苗接种在歌乐山社区卫生服务中心正式启动,沙坪坝区本次疫苗接种面向全区无免疫史的初二在校女生。目前,重庆多个城区多个街道的社区卫生服务中心已启动适龄女生HPV疫苗接种,接种女孩和家长可自主选择接种二价、四价或九价疫苗,均按照最高每人600元的标准,以不超过疫苗总费用为限实施定额补助。
2.北京出台药品创新服务提质增效行动方案。近日,北京市药监局印发《药品创新服务提质增效行动方案(2023-2025年)》。《方案》明确,到2023年底,全面落实项目制管理工作机制,本市在研品种纳入项目制管理品种数量不少于100项;启动在线咨询、重点项目跟踪服务管理模块等信息化建设;到2024年底,累计纳入项目制管理品种数量不少于200项;完成在线咨询、重点项目跟踪服务管理模块等信息化建设并上线运行;到2025年底,累计纳入项目制管理品种数量不少于300项;三年内获批药物临床试验创新药项目不少于200项。
3.王大军任首都医科大学附属复兴医院党委书记。9月12日,首都医科大学附属复兴医院召开干部大会,宣布复兴医院领导干部任免决定:王大军同志任首都医科大学附属复兴医院党委书记,刘云军同志不再担任首都医科大学附属复兴医院党委书记职务。首都医科大学附属复兴医院始建于1950年,前身为公安部直属医院,1958年归属地方管理,并与国家计委三里河门诊部合并后更名为北京市复兴医院,1998年被首都医科大学认定为附属医院。
评审动态
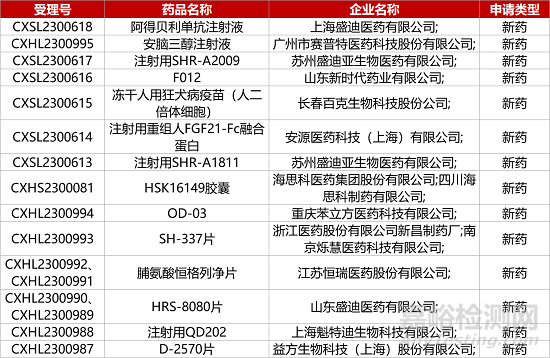
1. CDE新药受理情况(09月13日)
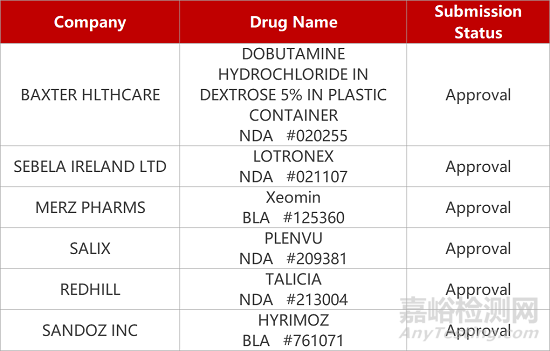
2. FDA新药获批情况(北美09月11日)