您当前的位置:检测资讯 > 生产品管
嘉峪检测网 2024-07-28 12:23
摘要 目的:药品上市许可持有人制度实施后,仅委托生产的持有人数量不断增加,带来潜在的风险隐患。本研究旨在对仅委托生产的药品上市许可持有人完善质量管理体系和监管部门制定举措提供参考。方法:以江苏省内企业为研究对象,开展仅委托生产的药品上市许可持有人质量管理现状调查,发现其质量管理方面存在的问题,分析原因并提出建议。结果:仅委托生产的药品上市许可持有人基础相对薄弱,质量管理存在质量安全主体责任落实不到位、质量和风险管控能力不足等问题,其原因主要为质量意识薄弱、合作匹配不易、主体地位弱势、体系衔接困难等。结论:仅委托生产的药品上市许可持有人应积极履行质量安全主体责任,药品监管部门可以采取创新监管方式、强化行政指导等措施,不断完善质量管理体系,优化监管举措,保障药品质量和用药安全。
药品上市许可持有人(Marketing Authorization Holder,MAH)制度(以下简称持有人制度)对于鼓励药品创新、提升药品质量、促进行业发展、优化资源配置、落实药品全生命周期主体责任、推进科学监管具有重要意义[1]。不具备自行生产药品能力,仅委托生产药品且其药品生产许可证分类码仅为B的药品上市许可持有人,本文简称为纯B证持有人。截至2023年12月底,全国纯B证持有人已经超过了1000家(药品生产许可证占比已接近总数的13%)且仍在快速增长。然而,其质量安全主体责任落实不到位、质量和风险管控能力不足等一系列问题亟待解决,质量安全风险也随之凸显[2]。
截至2023年12月底,江苏省药品生产许可证持证企业数、仿制药质量和疗效一致性评价获批数、药品新获批数、创新药获批数全国占比分别为7.68%、14.56%、17.56%、26.58%,均居全国前列。本研究以江苏省份为例具有一定的样本基础和代表性,通过对江苏省内纯B证持有人委托生产开展现状调研,发现其质量管理存在的问题,分析原因,结合委托生产新法规要求提出针对性意见建议,为持有人不断完善质量管理和监管部门制定监管对策提供参考。
1、 委托生产质量管理法规新要求
自《中华人民共和国药品管理法》(以下简称《药品管理法》)从法律层面正式确定了我国持有人制度后,一系列质量管理的配套法规随后颁布,使MAH从研发、生产、流通到使用的全生命周期活动得到了有效的法规保障和约束。法律、法规、规章、规范性文件的法律效力依次递减但都具有强制性约束力,部分公告、指南、行政指导性文件虽然是非强制性的,但仍会对药品监管部门与持有人带来实际的约束力[3]。
2023年以来,国家药品监督管理局先后发布、实施了《药品上市许可持有人落实质量安全主体责任监督管理规定》[4](以下简称《规定》)、《关于加强药品上市许可持有人委托生产监督管理工作的公告》[5](以下简称《公告》)、《药品上市许可持有人委托生产现场检查指南》[6](以下简称《指南》),对持有人的质量管理进行了进一步的规范和约束。《规定》《公告》《指南》(以下简称新法规)在审批许可、持有人质量管理、监督管理等方面对委托双方提出了近百条细化要求,涵盖了持有人的“准入”“质量管理”和“退出”全过程,还特别对特殊品种、特定情形的风险管理等进行了规范,提出了非常严格甚至部分是“劝退式”的要求,目的就是最大限度地减少药品质量安全风险隐患。新法规实施之后,纯B证持有人快速增长的势头明显缓和。纯B证持有人新法规的执行情况如何,质量管理的现状如何,持有人制度如何更好地落实,纯B证持有人如何才能更好地生存与发展,监管部门如何实施高效监管,本研究针对上述问题开展了专题调研。
2、 委托生产质量管理现状调研
调研以江苏省内纯B证持有人为研究对象,采取问卷调查、专项检查的方式开展。问卷调查旨在考察纯B证持有人质量管理现状和存在的问题,专项检查旨在考察纯B证持有人质量管理体系运行情况及委托生产质量管理新法规的执行情况。
2.1 问卷调查概况
2.1.1 问卷对象和内容
为便于对比,问卷对象涵盖了所有类型的委托生产持有人(包括有药品自行生产能力的持有人和纯B证持有人)。问卷内容分为客观问题和主观问题,主要涵盖三方面内容:一是行业背景及品种等情况,包括企业前身、研发及持有药品批准文号情况,是否有自建生产线计划,年度质量管理费用投入等;二是质量管理基本情况,包括是否按照GB/T19001-2016(ISO9001-2015)建立质量管理体系、委托生产质量管理人员数、委托生产质量协议制定、驻厂管理、委托检验、责任赔偿能力等;三是委托生产质量管理相关困难和建议。
2.1.2 问卷结果
截至2023年11月10日,江苏省共有委托生产持有人(按药品生产企业许可证分类码含B数量计,以下简称B证持有人)199家,其中纯B证持有人101家。调研共发出问卷199份,收回195份(回收纯B证持有人问卷101份),本文将纯B证持有人的问卷结果进行统计分析。
(1)行业背景和品种等情况:行业背景方
面,在取得B证前75家(在纯B证持有人回收问卷中占比74.2%,下同)为研发企业,9家(8.9%)为生产企业,6家(5.9%)为经营企业,11家(10.8%)为医疗器械等其他类型企业;品种持有方面,101家纯B证持有人共获药品批准文号240个,在研品种649个,其中无文号企业58家(57.4%),无在研品种企业16家(15.8%),无批准文号且无在研品种企业8家(7.9%,因获批品种转让等原因);生产能力方面,5年内有自建生产线计划的企业有24家(23.7%);当前有品种在产企业20家(19.8%);跨省委托方面,20家在产企业有11家(55%)存在跨省委托;经费投入方面,20家在产企业质量管理年均投入费用在300万元以上的有15家(75%),500万元以上的有11家(55%),1000万元以上的有7家(35%)。
(2)质量管理基本情况:体系建立方面,按通用标准建立本企业质量管理体系的企业有73家(72.7%),按药品生产质量管理规范(Good Manufacturing Practice,GMP)建立质量管理体系的企业有27家(26.7%);人员方面,从事质量管理的人员数量在10人及以上的有50家(49.5%),其中在产企业质量管理人员数10人以上的为15家(75%);协议签订方面,在产纯B证持有人全部参照《药品委托生产质量协议指南(2020年版)》内容与受托生产企业签订了质量协议;驻厂管理方面,20家在产纯B证持有人有18家(90%)在委托生产期间派驻人员进厂,平均派驻人员数2.4人;委托检验方面,有检验能力的纯B证持有人有63家(62.3%),其中在产纯B证持有人有检验能力的有16家(80%);责任赔偿方面,常见的为公司自有资产赔偿、担保、保险3种模式,101家纯B证持有人购买产品保险的为22家(21.7%),其中在产纯B证持有人购买保险的为14家(70%),其他责任赔偿方式为6家(30%)。
(3)MAH提出的委托生产质量管理的困难和建议:委托检验的报告方式不明确、缺少了解受托生产企业信息的渠道、无法约束受托方或沟通不畅(质量管理体系不同、涉密等)、全过程监督受托方困难、希望监管部门加大对持有人委托生产质量管理的培训力度、不对驻厂人员做硬性要求等。
2.1.3 问卷小结
江苏省内纯B证持有人约占其B证持有人的一半,三分之二的纯B证持有人具有研发和生产的背景基础,平均每家有药品批准文号2个、在研品种6个,研发势头活跃;纯B证持有人质量管理体系建立与运行不规范,部分纯B证持有人质量管理人员不足或有经验的质量管理人员流动性大;纯B证持有人质量协议均按法定要求进行签订但大部分套用模板,并未全面细化和完善具体条款;在产期间大部分企业实行了驻厂管理但驻厂人员素质参差不齐,全过程监督的方式不一;虽然80%纯B证持有人具备一定的检验能力但大都不具备委托生产制剂出厂放行全项目检验能力,委托受托生产企业进行出厂放行检验较为普遍;除了在产的纯B证持有人,大部分企业都倾向于在品种获批后、生产前强化其药品责任赔偿能力。
2.2 专项检查概况
选择江苏省内委托生产运行时长一年以上、有品种在产的14家药品上市许可持有人(含9家纯B证持有人、3家具备自行生产能力的B证持有人和2家跨省受托生产企业)为对象开展专项检查。
2.2.1 检查依据和检查结论
检查依据为持有人制度在质量管理方面涉及的既往法规及新发布的《指南》,14家企业的检查结论均为符合或待整改后评定(涉及《指南》的检查缺陷项均需转化为GMP相关条款)。
2.2.2 检查缺陷情况
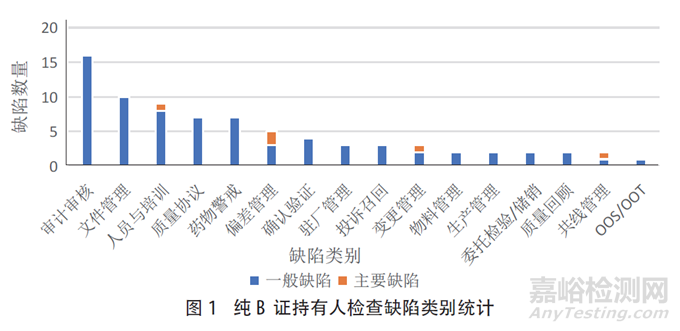
对9家纯B证持有人的现场检查共发现缺陷项78条(无严重缺陷,其中主要缺陷5条,一般缺陷73条,检查缺陷类别统计详见图1)。按照人员培训、审计审核、文件管理、委托检验/储销、驻厂管理等16个细分类别对纯B证持有人的检查缺陷进行分类统计,缺陷排序前三的分别为审计审核16条(21%,条款对应《指南》第三部分持有人对受托生产的管理)、人员与培训9条(12%,条款对应《指南》第一部分机构与人员)、文件管理和质量协议17条(22%,条款对应《指南》第二部分质量管理体系)。
(1)审计审核典型缺陷:持有人未结合无菌
产品特点评估受托方的无菌保障能力;4次受托方审计缺陷全部为0,2次审计报告内容高度重叠;持有人未对受托方检验能力进行充分评估就实施了委托检验,受托方未得到持有人授权而实施检验取样;不同供应商、不同委托方的同种物料放置同一区域甚至采用同一代码;委托方虽然审核了委托生产药品出厂放行审核单、批记录等,但是批记录未包含环境监测记录、设备清洁记录等无菌相关记录;对受托方的生产监督记录均采用打勾形式、仅对少数固定项目进行评估,对委托生产全过程监督不充分、不全面;批记录未记录偏差等异常情况等。
(2)文件管理典型缺陷:文件未及时更新(例如合格供应商目录、变更后的工艺文件等);委托销售和储存规程未明确相关责任或内容前后矛盾;委托检验合同未明确受托方有义务接受药品监督管理部门检查;文件中规定由持有人开展的活动实际由受托方实施等。
(3)人员与培训典型缺陷:岗位人员配备与产品规模不相适应;部分人员岗位职责不清、职能相互交叉;产品为无菌但培训档案里缺少无菌生产专题培训;文件拟定部门人员未参加相关培训;财务人员未参加事故责任赔偿程序培训;多数培训采用自学,未开展培训效果评估等。
(4)质量协议典型缺陷:照搬照抄模板内容而与实际情况不符;未明确物料采购等工作的责任方;未明确工艺再验证周期参照委托双方哪方标准执行;未明确委托生产沟通交流的内容和形式,执行过程中遇到质量问题仅靠口头告知;委托生产日期确定方法不一致,一方以配制日期为准,另一方以灌装日期为准,双方未进行有效衔接商定等。
2.2.3 专项检查问题情况
从检查缺陷分布看,纯B证持有人质量管理存在的主要问题:质量管理手册和程序文件制定不系统、不全面,内容不够个性化、具体化;体系建立与运行“两层皮”;质量协议未认真制定或履行;审计审核流于形式;质量管理人员配备数量不足或不能胜任岗位要求;变更偏差研究评估不充分、共线评估不充分、药物警戒开展不到位;责任赔偿能力不足;委托检验、委托销售、委托储运未按规程进行管理等。由于新法规实施时日尚短,与GMP等既往法规相比,新法规增加了不少委托生产质量管理方面的新要求(详见表1),纯B证持有人在贯彻执行新法规方面尚有较大差距。


3、 质量管理问题原因分析
持有人制度在我国正式实施不足5年,纯B证持有人如何有效履行质量安全主体责任尚是个新课题。本次问卷和检查的结论表明,纯B证持有人质量管理体系建立还不完善,新法规执行还不到位,企业与监管部门均处于边摸索边规范状态,分析其深层次原因,主要可以概括为以下几点。
3.1 质量管理的能力和意识薄弱
纯B证持有人普遍为小微企业,年均质量管理投入少,质量管理关键岗位难以招聘到经验丰富的优质从业者且难保持质量管理队伍的稳定。质量管理团队人员数量、质量双双薄弱,企业很难量体裁衣、真正依据委托生产需要和法律法规要求健全质量管理体系并有效运行。高层管理人员比较关注的仍是生存指标,例如品种研发进展、能否尽快获得注册批件、集采能否中标入选等,在履行质量安全主体责任上普遍存在“不会履行、不愿履行、履行不好”的问题。企业普遍对内、外部审核审计,变更偏差,药物警戒等质量管理概念不强[7],这与调研中发现的问题高度一致。
3.2 良好的合作方匹配困难
目前江苏省101家纯B证持有人中仅20家有品种在产,多数企业的品种处于在研或申报阶段。因为产能、共线、商业利润等因素,不少纯B证持有人很难在本省匹配到质量管理、产能等各方面良好的受托方,不得不跨省委托生产,甚至将品种委托至监管和质量管理均薄弱的省份生产。随着监管趋严,企业既担心因共线、质量管理等原因通不过现场检查,又苦于已签约合作投入巨大无法变更,进退两难。不少企业表示,现有的委托合同只能继续执行,待品种获批后,才能以新增生产场地的名义再寻找更好的合作企业。委托生产质量管理是合作的产物,没有找到受托方很难先行全面完善委托生产质量管理。从调研结果也不难看出,在产纯B证持有人相对非在产企业而言,其质量管理体系更加完善。
3.3 委托方质量管理主体地位弱势
江苏省药品主要委托给了药品生产许可证分类码同时含“AC”的企业生产,分类码仅为C的企业较少。具备自行生产能力,同时也是持有人的受托生产企业和受业内亲睐的合同加工外包(Contract Manufacture Organization,CMO)企业,其质量管理、生产管理甚至研发经验通常都强于纯B证持有人,从委托双方的话语权来看,纯B证持有人虽然是甲方,却是弱势方。由于药品质量安全的法定责任者是持有人,受托生产企业更容易把质量管理问题、生产检验过程异常情况处置等推给持有人,实践中发现个别受托生产企业对自产与受托的同一品规质量管理实行“区别对待”。
3.4 委托双方质量管理衔接困难
纯B证持有人与受托生产企业两者的管理重点不同,加上企业文化不同、质量管理风格不同、诉求不同,同样的风险与偏差,处置的方式、方法、标准各异,双方极易产生误解与分歧。此外,研发型持有人比较看重知识产权保护以及对委托药品生产的“把控力”[8],而受托方也担心自身的商业秘密被泄露,担心委托方审计多、要求多、驻厂干扰等。目前委托双方质量管理衔接普遍存在困难。
4、 意见和建议
4.1 纯B证持有人积极履行质量安全主体责任
4.1.1 全面增强质量管理的意识与能力
建议企业管理高层全面重视质量管理。从启动药品研发之日起,就按药品生产相关法律法规严格要求,注重全员培养和提升质量管理的意识和能力[9]。特别在组织机构上做出相应的改革,不断充实人力资源,加大人员培训力度,质量管理部门应当独立设置并配备足够的资源等[10]。企业负责人定期听取质量管理情况并推进解决相关问题。在合作方选择上,建议省内委托、“向上”委托、集团内委托,优秀的合作方更能保障产品质量和知识产权。具体可以结合双方企业质量管理体系、产线与产能、合作配合度和成本等因素综合考虑,建议参考部分省份(山东、北京)出台的受托生产企业遴选指南和检查指南。
4.1.2 建立有效沟通衔接机制
建议委托双方建立长效沟通机制并注重形成沟通记录,解决各类问题。如委托方对沟通的方式和频次等进行约定和规范,解决信息传递失真、沟通不畅的问题[11]。双方结合各自质量管理体系、品种情况、合作流程等情形对约定内容进行细化,将达成共识的内容列入质量协议,尽量涵盖双方所有的质量管理活动并明确界定双方的责任和义务[12]。
4.1.3 强化全过程监督
持有人对委托生产全过程的监督并不是盯紧生产过程的每一步,而是统筹全程,把握关键,及时准确地获知生产过程中的异常情况,以批次为单位审核相关记录,对可能出现的偏差、OOS/OOT等做到心中有数,确保持续稳定地生产出符合要求的产品。除了法规要求驻厂的情形以外,建议有条件的企业在排产期间安排有生产和质量管理经验的人员驻厂。对于集团内的委托生产,受托方还可开放生产检验等信息管理系统权限给持有人实施全过程监督。药品上市放行前,所有的异常情况要得到关注,所有的偏差等均应得到有效处置。
4.1.4 完善责任赔偿机制
法规要求持有人具备责任赔偿能力,但并未限定其方法。本次调研的9家在产纯B证持有人,其中5家购买了保险、2家由母公司或股东为其担保、2家自述以公司自有资产作为赔偿基金。由于公司资本(资产)只能反映某一时间节点的资产状况,难以保证将来损害发生时持续具有责任承担能力,担保在制药行业内的应用场景和应用经验也有限,相比之下,保险模式更加成熟,在药品领域运用也更为广泛[13]。建议纯B证持有人优先考虑购买保险。暂无产品获批、生产或上市的纯B证持有人,因产品市场规模无法确定等客观因素,也存在暂未参保的现象,但法规并未对此类持有人进行责任豁免。实践中,不同检查员对其评判标准也不统一。无论如何,企业应当具备与其市场规模相匹配的赔偿能力。
4.1.5 善用自检(内审)和管理评审
纯B证持有人普遍持证时间短,药品质量管理底子薄弱,若建立了自我完善机制,便可持续改进、不断进步。建议质量管理团队持续保持合规的敏锐性,系统策划并认真开展自检(内审)与产品服务供应商外审,积极参与监管部门发起的主体责任自查自纠,举一反三,不断完善质量管理体系。建议企业负责人亲自主持年度管理评审,对其质量管理体系的适宜性、充分性、有效性进行评估,统筹企业发展战略和目标,调动可以调动的一切资源持续改进。
4.2 受托生产企业认真履约并关注受托风险
药品质量源于设计,也源于生产全过程控制[14],纯B证持有人固然是质量安全责任主体,但产品质量风险归根结底是通过受托生产显现的。受托生产企业应当严格履行协议约定的义务,特别是配合持有人做好质量管理体系的衔接,有序、规范地安排生产。此外,建议受托生产企业特别关注受托行为带来的新风险,例如产能超限、质量管理能力瓶颈、物料记录混淆、品种共线污染等,认真评估受托风险,统筹企业各方面能力,谨慎签定受托生产协议,特别是在研品种的受托生产,以免带来合规风险。
4.3 药品监督管理部门履行监管和服务职责
4.3.1 创新监管方式
通过创新监管方式来提升监管效能,例如开展持有人示范建设,引领好的更优、差的变好,实现“良币驱逐劣币”的良好氛围;试点质量风险第三方评估,从不同视角提高监管部门的风险识别能力;建立委托生产“一企一档”和质量安全信用风险评估机制,探索分级分类监管,依风险实施精准监管;合并不同类别的检查,实施二合一、三合一,减少对持有人和受托企业的干扰;制定委托检验、委托储存、委托销售等报告程序,开发信息化报告系统,方便持有人及时报告,等等。
4.3.2 强化行政指导
建议监管部门不能只关注检查、抽验、督导等风险排查的硬手段,更要用好一揽子助企纾困的软措施,尤其是在新法规实施前期,纯B证持有人常常只能理解“字面意思”。建议不定期开展新法规宣贯、质量管理培训、企业“面对面”沟通交流等,帮助纯B证持有人平稳有序实施新法规。此外,对于受托方信息了解渠道有限等问题,建议监管部门(或行业协会)搭建相应的平台,加强委托受托信息共享,例如海南省定期统计并向持有人推送受托生产厂家信息,内容涵盖剂型(细化到药理学分类)、产线认证情况(欧盟、美国、西班牙等)、代加工年限、最大产量等关键信息,值得各省监管部门借鉴。
4.3.3 提升监管人员监管与服务产业能力
持有人数量陡增,监管压力巨大。药品监督管理部门机构改革后,抽调检查员困难,建议持续健全职业化、专业化检查员管理机制,增加人员编制,完善激励机制。此外,法律法规陆续频繁出台、技术规范不断细化,分段生产、连续制造等前沿技术日新月异,建议不断完善内部培训机制,加大实训的占比,不断提升监管人员的风险排查能力和服务发展能力。
4.3.4 加强跨省协同监管
跨省委托风险叠加,目前国家市场监督管理总局、国家药品监督管理局出台了《关于加强跨区域跨层级药品监管协同的指导意见》,但是统一的跨省委托生产监管机制及其信息共享平台尚在建设中,跨省监管仍靠双边协商,监管信息基本依靠互相发函推送,存在滞后性,严重影响了药品异地监管的效能,存在一定的风险[15]。为此,建议尽快建立协同监管机制,依托国家一体化智慧监管平台,探索打通跨省药品监管数据共享渠道,以点带面、以面带全,先行实现监管信息区域共享,例如以长三角区域一体化发展战略为基础,实现检查结果互认、企业档案互联、监管信息共享等。
参考文献
[1] 颜若曦,曹轶,俞佳宁,等. 对药品上市许可持有人检查工作的调研分析[J]. 中国药物评价,2022,39(1):83-86.
[2] 张磊,朱夜琳,张海龙. 当前我国仅委托生产的药品上市许可持有人存在问题及对策分析[J]. 中国食品药品监管, 2023(11):92-97.
[3] 王波,邵蓉. 国家药监局技术指导原则的法律属性分析[J]. 中国食品药品监管,2022(6):10-17.
[4] 国家药品监督管理局. 药品上市许可持有人落实药品质量安全主体责任监督管理规定[EB/OL].(2022-12-29)[2024-01-20]. https://www.nmpa.gov.cn/xxgk/fgwj/xzhgfxwj/20221229195805180.html.
[5] 国家药品监督管理局. 国家药监局关于加强药品上市许可持有人委托生产监督管理工作的公告(2023年第132号)[EB/OL].(2023-10-23)[2024-01-20]. https://www.nmpa.gov.cn/xxgk/fgwj/xzhgfxwj/20231023160426145.html.
[6] 国家药品监督管理局. 国家药监局综合司关于印发药品上市许可持有人委托生产现场检查指南的通知[EB/OL].(2023-10-24)[2024-01-20]. https://www.nmpa.gov.cn/xxgk/fgwj/gzwj/gzwjyp/20231024161543188.html.
[7] 张书卉. B类药品生产许可证核发检查常见问题分析[J].上海医药,2022,43(3):63-66.
[8] 汤涵,王敏娇,王文,等. 药品研发企业开展MAH委托生产的影响因素研究[J]. 中国医药工业杂志,2020,51(10):1329-1333.
[9] 姚炜凯,陈航,吴声杨,等. 福建省药品上市许可持有人委托生产检查现状分析[J]. 中国药业,2024,33(2):15-19.
[10] 任晓辰,陈先红. 科研院所成为上市许可持有人的挑战与机制探索[J]. 中国医药工业杂志,2020,51(9):1213-1216.
[11] 招伟汉,江映珠,谢正福,等. 药品上市许可持有人申报药品生产许可证(B证)检查发现主要问题分析及建议[J]. 广东化工,2021,48(15):98-99.
[12] 张然,陶群山,罗京京. 安徽省药品上市许可持有人质量管理体系调研分析[J]. 中国医药导刊,2023,25(12):1213-1218.
[13] 邵蓉,曹丽君,谢金平. 药品上市许可持有人责任承担能力的模式辨析[J]. 中国食品药品监管,2022(4):12-19.
[14] 孙京林,余伯阳. 药品上市许可持有人制度下的质量管理体系[J]. 中国药学杂志,2020,55(23):1919-1922.
[15] 徐大丽,章文霞. 上市许可持有人制度实施以来我国药品监管现状探究[J]. 中国药事,2023,37(8):857-863.

来源:中国药事


