您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2018-07-09 08:25
人类和癌症的抗争持续了上千年,我们对癌症的认知从一个简单的肿块到如今懂得利用免疫系统与之抗击。从公元前2625年到2018年,在4000多年的历史长河中,我们对于癌症的认知正在不断革新。而癌症在人体内所处的环境——肿瘤微环境,也逐渐成为我们研究和攻克癌症的重要方向。
癌症“地心说”的坍塌
在哥白尼提出“日心说”之前,人们一直认为地球是万物的中心,宇宙均以地球为中心,也就是我们所说的“地心说”。同样的,对于癌症,人们起初也有着癌症“地心说”的想法——癌症转移是以癌症为中心,在人体内向四周扩散。人们对此深信不疑,然而事实真的如此吗?
1863年,Rudolph Virchow发现在实体肿瘤所处的部分都会产生免疫细胞的聚集,这是人们观察到肿瘤和人体间相互关系的最早研究。
“种子与土壤”假说
此后1889年,Stephen Paget通过分析735个乳腺癌病例,证实了癌症转移灶不是随机的,癌症之所以能转移是因为某些特定器官可以提供适合特定转移灶生长的环境。这就是癌症转移的著名的“种子与土壤”假说。
有个成语为“南橘北枳”,《晏子春秋》中曾写道:橘生淮南则为橘 生于淮北则为枳。在南方种植橘树,结出来的是又大又甜的橘子,但是如果移植到北方,就会长出又小又涩的枳。都说一方水土养一方人,不同的环境会早就不同的结果。而肿瘤的转移也是如此,相对于人体内的其他细胞而言,癌细胞生长同样需要适应的环境。
而癌细胞的扩散就像随风飘扬的蒲公英,飘到哪,种子就到哪。癌细胞的种子随着血管在人体内四处游走,移动到肝脏的时候,发现很适合自己生长发展,于是便在这里扎下根来;游走到肾的时候,发现不适合自己定居,就逐渐枯萎消亡,癌症也就无法转移到这里。
“种子和土壤”学说显示出了癌症与人体间会的联系与沟通,而更早期的癌症转移以癌症为中心的学说显然已经无法解释癌症发生发展的机制,于是越来越多的人开始将目光投向癌症与人体微环境之间的联系——肿瘤微环境(Tumour MicroEnvironment ,TME )。
肿瘤微环境(TME)的诞生
20世纪80年代以前,对TI作用机制的研究相当少,大多数都只是描述现象。难得有一些相关的研究发现也是作为研究的“附带现象”,并没有引起人们的关注。然而到了20世纪80年代,人们对TME的认知得到了颠覆性的改变,当时的研究报道发现原来TME会和癌细胞狼狈为奸,通过信号传导,重新编码癌细胞的表型,与癌细胞的生长和增殖有着密不可分的联系。
但说起TME真正的理念体系建立,还是在上世纪50年代初到80年代中期。这些具有突破性的结果阐明了癌症和TME之间信号传导的通用机制——与“经典”原癌基因或肿瘤抑制基因相比,癌症细胞基因同样收到受TME来源的信号所调控,对于癌症进展方面同样有着非比寻常的重要性,而这也促使了人们开展对TME的研究。
那么什么是肿瘤微环境呢?近些年来的研究为我们详细的描绘了其构成:
TME是由肿瘤细胞、常驻和招募的宿主细胞(分别与癌症相关的成纤维细胞和免疫细胞)、以及上述细胞的分泌产物(如细胞因子和趋化因子)和细胞外基质(ECM)中的非细胞成分组成。同时也可能存在TME的代谢产物,如源自肿瘤和非瘤细胞的过氧化氢,和特定的环境,比如缺氧、低pH值或间质压增加。如果把肿瘤比喻为一栋楼,那这栋楼所处的小区以及邻居就是肿瘤微环境)。
近墨者黑的TME
我们也可以将TME看成是一个肿瘤交易场所。在这里,肿瘤细胞扮演着恶徒的角色,不断的通过微环境来胁迫他人,获得自己发展所需的资源。原本微环境其实是遏制肿瘤细胞生长保护正常细胞存活的地方,但是随着肿瘤的生长发展,正常的环境被肿瘤细胞不断的破坏,环境开始被慢慢的改造成适合肿瘤细胞所生活的场所,而正常细胞就逐渐被驱逐出来。
正如上文说到的,研究人员也发现早期的肿瘤微环境往往是遏制肿瘤发展的,但是肿瘤通过微环境的相互作用包括征用或劫持生理信号通路等多种机制,或正向或负向调节肿瘤的生存、增殖和进展,到了后来,晚期肿瘤的微环境则具有促恶性作用的。
同时,当肿瘤细胞要侵入到一个新的组织和器官的时候,需要和该器官的微环境进行“谈判”,有的微环境容易被说服,肿瘤就会轻而易举的扩散到该器官上,但是有的微环境不听癌细胞的花言巧语就直接开打,癌细胞就被消灭无法形成转移。
风起于青萍之末,当我们回顾肿瘤微环境的一路发展,会发现有如此多的名字被镌刻在了历史的功劳簿上:
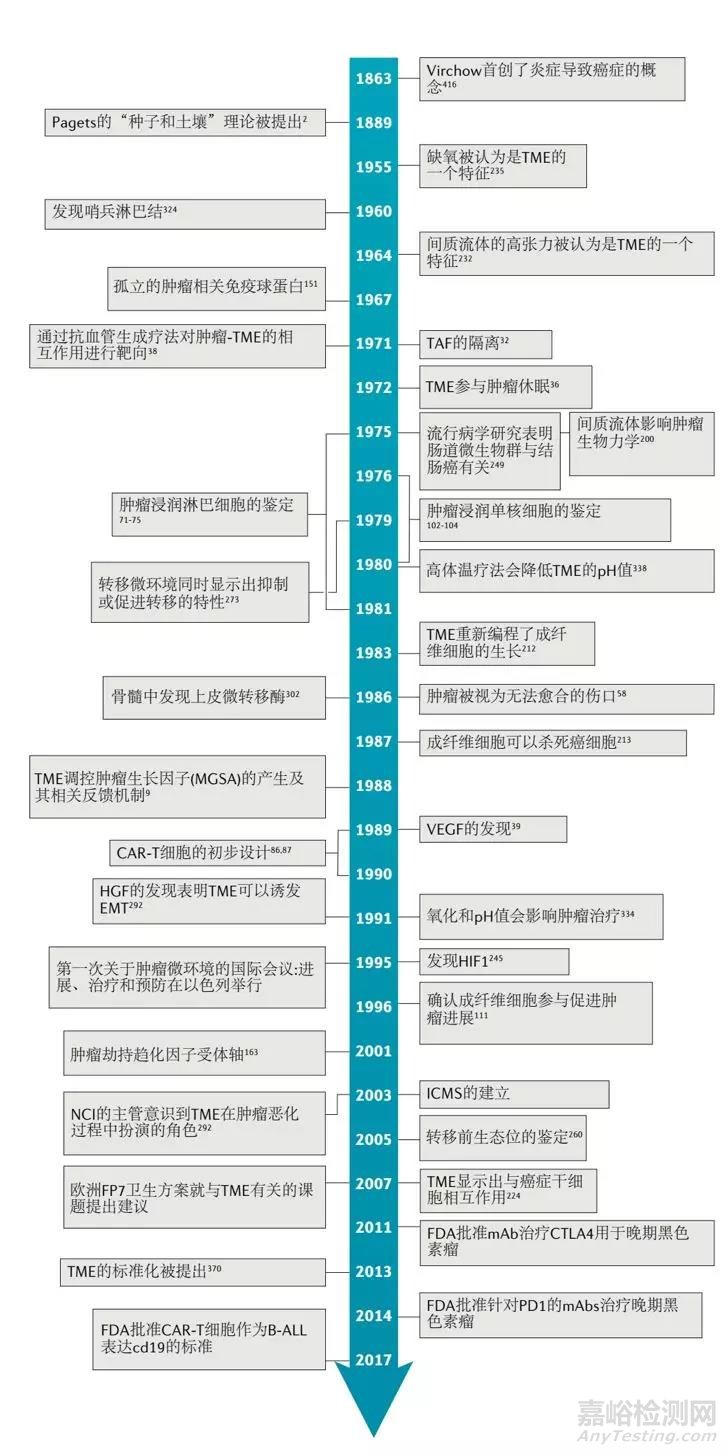
图1. |肿瘤微环境研究的年表。这张年表能显示出与肿瘤微环境研究相关的关键概念和发现。
B-ALL:B细胞急性淋巴细胞白血病; CAR:嵌合抗原受体; CTLA4:细胞毒性T细胞淋巴细胞抗原4; EMT:上皮间充质转变; FDA:美国食品和药物管理局; HGF:肝细胞生长因子; HIF1:低氧诱导因子1; ICMS:国际癌症微环境协会;mAb:单克隆抗体; MGSA:黑色素瘤生长刺激作用(也称为CXCL1); NCI:国家癌症研究所; PD1:程序化细胞死亡蛋白1; TAF:肿瘤致瘤因子; VEGF:血管内皮生长因子。
而在现代研究中,对TME的研究被拓展成了2个分支,一个是肿瘤发生发展和转移过程中必须要建立的运粮通道血管,另一个便是需要对抗人体的免疫环境。着这两个分支成了研究现代TME的重要方向,也在不断地加深人们对于癌症的认知。下面我们就先从在贯穿癌症发展始终的血管生成讲起。
兵马未动,粮草先行——要想富,先修路
在上世纪80年代,中国农村的墙面上大都刷上了白底红字的宣传标语,在着这其中就有一个传播度很广的标语:要想富,先修路。
而对于癌细胞而言,这句话同样适用,不过就变成了“肿瘤要生长,修路要优先”。人体内有着远比京杭大运河还要厉害无数倍的运输道路——血管。我们身体所需要的各种养分都需要通过血管来运输。相对于正常细胞而言,癌细胞对于营养物质的需求更高,细胞分裂需要更多的养分,转移入侵也需要养分,那怎么办呢?修路(血管生成)。
人体内的血管网四通八达,但是癌细胞不是我们正常的细胞,发生转移的时候也不可能每次都刚刚好有大血管在旁边供应养分,那怎么办呢?只能自己动手修路了。通过现代的显像手段,我们可以看到大肿瘤必然有强大的血供,癌细胞通过影响微环境建立了可以为自己单独供给养分的通道。
而这个发现,早在1940年就已经被确认。在随后的1971年,癌症相关血管生成研究的先驱之一Judah Folkman也强调:在肿瘤发生发展的阶段中,血管的生成都有着至关重要的作用。
那么癌细胞是如何为自己修路的呢?
在70年代中期,随着鉴别和分离出如血管抑素等固有血管生成抑制因子,研究人员提出:肿瘤如果要生成血管,就会分泌一些诱导血管生成因子,当人体内的抑制血管生子生成的因子分泌不足时,新的血管就会建立起来。
VEGF:抗血管生成治疗癌症
血管生成在肿瘤发生和进展中的重要性在20世纪70年代末到80年代初的一系列研究中得到了证明。研究显示:肿瘤的存在诱导了血管生成,肿瘤的生长受周围血管所控制,抑制血管生成可引起肿瘤的休眠,新血管的生存促进了肿瘤的生长。这些数据最终构成了Folkman在1971年提出抗血管生成疗法治疗癌症的雏形。也成就了后来的抗血管生成药物的诞生。
而到了1989年,Ferrara的小组率先观察发现了血管内皮生长因子VEGF。
VEGF除了直接的促血管生成功能外,VEGF还通过招募具有支持血管生成并分泌VEGF的肿瘤相关巨噬细胞(TAMs) 到TME中来间接刺激血管生成。就相当于一个包工头网罗了一帮小弟开工来修路,帮助肿瘤成长。
这么明显的一个帮手,医学研究人员自然不会放过。因此,VEGF成为了抗血管生成治疗癌症的一个有吸引力的靶点。通过阻断VEGF来抑制血管生成和肿瘤生长很快得到了实验模型和临床数据的证实。与此同时,FDA也批准了靶向VEGF或其受体的药物。
但随后出现了一个很重要的问题:肿瘤患者接受VEGF治疗之后很快出现了耐药性,于是人们的精力开始落到如何克服肿瘤患者的耐药。
2011年,Harris的团队发现Delta样配体4 (DLL4)-Notch信号通路通过不依赖VEGF信号的诱导血管形成,介导肿瘤抵抗VEGF治疗。靶向这一信号通路治疗可以增强抗VEGF治疗的反应。在20世纪90年代中期发现的用免疫球蛋白靶向的血管生成素2 (ANGPT2)配体-酪氨酸激酶和EGF同源结构域2(TIE2,也称为TEK)受体系统构成了第二代血管生成抑制剂。抑制ANGPT2减少招募刺激血管生成的TAM。这能进一步大大减少血管生成,目前靶向ANGPT2-TIE2系统的临床试验也正在进行中。
此外,研究人员还发现了一种称为血管征用的非血管生成的肿瘤生长形式,通过这种方式,肿瘤细胞可以利用已有的血管来帮助自己生长,这可能是某些肿瘤克服血管生成抑制的机制。
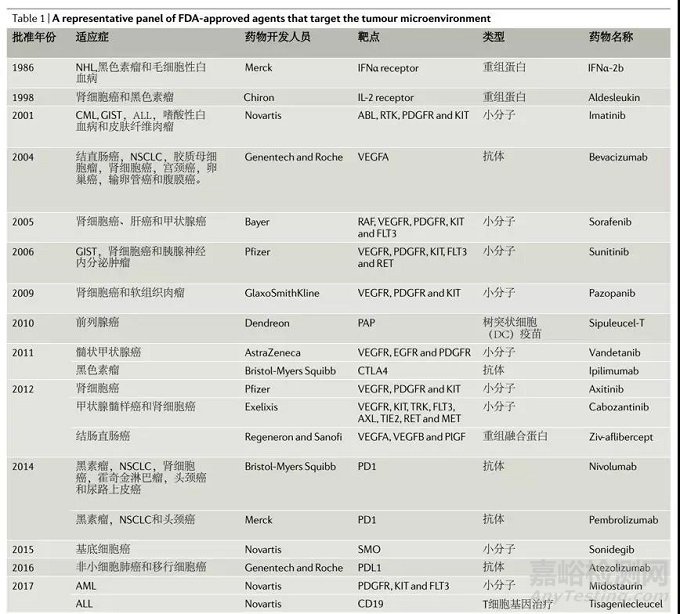
这张表列出了美国食品和药物管理局(FDA)批准的针对肿瘤微环境(TME)不同因素的药物
ALL,急性淋巴细胞白血病;AML,急性髓样白血病;CML,慢性粒细胞白血病;CTL A4,细胞毒性T淋巴细胞抗原4;EGFR,表皮生长因子受体; FLT3, FMS样酪氨酸激酶3; GIST,胃肠道间质瘤; HCC,肝细胞癌;IFNα , α干扰素; IL-2,白介素2; NHL,非霍奇金淋巴瘤; NSCLC,非小细胞肺癌; PAP,前列腺酸性磷酸酶; PD1,程序化细胞死亡蛋白1; PDGFR,血小板衍生生长因子受体; PDL1,程序性细胞凋亡配体1; PIGF,胎盘生长因子; RTK,受体酪氨酸激酶; SMO, Smoothened受体; TIE2,酪氨酸激酶,免疫球蛋白和EGF同源结构域2; TRK,原肌凝蛋白相关激酶(也称为NTRK); VEGF,血管内皮生长因子; VEGFR, VEGF受体。
血管的生成是癌细胞走上扩展的必经之路,但是我们人体海中还有着坚实的护盾免疫系统保卫我们的健康。而免疫系统和癌症之间的战争,也是我们健康的重中之重。

来源: 上海细胞治疗工程技术研


