您当前的位置:检测资讯 > 实验管理
嘉峪检测网 2021-02-23 08:10
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
君实PD-1二线治疗鼻咽癌获批。君实生物PD-1特瑞普利单抗(拓益)第二个适应症获国家药监局批准,用于治疗既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌(NPC)患者。值得一提的是,该单抗联合化疗一线治疗复发转移性NPC的新适应症上市申请刚刚获得了NMPA的受理。在美国,拓益用于治疗NPC已分别获FDA授予的孤儿药资格和突破性疗法认定,是首个获FDA突破性疗法认定的中国国产PD-1单抗。
国内药讯
1.赛诺菲非索非那定片在华获批。赛诺菲抗过敏药盐酸非索非那定片(Allegra)的三项上市申请获国家药监局批准。Allegra是一款第二代H1受体拮抗剂,已在美国获批上市,用于缓解12岁以上的成人和儿童的季节性和常年性过敏性鼻炎相关的症状;以及缓解成人和12岁以上儿童的慢性特发性荨麻疹相关症状。盐酸非索非那定片此次获批的适应症预计为过敏性鼻炎和慢性特发性荨麻疹。
2.太阳药业SMO抑制剂申报上市。太阳药业引进品种磷酸索尼德吉胶囊新药上市申请获CDE受理。磷酸索尼德吉(sonidegib phosphate,商品名Odomzo)是诺华开发的一种口服选择性SMO抑制剂,已在美国获批用于治疗晚期基底细胞癌。一项在不适合局部治疗的局部晚期/转移性基底细胞癌成人患者中开展的Ⅱ期临床BOLT结果显示,磷酸索尼德吉200mg剂量组客观缓解率(ORR)为58%,其中完全缓解率(CR)为5%,部分缓解率(PR)为53%。
3.开拓药业ALK-1抗体联合用药美国临床获批。开拓药业ALK-1抗体GT90001获FDA批准,拟联合百时美施贵宝PD-1单抗纳武利尤单抗(Opdivo),开展二线治疗晚期肝细胞癌(HCC)的Ⅱ期临床试验(全球多中心临床试验,MRCT)。值得一提的是,这一组合针对一线索拉非尼或仑伐替尼治疗后进展的晚期HCC患者的Ⅱ期临床此前已在台湾开展。公布于ASCO GI 2021上的试验数据显示,该联合疗法的客观缓解率(ORR)达到40%。
4.默沙东HIF-2α抑制剂申报中国临床。默沙东1类新药belzutifan片临床试验申请获CDE受理。Belzutifan(MK-6482)是一款在研口服HIF-2α抑制剂,目前正在多个临床中评估治疗VHL相关性肾细胞癌(RCC)、晚期RCC以及晚期实体瘤的潜力。一项Ⅱ期临床数据显示,belzutifan在VHL相关透明细胞RCC患者中达到27.9%的总缓解率,86.9%的患者靶标病变缩小。FDA已授予Belzutifan突破性疗法认定和孤儿药资格。
5.百济神州引进TNFR2拮抗剂独家开发权益。百济神州与Boston Immune 公司达成合作协议,获得Boston Immune一款TNFR2拮抗剂BITR2101在亚洲(日本除外)、澳大利亚和新西兰的独家开发、生产和商业化授权选择权。根据协议,Boston Immune将获得1660万美元的预付款和近期里程碑付款;若百济神州在概念验证研究后行使选择权,Boston Immune有资格获得1.05亿美元的开发、注册及销售里程碑付款;以及产品的销售分成。此外,百济神州参与了该公司A轮优先股融资,为其投资400万美元。
国际药讯
1.以色列接种辉瑞/BioNTech疫苗真实保护数据发表。《柳叶刀》日前发表了以色列大型医学中心接种辉瑞/BioNTech新冠疫苗BNT162b2后的早期保护数据。来自170例确诊病例的数据显示,相较于未接种的医务工作者,接种第一剂疫苗后第1-14天和第15-28天,新冠病毒感染风险分别降低了30%和75%,发展为COVID-19的风险分别降低了47%和85%。值得注意的是,这项分析纳入了无症状感染数据,初步显示了疫苗减少感染风险的功效。
2.武田异体干细胞疗法darvadstrocel申报日本上市。武田扩增脂肪干细胞(eASC)悬浮液darvadstrocel(Cx601)已向日本厚生劳动省(MHLW)提交了上市申请,用于治疗非活动性/轻度活动性管腔克罗恩病(CD)成人患者的复杂肛瘘。darvadstrocel是一款供体来源eASC疗法,已于2018年3月在欧盟获批上述适应症(商品名:Alofisel)。在美国,FDA已授予其治疗CD成人患者复杂肛周瘘的再生医学先进疗法资格和孤儿药资格。
3.创新TCR疗法获FDA突破性疗法认定。FDA授予Immunocore公司新型双特异性TCR疗法tebentafusp(IMCgp100)突破性疗法认定,用于治疗HLA-A*02:01阳性、不可切除性或转移性葡萄膜黑色素瘤(mUM)患者。如果获批,这款新药将是40年来治疗mUM的首个新疗法。一项Ⅲ期临床中期分析显示,与研究人员所选疗法相比(包括dacarbazine、ipilimumab或pembrolizumab),tebentafusp显著提升患者总生存率(OS)。目前数据尚未完全成熟,但tebentafusp组的一年生存率为73%,优于其他疗法组的58%。
4.Incyte外用JAK抑制剂获FDA优先审评资格。FDA受理Incyte公司芦可替尼(ruxolitinib)乳膏的新药申请(NDA)并授予其优先审评资格。ruxolitinib是一种局部用药的选择性JAK1/JAK2抑制剂,用于治疗特应性皮炎(AD)。在包含两项Ⅲ期试验的TRuE-AD研究中,与对照组相比,不同剂量ruxolitinib治疗组8周后达到IGA-TS的患者比例显著更高。FDA预计在今年6月21日之前做出回复。
5.赛诺菲长效因子VIII疗法获FDA快速通道资格。FDA授予赛诺菲创新凝血因子VIII替代疗法efanesoctocog alfa(BIVV001,rFVIIIFc-VWF-XTEN)治疗A型血有病患者的快速通道资格。efanesoctocog alfa是一种新型融合蛋白,已在A型血友病临床前模型中显示出比rFVIII高4倍的止血控制效果,有潜力在一周的大部分时间内提供接近正常的出血保护,用于一周一次的预防性治疗方案中。
6.礼来联手Rigel开发RIPK1抑制剂。礼来与Rigel Pharmaceuticals达成一项独家许可协议,获得Rigel在研RIPK1抑制剂R552在全球开发和商业化包括自身免疫性疾病和炎症性疾病等所有适应症的授权。根据协议,Rigel将获得1.25亿美元前期付款、8.35亿美元的里程碑付款以及分层特许权使用费。此外,Rigel将有资格和礼来共同进行R552在美国的商业化工作,而礼来将承担R552在全球范围内的商业化费用。
7.APOE抗体有望成为阿尔茨海默病的潜在疗法。美国华盛顿大学与Denali Therapeutics公司联合开发的APOE靶向单抗HAE-4,在阿尔茨海默病和脑淀粉样血管病的小鼠动物模型中,与抗淀粉样蛋白抗体相比,能够有效清除大脑组织和血管中的淀粉样蛋白沉积,而且没有增加血管微出血的风险。研究成果发表于Science Translational Medicine上。
医药热点
1.首部医保监管条例出台。《医疗保障基金使用监督管理条例》于2月19日发布,将于2021年5月1日起实施。条例首次具体明确参保人员义务,并明确个人、医药机构以及医保经办机构的骗保处罚。其中,定点医药机构一旦出现骗保行为,最重可面临骗取金额2倍以上5倍以下的罚款,暂停6个月以上1年以下涉及医保基金使用的医药服务;有执业资格的,由相关部门依法吊销执业资格。
2.日本:接种新冠疫苗死亡将获一次性赔款270万元。日本厚生劳动大臣田村宪久19日表示,接种新冠疫苗后,如果因过敏反应等原因死亡,将依据国家预防接种健康受害救济制度一次性赔偿给死者家属4420万日元(约合人民币270万元)。此外,作为丧葬费还会额外支付20.9万日元。日本17日已启动了新冠疫苗接种计划,预计首批将有4万名医护人员接种辉瑞/德国公司新冠疫苗。
3.跨国药企2020年中国业绩出炉。7家跨国药企日前公布了2020年财报。根据财报,这7家跨国药企2020年在中国合计实现214亿美元(约合人民币1476亿元)收入。其中阿斯利康中国业绩为53.75亿美元(占比20.2%),位居第一,其次分别为默沙东35.34亿美元(占比8.2%)、罗氏35.32亿美元(占比7.1%)、赛诺菲29.75亿美元(占比6.8%)、诺华25.73亿美元(占比5.3%)、诺和诺德22.97亿美元(占比11.1%)、礼来11.17亿美元(占比4.6%)。除了受制于带量采购的赛诺菲外,6家药企均实现了正增长。
4.诺华首席执行官去年年薪降至1161万美元。诺华最近发布的2020年度财务详细报告显示,该公司首席执行官瓦斯·纳拉西姆汉2020年的薪酬为1038万瑞士法郎(约合1161万美元),低于2019年的1144万瑞士法郎,同比下降约10%。虽然纳拉西姆汉基本工资比2019年增长了5.5%,但由于诺华2020年实现的总销售额(487亿美元)未达到纳拉西姆汉奖金设定的业绩目标值,致使其最终总薪酬较上一年减少。
股市资讯
【华大基因】降钙素原测定试剂盒/白介素-6测定试剂盒/氨基末端脑利钠肽前体测定试剂盒等十五款试剂盒获批注册
【天士力】氯氮平片(用于精神分裂)获一致性评价
【艾德生物】快报2020年度盈利1.79亿元,同比增长32.47%
审评动向
1. CDE最新受理情况(02月21日)
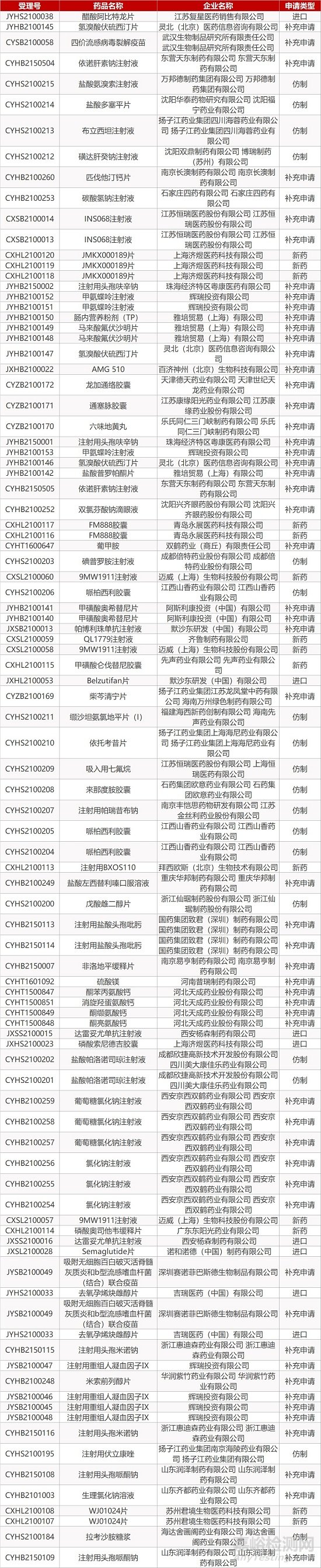
2. FDA最新获批情况(北美02月18日)
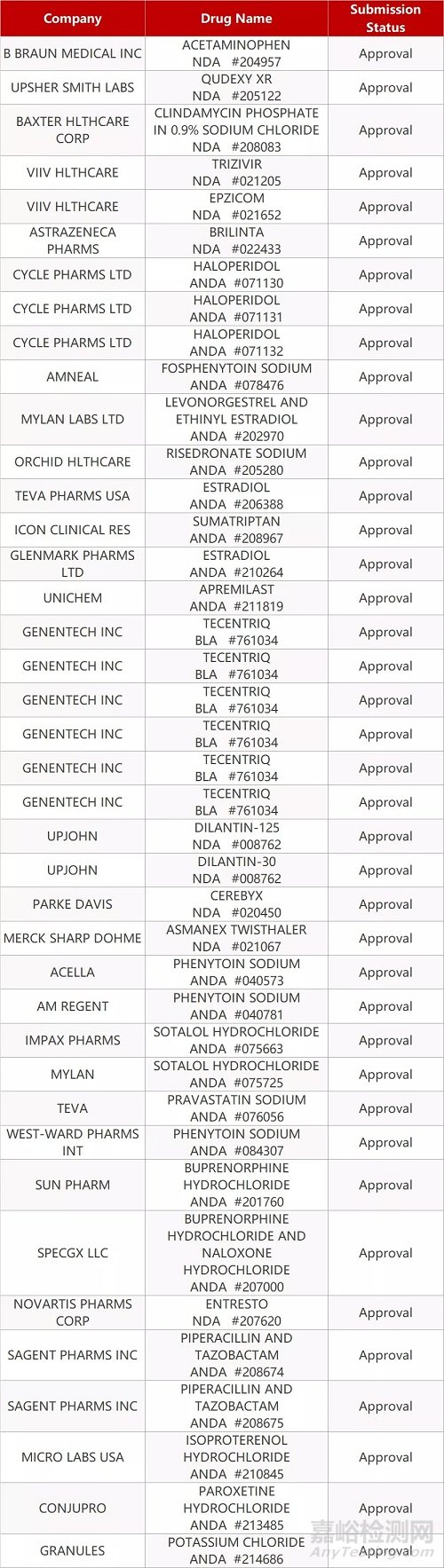

来源:药研发


