您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2021-09-28 23:09
医疗器械临床评价等同性论证技术指导原则
一、前言
对于需要进行临床评价的第二类、第三类医疗器械,若通过等同器械的临床数据进行临床评价,需要进行等同性论证。等同性论证是指将适用范围相同的申报产品与对比器械在技术特征和生物学特性方面进行比对,证明二者基本等同的过程。基本等同包括两种情形:
(一)申报产品与对比器械具有相同的适用范围、技术特征和生物学特性;
(二)申报产品与对比器械具有相同的适用范围,相似的技术特征和生物学特性;有充分的科学证据证明申报产品与对比器械具有相同的安全有效性。
本指导原则中提及的对比器械,指的是注册申请人选择的,用于等同性论证的医疗器械,若对比器械与申报产品通过等同性论证,证明二者基本等同,则对比器械被认为是等同器械。
本指导原则旨在为注册申请人进行等同性论证及药品监督管理部门对等同性论证资料进行技术审评时提供技术指导。
本指导原则是医疗器械临床评价通用指导原则体系的一部分,与《医疗器械临床评价技术指导原则》《医疗器械注册申报临床评价报告技术指导原则》等文件相互引用。
二、适用范围
本指导原则适用于第二类、第三类医疗器械通过等同器械的临床数据进行临床评价时的等同性论证,不适用于按医疗器械管理的体外诊断试剂。
三、产品描述和研发背景
注册申请人需阐明申报产品的基本信息、研发背景、适用范围、已有的诊断或治疗方法及临床应用情况等,建议涵盖以下方面的适用部分,如不适用,需说明不适用的理由:
(一)产品基本信息,如结构组成、材料、软件等;
(二)适用范围;
(三)研发背景与目的;
(四)工作原理和/或作用机理及涉及的科学概念,尤其是器械关键设计特征旨在达到的临床目的以及如何实现其临床目的;
(五)现有的诊断或治疗方法、涉及的产品(如有)及临床应用情况;
(六)申报产品与现有诊断或治疗方法的关系,包括申报产品所支持的诊断或治疗方法,相较于现有方法的创新性;申报产品相对于现有产品的改进点或对其进行仿制;预期是否联合或辅助现有治疗或诊断方法使用等。
(七)申报产品预期达到的临床疗效,如治疗类产品是否可以降低死亡率、改善功能、缓解症状、提高生活质量、降低功能丧失的可能性;明确对症治疗或根治性治疗等;诊断类产品是否用于疾病的预测、检查、诊断或识别对特定治疗有效性较高的患者。
(八)申报产品预期的临床优势,如提高临床安全性和/或有效性,提高使用的便利性等。
四、对比器械的选择
(一)对比器械的要求
对比器械应与申报产品需具有相同的适用范围,相同或相似的技术特征和生物学特性。对比器械应已在境内获准注册。
(二)多个对比器械的使用
建议注册申请人在适宜的情形下,尽量选择一个对比器械,以简化和促进等同性论证过程。当选择一个以上的对比器械时,注册申请人应说明理由,并将多个对比器械分别与申报产品进行充分对比,以论证多个对比器械的数据可用于支持申报产品的安全有效性。此种情况下,建议注册申请人选择与申报产品最相似的产品作为主要对比器械,并尽量减少对比器械的数量。将可能采用多个对比器械的情形举例如下:
1.若申报产品结合了来自多个对比器械的设计特征,在申报产品与多个对比器械具有相同适用范围的前提下,若不同的设计特征在申报产品中组合时不会相互影响,或不同设计特征的组合分别与多个对比医疗器械相比,没有引起不同的安全性有效性问题;
2.若申报产品结合了多个对比医疗器械的适用范围,在申报产品与多个对比器械具有相同适用范围的前提下,若不同的适用范围在申报产品中组合时不会相互影响,或不同适用范围的组合分别与多个对比医疗器械相比,没有引起不同的安全性有效性问题。
(三)对比器械的选择与等同性论证
等同性论证既是判断申报产品与选择的对比医疗器械是否等同的过程,也是判断所选产品是否适宜作为对比医疗器械的过程。若所选产品不适宜作为对比医疗器械,注册申请人可更换或增加其他产品再次进行等同性论证,也可选择其他评价方法。
(四)其他
从医疗器械全生命周期管理的角度,产品获得上市批准后积累临床经验数据非常重要,通过积累临床使用经验进一步确认产品的有效性,充分识别产品的风险,分析产品需要改进的重点,可更为安全有效地对产品进行改进,从而研发出下一代医疗器械。鼓励注册申请人在可行的前提下,选用本企业改进前的产品即前代产品或同系列产品,作为对比医疗器械。
五、等同性论证的基本要求
(一)申报产品与对比器械是否具有相同的适用范围
1.适用范围及临床使用相关信息
适用范围由注册申请人提出,反映在其提供的说明书、产品技术文件和其他信息文件中,包括申报产品在何种临床使用条件下实现哪些具体医疗目的。适用范围相关信息一般包括适应证、适用人群、适用部位、与人体接触方式和时间、适用的疾病的阶段和程度、使用条件、重复使用等。对于具体的医疗器械,由于其设计特征、临床目的、使用经验的不同,以上信息可能是适用范围的组成部分,也可能是适用范围的影响因素。临床使用相关信息一般包括使用方法、禁忌证、警告及预防措施等。
2.适用范围及临床使用相关信息的比较
建议注册申请人在适用的前提下,从如下方面收集申报产品与对比器械的相关信息并进行比较:
(1)适应证:包括器械预防、诊断、缓解、治疗或者监护的疾病或症状;
(2)适用人群:如年龄、性别、体重等对适用人群的限定;
(3)适用部位:如临床应用的具体人体部位、器官、组织、体液等;
(4)与人体接触方式和时间:如植入或体表接触、接触时间、接触次数等;
(5)疾病的严重程度和阶段:如疾病的名称、分型、分期、严重程度等;
(6)使用条件:如使用环境(家用、医院、具体科室、手术室、救护车等)、配合使用的器械或药品、使用者要求等;
(7)重复使用:如可否重复使用、可重复使用的次数和时间等;
(8)使用方法;
(9)禁忌证;
(10)警告及预防措施;
(11)其他。
以上方面的信息,若对于申报产品不适用,可说明不适用的理由。例如,对于预期用于健康人群的器械,适应证可不适用;对于不需要明确具体疾病或症状的器械,如常规使用的无源手术刀,适应证亦可不适用。
3.适用范围是否相同的判定
通过对申报产品与对比器械的适用范围及临床使用相关信息的比较,对二者差异进行充分识别、详细阐述及科学评价,以做出适用范围是否相同的判定。当适用范围的不同引起申报产品与对比器械临床安全有效性的显著差异时,可认为对比器械与申报产品的适用范围不同。
例如,申报产品为α-氰基丙烯酸酯类医用粘合剂,其适用范围为“在其他方法无效的情况下体内组织创面的辅助粘合封闭”,所选对比器械的适用范围为“用于体表切口的局部封闭”。与对比器械相比,申报产品增加了体内使用的相关风险,临床安全有效性具有显著差异,因此,认为对比器械与申报产品的适用范围不同。
又如,申报产品为高压氧舱,其适用范围为“用于婴幼儿缺血、缺氧性疾病的治疗”,所选对比器械“用于成人缺血、缺氧性疾病的治疗”,考虑到婴幼儿和成人在耐受性等方面需要考虑的安全性问题虽有类似,但程度明显不同,婴幼儿人群使用所面临的风险较高,二者间临床安全有效性具有显著差异。因此认为对比医疗器械与申报产品的适用范围不同。
值得注意的是,申报产品与对比器械在适用范围的差异可能引起但并非均会导致适用范围的不同。如申报产品与对比医疗器械虽具有不同的适应证,但对于产品的使用,不同的适应证之间具有同质性,则可认为二者具有相同的适用范围。
例如,常规设计的非骨水泥固定髋关节假体,适用范围可描述为“作为非骨水泥型髋关节假体,适用于具有髋关节置换术适应证的骨骼成熟患者的髋关节置换,以恢复关节功能,缓解疼痛”。该类产品的适应证可包括原发性退变性髋关节骨关节炎、股骨头缺血性坏死进入第IV期、类风湿性关节炎或强直性脊柱炎等全身疾病累及髋关节、髋部创伤后骨关节炎,均为髋关节置换术的适应证,从髋关节置换适用性的角度,具有同质性。当申报产品与对比器械均在上述适应证的范围内,但二者存在差异时,注册申请人可经充分论证,证明申报产品与对比器械在适应证存在差异的情形下,具有相同的适用范围。”
又如,常规设计的强脉冲光治疗仪,适用范围可描述为“用于良性色素性表皮和皮肤病变、良性皮肤血管性病变及脱毛的治疗”。该类产品的适应证可包括雀斑、老年斑、黄褐斑、毛细血管扩张症、红斑性痤疮。当申报产品与对比器械均在上述适应证的范围内,但二者存在差异时,注册申请人可经充分论证,证明适应证的差异将不引起适用范围的不同。
(二)申报产品与对比器械是否具有相同/相似的技术特征、生物学特性
1.技术特征、生物学特性的对比
在确定申报产品与对比医疗器械具有相同的适用范围后,注册申请人需提供技术特征和生物学特性的充分信息并对其进行对比。为便于理解,将技术特征和生物学特性举例并说明如下:
(1)技术特征:
①设计信息:
—工作原理、作用机理;
—器械设计特征及依据:如组成、材料、产品结构的表征(可根据产品特征,选择适用的方式,包括结构图、三视图、爆炸图、局部细节放大图、工程图等)、尺寸和公差、软件等;
—申报器械的重大特性,明确其在整体设计和适用范围下的用途;如果没有明确的用途,应重点详述特定的设计或组件如何促进申报器械的整体使用和功能。
②材料:
—部分产品尤其是植入性医疗器械由于与人体组织直接接触,需明示组成材料详细、完整的化学组成,识别添加剂,如着色剂、涂层或其它表面改性剂等;
—部分产品的材料加工方式(如锻造或铸造)及其状态(如无定形或结晶)可能影响产品的安全有效性,适用时需考虑列出;
—除医疗器械常见组成材料外,部分产品可能涉及生物制剂、药物、涂层、添加剂等。
③能源:如对器械的能源传递(如电池的使用),作为器械功能方面的一部分且对使用产品的患者和/或医务人员有影响的能源传递(如X射线、激光、射频、超声)等。
④产品性能、功能及其他关键技术特征:
—从测试方式角度,如实验室测试、计算机模拟、动物试验、其他模拟临床使用的非临床研究等。
—从技术特征角度,如疲劳、磨损、抗拉强度、压迫、流量、爆裂压力、软件/硬件特性、软件核心算法、密度、孔隙度、体外降解特性、试验方法的原理等。
(2)生物学特性:如降解性能、生物学反应(如免疫反应、组织整合等)等。
值得注意的是,上述各对比项目举例仅为便于理解而提出的一般性举例。对比项目、数据类型和数据量需与产品的研发背景、设计特征、关键技术、适用范围和风险程度等相适应,注册申请人应基于申报产品的具体情况,选择适宜的对比项目,并充分识别、详细阐述申报产品与对比器械间的差异。
2.如何评价技术特征、生物学特性的差异
(1)提供充分的科学证据证明二者具有相同的安全有效性
当申报产品的技术特征和/或生物特性与对比器械存在差异时,需提交充分的科学证据证明二者具有相同的安全有效性,从而论证其等同性。
(2)选择适宜的对比医疗器械,尽可能缩小二者差异
随着差异程度的增大,特别是显著影响或可能显著影响产品安全有效性的差异,进行等同性论证时所需的科学证据将增加。基于上述考虑,建议在适宜的前提下,选择与申报产品尽可能相似的产品作为对比器械,二者的差异不引起不同的安全有效性问题,即申报产品未出现对比器械不存在的且可能引发重大风险和/或引起显著影响有效性的问题。
申报产品与对比器械在技术特征和/或生物学特性的各方面都可能存在差异,某一方面的差异是否引发不同的安全有效性问题,因具体产品和不同情形而异。以无源医疗器械的主要组成材料为例,当申报产品的主要组成材料与选择的对比器械不同时,若该材料已用于具有相同适用范围且已在境内获准上市的同类产品,注册申请人可从材料变化对该产品临床安全有效性的影响、材料性能差异、材料与结构的相互作用、使用该材料的具有相同适用范围的已在境内上市的同类产品的数据等方面进行充分分析,有可能得出“申报产品与对比器械相比,未出现可能引发重大风险或显著影响有效性问题”的结论。此种情形下,选择的对比器械多为申报产品的前代产品,或者其设计特征(如结构)与申报产品最为相似,因此注册申请人未优先选择制造材料最为相似的已上市产品作为对比器械。例如:常规设计的髋关节假体组件-股骨柄,其主要制造材料由前代产品的不锈钢更换为钛合金,结构不变或仅进行微小改进,由于钛合金已广泛应用于其他已获准上市的股骨柄并已有充分的相关数据,注册申请人可考虑使用不锈钢材料制造的前代产品作为对比器械进行等同性论证。又如,申报产品为泌尿导管,在前代产品的基础上增加亲水涂层,该涂层已用于其他已获准上市的泌尿导管并已有充分的相关数据,注册申请人可考虑使用无涂层的前代产品作为对比器械进行等同性论证。
对于无源医疗器械,主要组成材料的不同可能引起产品技术特征、生物学特性的不同,特别是申报产品所用材料尚未用于已上市同类产品的情形,申报产品可能出现选择的对比器械不存在的、可能引发重大风险和/或引起显著影响有效性的问题。例如,隐形眼镜多功能护理液使用的消毒剂尚未用于具有相同适用范围的已上市产品。
(三)相关支持性资料的准备
等同性论证时,申报产品与对比器械进行比对时所用的数据和信息,二者存在差异时证明其具有相同的安全有效性所用的有效科学证据,均为等同性论证的支持性资料。支持性资料通常需包括准确、可靠、完整、可追溯的数据,必要时包括数据的产生过程,试验/实验数据建议来自有良好质量控制的实验室;仅在极少数情形下,可使用一般性描述(如行业的普遍性共识)。未经证实的观点,以及未基于详细数据的科学评价报告不能作为支持性资料。本指导原则只要求做出等同性判定所必需的支持性资料,注册申请人对资料的真实性负责。
医疗器械的研发和改进多为渐进式发展,应基于申报医疗器械的研发历史和设计理念,从产品研发初期开始全面、客观、有序地收集对比器械相关信息和数据,其可为公开发表的文献、数据、信息等,也可来自注册申请人进行的实验室测试、计算机模拟研究、动物试验等;可为注册申请人前代产品或同系列产品的数据和信息,也可为其他注册申请人授权使用的同品种产品非公开数据和信息,后者需提供数据使用授权书,以保证数据来源的合法性。
六、临床评价报告中等同性论证相关内容的编写
建议注册申请人按照附件1所述的步骤并结合正文相应内容进行等同性论证,若已建立申报产品和对比产品的等同性,可使用等同器械的临床数据进行临床评价,并按照《医疗器械注册申报临床评价报告技术指导原则》要求完成临床评价报告中等同性论证相关内容的编写。
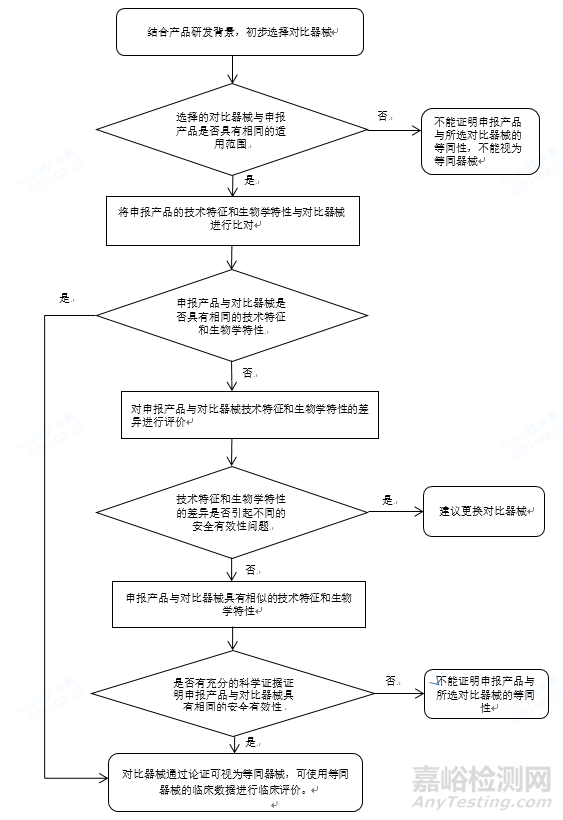
附件:等同性论证流程图
等同性论证流程图

来源:NMPA


