您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-03-16 13:25
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.誉衡生物PD-1新适应症报产。誉衡生物PD-1赛帕利单抗注射液的新适应症上市申请获CDE受理,新适应症推测为宫颈癌。赛帕利单抗注射液(zimberelimab,GLS-010)是由誉衡生物委托药明生物研发的一款全人源抗PD-1单克隆抗体,已于去年8月首次获得NMPA批准上市,用于治疗二线以上复发或难治性经典型霍奇金淋巴瘤。该新药也是誉衡生物首款获批上市的产品。
2.诺华补体抑制剂拟纳入突破性疗法认定。诺华1类新药LNP023胶囊获CDE拟纳入突破性治疗品种,用于C3肾小球病(C3G)患者的治疗。LNP023(Iptacopan)是一款同类首创靶向B因子抑制剂,目前正在Ⅲ期临床中用于治疗IgA肾病(IgAN)、C3G、以及非典型溶血性尿毒综合征。此外,诺华还在开发Iptacopan用于膜性肾病(MN)、阵发性睡眠性血红蛋白尿(PNH)等其他适应症。
3.思路迪CD47抗体启动临床。思路迪医药新一代CD47单抗3D-197登记启动一项I期临床,评价单药在局部晚期或转移性实体瘤和复发或难治性血液肿瘤患者中的安全性、耐受性、药代动力学、药效动力学特征以及有效性。主要研究者为中国医学科学院北京协和医院周道斌博士。在临床前研究中,3D-197(IMC-002)能以高亲和力与CD47结合提高疗效,并未引起体外红细胞凝集,也未引起贫血等CD47抑制剂常见的副作用。
4.恒瑞HER2-ADC获批临床。恒瑞旗下苏州盛迪亚注射用SHR-A1811获国家药监局临床试验默示许可,拟联合氟唑帕利开展用于治疗HER2表达的晚期实体瘤的临床研究。SHR-A1811是恒瑞自主研发的HER2靶向抗体偶联药物,目前已开展多项临床研究,涵盖乳腺癌、晚期实体瘤、晚期胃癌、晚期结直肠癌和晚期非小细胞肺癌。临床前研究显示,SHR-A1811联合氟唑帕利能够产生抗肿瘤协同增效作用。
5.中国抗体IL-17RB单抗获批哮喘临床。中国抗体制药注射用人源化抗IL-17RB单抗SM17获FDA临床许可,计划今年第一季度在美国启动SM17的首次人体临床研究。SM17通过与IL-17RB靶向结合,可抑制人白细胞介素-25(IL-25)导致的Th2细胞相关免疫反应。SM17预计将对气道炎症相关的病理变化产生更广谱的作用,并改善疾病病情,有望在哮喘治疗中发挥潜力。
6.礼来每周1次长效胰岛素在华报IND。礼来长效基础胰岛素LY3209590注射液的临床试验申请获CDE受理。LY3209590是一款每周一次的基础胰岛素-Fc融合蛋白 (BIF),由一个工程化的单链胰岛素类似物融合到IgG Fc区域,以此达到长效目的。在一项II期临床中,每周一次皮下注射BIF与每天一次皮下注射标准的德谷胰岛素相比,患者获得了类似的长期血糖控制,两个治疗组患者32周时A1c平均改善了0.6%和0.7%。
国际药讯
1.诺华SMA基因疗法最新临床积极。诺华基因疗法Zolgensma治疗脊髓性肌萎缩症(SMA)的Ⅲ期临床结果积极。在15例携带3个拷贝的患者队列中,100%患者达到24月龄时无辅助站立≥3秒的主要终点;93%患者实现独立行走;100%患者在试验期间均不依赖营养和呼吸支持。临床中未发生与治疗相关的严重不良事件。3项临床的汇总分析显示,Zolgensma使1型SMA患儿实现或维持了重要的延髓功能(Bulbar Function)指标,包括说话能力、吞咽和满足营养需求以及维持气道保护。
2.长效甲状旁腺激素前药Ⅲ期临床成功。Ascendis公司长效激素疗法TransCon PTH在治疗甲状旁腺功能减退(HP)的Ⅲ期临床达到主要复合终点和所有关键性次要终点。与对照组相比,TransCon PTH治疗组实现不依赖常规治疗并保持血清钙水平在正常范围内(8.3–10.6 mg/dL)的患者比例更高(78.7%vs4.8%,p<0.0001)。TransCon PTH总体耐受良好。Ascendis计划在2022年下半年分别向FDA和EMA提交上市许可申请。
3.遗传性肌萎缩症疗法Ⅱ期临床积极。BridgeBio公司创新口服疗法BBP-418治疗肢带型肌营养不良2i型(LGMD2i)患者的Ⅱ期临床结果积极。数据显示,BBP-418使患者糖基化αDG与总αDG比值较基线平均增加43%;患者肌酸激酶(CK)水平在治疗90天和180天后分别显著降低了70%和77%。未观察到治疗相关严重不良事件、剂量限制性毒性或停药。BridgeBio计划在下半年启动Ⅲ期临床试验。
4.新型IL-2抗体启动首次人体试验。Aulos Bioscience宣布即将启动IL-2单抗AU-007的Ⅰ/Ⅱ期临床试验。AU-007是一种由Biolojic Design计算设计的单克隆抗体,以选择性的有效方式与白细胞介素-2 (IL-2) 结合,能够从物理上阻断IL-2与调节性T细胞上IL-2受体α链结合的能力。AU-007可阻断IL-2与CD25(即α链)的相互作用,从而使内源性IL-2只诱导效应T细胞激活,而不影响调节性T细胞。这是AU-007的首次人体试验。
5.BMS/Nektar免疫组合Ⅲ期黑色素瘤临床失败。Nektar公司CD122偏向性IL-2通路激动剂bempegaldesleukin(BEMPEG,NKTR-214)联合百时美施贵宝PD-1抗体Opdivo治疗转移性黑色素瘤的Ⅲ期临床PIVOT IO-001未达到PFS和ORR的主要终点。NKTR-214是Nektar公司先导免疫肿瘤学候选药物,此前已获FDA授予用于治疗IIB-IV期黑色素瘤的孤儿药资格。值得一提的是,FDA此前已授予bempeg+Opdivo一线治疗不可切除性或转移性黑色素瘤的突破性药物资格。
6.阿斯利康Fasenra新适应症遭FDA拒绝。FDA针对阿斯利康IL-5抑制剂Fasenra的鼻息肉治疗适应症申请发布一份完整回应函(CRL)。FDA认为其Ⅲ期试验OSTRO数据不足以支持该项申请。在这项临床中,与安慰剂相比,Fasenra治疗组第40周时患者的内镜总鼻息肉评分(NPS)和平均鼻塞分数(NBS)均具有统计学意义的改善。目前,一项评估Fasenra与安慰剂相比治疗嗜酸性慢性鼻窦炎伴鼻息肉患者的Ⅲ期临床ORCHID正在进行当中,研究数据预计明年下半年获得。
医药热点
1.北京:医保个人账户资金将专款专用。北京市政府办公厅日前下发《健全北京市职工基本医疗保险门诊共济保障机制实施办法》,改进医保个人账户计入办法,同时规范个人账户使用管理,实现个人账户资金专款专用,提高医保基金使用效率。办法中强调,个人账户不得用于公共卫生费用、体育健身或养生保健消费等不属于基本医疗保险保障范围的支出。
2.李兰娟院士荣获“联合国教科文组织生命科学研究奖”。3月14日晚,联合国教科文组织在法国巴黎举行“联合国教科文组织-赤道几内亚国际生命科学研究奖”颁奖仪式,中国科学家李兰娟院士因在人工肝、微生态及传染病防治领域取得的卓越成就荣获该奖项。此前,中国中医科学院教授、2015年诺贝尔奖获得者屠呦呦也获得该奖项。
3.内地本轮疫情预计4月初得到控制。3月14日,兰州大学新冠肺炎疫情全球预测系统针对我国内地本轮疫情作出预测。初步结果显示,内地本轮疫情预计有望于4月初得到控制,预计累计感染约3.50万人(含确诊病例及无症状感染者)。该团队同时表示,预计到2023年底,全球疫情才有望平息。
4.法国开展第四剂新冠疫苗接种。按照法国官方安排,法国疫苗通行证措施自14日起取消,进入餐饮场所和文化场所均不需出示疫苗通行证;法国的绝大部分室内场所同日起也不再强制要求戴口罩。法国14日起展开第四剂新冠疫苗接种,接种范围是80岁以上老年人群和免疫功能低下的脆弱人群。目前官方没有给其他年龄段的人群接种第四剂疫苗的计划。
评审动态
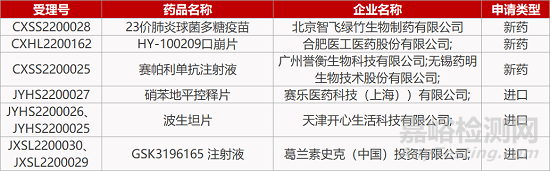
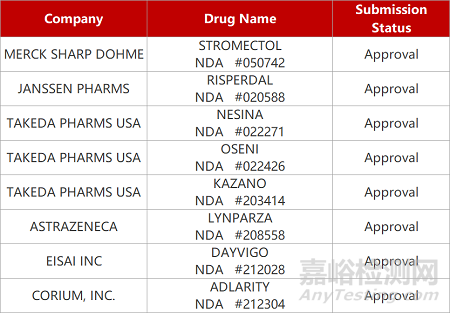

来源:药研发


