您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-04-23 11:54
「 本文共:16条资讯,阅读时长约:3分钟 」
今日头条
复宏汉霖“不限癌种”PD-1单抗拟纳入优先审评。复宏汉霖「斯鲁利单抗注射液」上市申请获CDE拟纳入优先审评,适应症为用于经过标准治疗失败的、不可切除或转移性高度微卫星不稳定型(MSI-H)实体瘤。根据此前披露的临床进展,推测斯鲁利单抗应为PD-1单抗HLX10。该疗法目前正在全球开展多项单药及联合疗法的临床研究。HLX10是国内第10个申报上市的PD-1抗体药物,也是首个用于MSI-H实体瘤适应症的PD-1单抗。
国内药讯
1.NMPA发布2020年药品监督管理统计年度报告。4月20日,国家药监局发布《药品监督管理统计年度报告(2020年)》。报告显示2020年国家药监局受理587件进口临床试验申请,3397件省市补充审批申请;1096个创新药获批临床,20个创新药获批生产,其中仅2个为生物制品;此外,879件新药临床获批(不包含进口药品),其中中药与天然药物共9件,化学药品647件,生物制品223件。
2.国药中生新冠疫苗大规模紧急使用安全性良好。《中华流行病学杂志》刊登题为“新型冠状病毒灭活疫苗(Vero细胞)大规模紧急使用安全性评价”的研究论文,对超过51万人次接种数据的分析显示,国药中生北京所和武汉所开发的新冠灭活疫苗大规模紧急使用总不良反应发生率为1.06%,未发现严重不良反应,该疫苗显示出良好的安全性。
3.罗氏即用型曲妥珠单抗国内申报上市。罗氏曲妥珠单抗注射液(皮下注射)上市申请获CDE受理。皮下注射的曲妥珠单抗是曲妥珠单抗和重组人透明质酸酶组成的复方制剂,已于2019年2月获FDA批准用于治疗成人HER2过表达的转移性乳腺癌,商品名为Herceptin Hylecta®。这种即用型制剂,在2-5分钟内即可完成给药,而静脉输注剂型赫赛汀则所需要的时间是30-90分钟,极大缩短了给药过程的耗时。
4.恒瑞CDK4/6抑制剂SHR6390拟纳入优先审评。恒瑞1类新药SHR6390片上市申请获CDE拟纳入优先审评,适应症为联合氟维司群用于HR阳性、HER2阴性的经内分泌治疗后进展的复发或转移性乳腺癌的治疗。SHR6390是一款口服小分子CDK4/6抑制剂,SHR6390联合氟维司群已在III期临床(SHR6390-III-301)中显著延长这类乳腺癌患者的无进展生存期。全球范围内,已有四款CDK4/6抑制剂获批,分别为辉瑞制药的palbociclib、诺华的Ribociclib 、礼来的Abemaciclib和G1公司的Trilaciclib(国内授权给先声药业)。
5.创新乙肝功能性治愈组合疗法Ⅱ期临床启动。腾盛博药、VIR Biotechnology、与VBI Vaccines公司宣布,VBI Vaccines公司免疫疗法BRII-179(VBI-2601)联合Vir公司候选siRNA疗法BRII-835(VIR-2218),在结合干扰素辅助治疗慢性乙肝病毒(HBV)感染的Ⅱ期临床中完成首例患者给药。这项国际多中心临床将在澳大利亚、中国、韩国、新西兰、新加坡和泰国等国家开展,腾盛博药将主导这项功能性治愈概念验证研究的设计和实施。
6.复旦张江Trop-2靶点ADC新药申报临床。上海复旦张江1类新药注射用FDA018抗体偶联剂临床试验申请获CDE受理。该药物是一款Trop-2靶向抗体偶联药物(ADC),临床拟开发适应症为实体瘤。Trop-2在乳腺癌、肺癌、胃癌等多种肿瘤中的表达水平都会显著升高。Trop-2的高度表达在肿瘤生长过程中起到关键作用。该药物通过与Trop-2结合,递送抗癌小分子药物,杀死癌细胞。该药物的研究旨在探索合适的适应症及相应的治疗窗。
7.上海赛默罗德SR419胶囊申报临床。赛默罗德生物1类新药SR419胶囊的临床试验申请获CDE受理。SR419是该公司自主研发并具有全新机制的治疗外周神经病理痛候选药物,正在澳大利亚进行临床开发。SR419用于外周神经病理痛患者的Ⅰ期临床试验已于去年9月实现了首例患者给药,该项研究旨在评估SR419的有效性、安全性、耐受性以及药代动力学特征。此次是SR419首次在国内申报临床。
国际药讯
1.大麻素新型抗癫痫药Epidyolex新适应症获欧盟批准。欧盟委员会(EC)批准GW Pharma公司Epidyolex(cannabidiol,大麻二醇,CBD)口服液体制剂的II类变更申请,作为一种辅助疗法,用于年龄≥2岁的患者,治疗与结节性硬化综合症(TSC)相关的癫痫发作。这是Epidyolex在欧洲的第三个适应症。此前,该药已被批准用于≥2岁患者辅助治疗与Lennox-Gastaut综合征(LGS)和Dravet综合征(DS)相关的癫痫发作。
2.“渐冻症”新药AMX0035即将在加拿大申报上市。Amylyx制药公司日前宣布其复方制剂AMX0035(苯丁酸钠/牛磺酸二醇)即将在今年上半年和年底前,向加拿大卫生部和欧盟监管机构提交上市申请,用于治疗肌萎缩侧索硬化症(ALS,渐冻症)。在一项CENTAUR试验中,AMX0035与安慰剂相比延长了患者中位总生存期(25个月vs18.5个月),将患者死亡风险降低44%(HR,0.56;95% CI,0.34-0.92;P=0.023)。
3.诺和诺德口服减肥药即将启动关键临床。诺和诺德宣布其口服司美格鲁肽(semaglutide,Rybelsus)即将于今年下半年在肥胖或超重、并伴有合并症的患者中启动国际关键性Ⅲa期临床。司美格鲁肽是一款长效GLP-1类似物,其注射剂型在名为STEP的临床试验中将肥胖症患者的体重平均减轻15公斤。在美国、欧盟和日本,Rybelsus被批准作为饮食和运动的辅助药物,以改善2型糖尿病成人患者的血糖控制。Rybelsus也是首款获FDA批准的口服GLP-1RA。
4.强生放弃前列腺癌组合疗法的监管申请。强生日前宣布将不寻求前列腺癌药物组合Erleada和Zytiga的监管申请。在今年2月发布于ASCO GU 2021会议上的一项Ⅲ期ACIS试验中,Erleada和Zytiga、泼尼松联用与对照组(安慰剂和ZYTIGA、泼尼松)相比,显著改善了化疗初治、正接受ADT治疗的转移性去势抵抗性前列腺癌患者的放射学无进展生存期,将放射学进展或死亡风险降低31%。但在总生存期、启动长期阿片药物的时间、启动细胞毒性化疗的时间等次要终点方面,不具统计学意义上的显著差异。
5.罗氏一季度肿瘤业务总销售额下降19%。罗氏总裁比尔·安德森4月21日在电话会议上透露,在2021年第一季度,该公司销售额达到106亿瑞士法郎,同比下降14%;其中,生物仿制药业务销售额为16亿瑞士法郎,其肿瘤总销售额下降19%;多发性硬化症药物Ocrevus位居销售榜首,达到12.3亿瑞士法郎(+10%),Avastin(8.63亿瑞士法郎,-42%)、Herceptin(7.55亿瑞士法郎,-37%)和Rituxan(7.05亿瑞士法郎)销售分别排第三、第六和第七。
医药热点
1.2021年版国家基本公共服务标准发布。国家发改委等21个部门印发《国家基本公共服务标准(2021年版)》,从幼有所育、学有所教、劳有所得等9个方面明确了国家基本公共服务具体保障范围和质量要求。其中,《国家标准2021》明确为辖区内常住居民建立统一、规范的电子居民健康档案,为辖区内35岁及以上常住居民中原发性高血压患者和2型糖尿病患者提供筛查、随访评估、分类干预、健康体检服务等。
2.川渝签订妇幼健康合作协议。四川省和重庆市签订了《推动成渝地区双城经济圈建设卫生健康一体化发展川渝妇幼健康交流合作协议(2021-2025年)》,川渝两地将建立健全妇幼健康联系协调机制,细化区域合作实施方案;统一制定危重孕产妇和新生儿救治中心评估标准;建立川渝妇幼健康专家库和川渝互派专家机制,建立妇幼远程诊疗机制;深化妇幼健康领域交流合作,健全母婴安全防护网络。
3.广东省药品集采实施方案公开征求意见。广东省医保局发出通告,对广东省药品集采实施方案进行意见征求。计划将医保目录同通用名同剂型药品,按采购金额从高到低依次排序,重点将用量大、采购金额占年度总采购金额前80%的药品纳入省级药品带量采购范围,逐步把更多慢性病、常见病药品纳入带量采购。原则上每年不少于1次。2025年实现省级集团带量采购覆盖国内上市的临床必须、质量可靠的各类药品。
审评动向
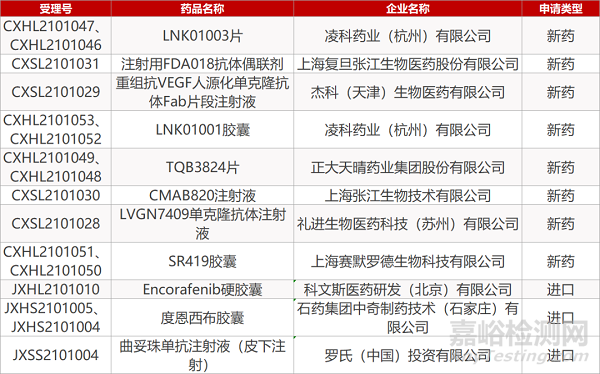
凌科药业的LNK01003片(2个规格)和LNK01001胶囊(2个规格)、复旦张江的注射用FDA018抗体偶联剂、杰科(天津)的重组抗VEGF人源化单克隆抗体Fab片段注射液、正大天晴的TQB3824片(2个规格)、上海张江的CMAB820注射液、礼进的LVGN7409单克隆抗体注射液、上海赛默罗德的SR419胶囊(2个规格)、科文斯医药的Encorafenib硬胶囊。

来源:药研发


