您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-07-14 12:18
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
海创AR抑制剂治疗新冠上Ⅱ/Ⅲ期临床。海创药业AR抑制剂HC-1119获巴西卫生监督局(ANVISA)批准,即将开展用于治疗新冠住院患者的Ⅱ/Ⅲ期临床。该项试验评估HC-1119联合标准治疗在新冠住院患者中的疗效及安全性。HC-1119是海创药业核心在研产品之一,目前正在多项临床中评估用于治疗前列腺癌、治疗高尿酸血症和痛风等适应症的潜力。其用于治疗前列腺癌的国际Ⅲ期临床正在进行当中。
国内药讯
1.基石PD-L1单抗治疗NSCLC结果积极。基石药业公布PD-L1疗法舒格利单抗用于一线治疗IV期非小细胞肺癌(NSCLC)患者的注册性研究(GEMSTONE-302)最终结果。继2020年在无进展生存期(PFS)期中分析时达到了主要疗效终点后, 在近期的PFS最终分析中,舒格利单抗联合化疗进一步延长了患者的PFS和生存获益。详细数据将于学术会议中公布。2020年11月,CDE已受理该新药的上市申请,用于联合化疗一线治疗转移性鳞状和非鳞状NSCLC患者。
2.辉瑞第三代ALK-TKI拟纳入优先审评。辉瑞Lorlatinib片(劳拉替尼 )上市申请获CDE拟纳入优先审评,拟用于既往接受过一种或多种ALK-TKI治疗的ALK阳性局部晚期或转移性非小细胞肺癌 (NSCLC) 患者。Lorlatinib是一款第三代ALK-TKI,具有血脑屏障渗透性特点,旨在用于抑制最常见可导致对当前药物耐药的肿瘤突变和肿瘤脑转移问题。该药目前已获FDA批准用于二线治疗ALK阳性转移性NSCLC患者;以及用于一线治疗ALK阳性NSCLC。
3.康方CD47单抗公布临床新进展。康方生物宣布其自主研发的二代CD47单抗AK117日前已完成澳洲I期剂量爬坡试验。AK117在各个剂量爬坡队列受试者(0.3mg/kg - 45mg/kg QW)中均未发生剂量限制性毒性(DLT),各队列受试者对药物耐受性良好,无需使用低剂量预激给药。该公司同时宣布,AK117已获得CDE批准,开展联合阿扎胞苷治疗急性髓系白血病(AML)的Ib/II期临床研究。
4.渤健获得奥布替尼授权。渤健与诺诚健华就奥布替尼达成合作许可协议。奥布替尼是共价结合的BTK抑制剂,已在国内获批治疗复发/难治慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、以及复发/难治套细胞淋巴瘤;并在多国开展用于治疗复发缓解型多发性硬化的Ⅱ期临床。根据协议,渤健将拥有该药在多发性硬化领域全球独家权利,以及除大中华区外的某些自身免疫性疾病领域的独家权利;诺诚健华将获得1.25亿美元首付款,可能达到8.125亿美元的后期付款,以及产品的销售分成。
5.合源生物完成C轮融资。合源生物宣布完成超4亿元人民币C轮融资。本轮融资由中金资本旗下基金与海松资本联合领投。本轮融资将用于推进该公司靶向CD19的CAR-T产品“CNCT19细胞注射液”在中国的新药注册和商业化、以及全球研发。CNCT19目前正在国内开展治疗复发或难治性急性淋巴细胞白血病、复发或难治性侵袭性B细胞非霍奇金淋巴瘤的临床试验。其中,CNCT19针对复发或难治性急性淋巴细胞白血病的申请已获CDE纳入突破性治疗品种。
国际药讯
1.杨森CD38抗体组合获批二线治疗多发性骨髓瘤。FDA批准杨森和Genmab联合开发的CD38抗体Darzalex Faspro联合泊马度胺和地塞米松(Pd),用于治疗既往接受过至少一种前期治疗的多发性骨髓瘤(MM)成人患者。这也是Darzalex Faspro治疗多发性骨髓瘤的第6个适应症。在一项Ⅲ期临床APOLLO中,与Pd疗法相比,Darzalex Faspro和Pd联用可使疾病进展或死亡风险显著降低37%(P=0.0018);两组患者的中位PFS分别为12.4个月与6.9个月。
2.武田HAE单抗长期疗效积极。武田在欧洲过敏和临床免疫学联合大会期间公布其遗传性血管性水肿(HAE)抗体药物Takhzyro在一项Ⅲ期长期扩展试验中的积极结果。此前的分析结果显示,与基线水平相比,接受Takhzyro治疗的患者血管性水肿发作平均减少了87.4%。长期随访的数据显示,每两周给予Takhzyro治疗,在2.5年治疗期结束的第70天测量HAE发作情况,患者发作率进一步降低至平均92.4%。
3.即用型CAR-T疗法上临床。诺奖得主Jennifer Doudna教授创建的基因编辑公司Caribou Biosciences宣布,该公司基于RNA-DNA杂合序列介导的CRISPR基因编辑系统(chRDNA)开发的创新同种异体抗CD19 CAR-T细胞疗法CB-010,在治疗复发/难治性B细胞非霍奇金淋巴瘤(r/r B-NHL)患者的Ⅰ期临床中完成首例患者给药。值得一提的是,这是首款进入临床试验阶段的敲除PD-1表达的同种异体CAR-T疗法。
4.创新STAT3降解剂显示抗癌活性。Kymera Therapeutics开发的STAT3靶向降解药物KT-333在治疗异常STAT3活化的外周T细胞淋巴瘤(PTCL)时显示出治疗潜力。最新临床前数据显示,KT-333在体外和体内均可导致ALK阳性间变性大细胞淋巴瘤(ALCL),以及携带STAT3突变体的NK/T细胞淋巴瘤,和ALK阴性ALCL细胞系的生长停滞和细胞死亡增加。在动物实验中,每周静脉给药后可导致动物体内ALK阳性ALCL肿瘤消退。该公司计划今年第四季度向FDA提交IND申请。
5.诺和诺德购进ATTR在研产品全球权益。诺和诺德将收购Prothena处于临床Ⅱ期阶段的PRX004抗体的全球开发权益。在临床前研究中,PRX004通过抗体介导的吞噬作用,促进不溶性淀粉样蛋白原纤维的清除并抑制淀粉样蛋白的形成,这有望为转甲状腺素蛋白淀粉样变性(ATTR)患者提供益处。根据协议,Prothena将有资格获得总计最高达12亿美元的开发和销售里程碑付款,其中包括1亿美元的前期和近期临床里程碑付款。
6.FDA暂停Sigilon血友病细胞疗法一项临床。FDA日前暂停Sigilon公司细胞疗法SIG-001在中重度A型血友病患者中进行的一项Ⅰ/Ⅱ期研究。该研究有3例患者接受SIG-001治疗,其中接受最高剂量SIG-001治疗的患者产生了因子VIII的抑制物(特异性中和FVIII的抗体)。FDA要求Sigilon公司提供可能导致这一严重不良事件( SAE)的更多数据。参与本研究的所有3例患者将继续按照研究方案进行随访。
医药热点
1.两款中国新冠疫苗进入COVAX疫苗库。当地时间7月12日,全球疫苗免疫联盟宣布,中国医药集团和北京科兴中维分别与“新冠肺炎疫苗实施计划”(COVAX)签署供应疫苗的合作协议。根据协议,两家企业将于7月起向“新冠肺炎疫苗实施计划”提供疫苗,用于发展中国家的新冠肺炎疫情防控。根据COVAX采购目标,至明年上半年,最多将购买5.5亿剂中国的新冠疫苗。
2.两地将开展12-17岁人群新冠疫苗接种。广西日报7月13日发布消息称,下半年广西壮族自治区将对12-17岁人群开展新冠疫苗接种。湖北省荆州市疾控中心同日也发布了《关于近期全市新冠病毒疫苗接种的提示》。8月1日起,该市将重点开展12-17岁人群和60岁以上人群新冠病毒疫苗免费接种工作,提示18-59岁市民请尽快于7月31日前完成接种。
3.卫生健康信息化发展指数公布。第16届中国卫生信息技术/健康医疗大数据应用交流大会日前在湖北省武汉市召开。会上公布的全国卫生健康信息化发展指数(2021)城市结果显示,直辖市、副省级城市及省会城市总指数排名前十的是:广州、深圳、北京、杭州、上海、宁波、南京、武汉、济南、银川。分指数计算结果显示,样本城市卫生健康信息化治理水平、建设水平和应用水平指数分别为79.22分、74.47分、69.24分。
审评动向
2. FDA新药获批情况(北美07月09日)
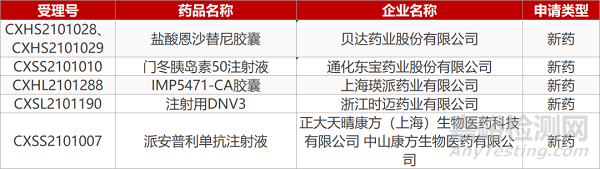
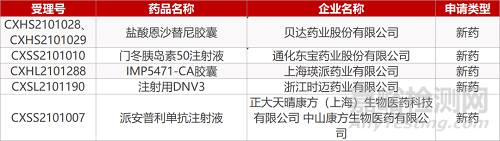

来源:药研发


