今日头条
舒泰神TSLP靶向单抗报哮喘IND。舒泰神1类生物制品“STSA-1201皮下注射液”的临床试验申请获CDE受理。STSA-1201是一款靶向胸腺基质淋巴细胞生成素(TSLP)的单抗药物,旨在通过特异性结合并阻断TSLP与其受体的结合,从而阻断其生物学功能(如树突细胞的激活、Th2细胞因子和趋化因子的释放、嗜酸性粒细胞浸润和IgE的产生,以及气道高反应等)。该新药拟开发用于哮喘的治疗。
国内药讯
1.安进钙敏感受体激动剂获批中国上市。安进盐酸依特卡肽(Etelcalcetide,AMG 416)注射液获国家药监局批准上市,为国内首个且唯一上市的静脉注射型拟钙剂。Etelcalcetide是一款钙敏感受体(CaSR)激动剂,已于2017年在美国获批用于治疗继发性甲状旁腺功能亢进症,针对那些接受血液透析治疗的成人慢性肾脏疾病患者。复星医药拥有Etelcalcetide在中国境内的商业化授权。
2.信达PD-1单抗第7项适应症获批上市。信达生物PD-1抑制剂信迪利单抗注射液(商品名:达伯舒)获国家药监局批准第7项适应症,联合达攸同(贝伐珠单抗生物类似药)以及化疗用于治疗EGFR-TKI治疗失败的EGFR突变非鳞状非小细胞肺癌(NSCLC)。信达最近已在《柳叶刀》子刊上发表关键III期ORIENT-31研究积极结果。此前,信迪利单抗已在中国获批6项适应症均已被纳入国家医保目录。
3.海思科引进渐冻症口溶膜报产。海思科从Aquestive Therapeutics引进的利鲁唑口溶膜(Exservan)的上市申请获国家药监局受理,用于治疗肌萎缩侧索硬化症(ALS,俗称渐冻症)。Exservan是利鲁唑的一种口腔膜剂,利鲁唑是FDA批准的首款治疗ALS的药物,用于推迟ALS患者对呼吸机的依赖、延长生命。该产品只需放在患者的舌头上,无需液体或食物即可迅速溶解,为吞咽困难或者无法吞咽的患者提供新的治疗选择。
4.康宁杰瑞HER2双抗获批Ⅲ期临床。康宁杰瑞与石药集团旗下津曼特生物联合开发的重组人源化抗HER2双特异性抗体注射液KN026获国家药监局批准开展一项Ⅲ期临床,评估与注射用多西他赛(白蛋白结合型)联用一线治疗HER2阳性复发转移性乳腺癌的有效性与安全性。在II期临床中,KN026联合多西他赛达到76.4%的客观缓解率(ORR),中位缓解持续时间(mDoR)为24.0个月,疾病控制率(DCR)为100%。
5.华海双通路融合蛋白获批实体瘤临床。华海药业旗下华奥泰生物自主研发的融合蛋白HB0025注射液获FDA批准开展一项Ⅰb/Ⅱ期临床,拟联合TIGIT单抗HB0030用于治疗晚期实体瘤患者。HB0025是全球首个获批进入临床、能同时阻断PD-1/PD-L1和VEGF/VEGFR这两条信号通路的双特异性融合蛋白,目前已分别在中国和美国获批临床。华海药业计划在中美两国同步开发HB0025以及HB0025的组合疗法用于治疗实体瘤。
国际药讯
1.Eyenoiva扩瞳产品获FDA批准上市。Eyenovia公司开发的托吡卡胺和盐酸苯肾上腺素眼用喷雾剂Mydcombi获FDA批准上市,用于在诊断过程和需要短期瞳孔扩张的情况下诱导散瞳。该产品采用了基于Eyenovia专有的微矩阵药膜(MAP)技术而开发的微量给药系统Optejet,可以将两种散瞳药以微液滴形式给药至眼表。极目生物拥有MydCombi在大中华区及韩国的开发和商业化权益。
2.台新药改良型眼科药物在美报NDA。台新药股份有限公司开发的针对眼科术后抗炎镇痛的改良型新药激素纳米混悬滴眼液(APP13007)已在美国递交了新药上市申请。GPN00833为一种强效皮质类固醇丙酸氯倍他索(0.05%)的新型水性纳米混悬滴眼液。远大医药拥有APP13007在中国大陆、香港和澳门地区的独家开发和商业化授权。今年4月,该新药已获国家药监局批准开展III期临床研究。
3.杨森IL-23抑制剂UC Ⅲ期临床积极。强生旗下杨森IL-23抑制剂Tremfya(guselkumab)治疗中重度溃疡性结肠炎(UC)的Ⅲ期临床QUASAR达到主要研究终点。与安慰剂组相比,Tremfya治疗组患者12周时达到临床缓解的比例更高(22.6%vs7.9%,p<0.001);两组临床应答、内镜改善和组织内镜粘膜改善的患者比例分别为61.5%vs27.9%(p<0.001)、26.8%比11.1%(p<0.001)和23.5%比7.5%(p<0.001)。药物相关不良事件发生率与安慰剂相似。
4.礼来IL-23p19单抗UC Ⅲ期临床积极。礼来IL-23p19单抗mirikizumab治疗中重度活动性溃疡性结肠炎(UC)的两项Ⅲ期试验(LUCENT-1和LUCENT-2)最新结果积极。在12周和52周时,mirikizumab治疗组患者由于急需排便的缓解导致炎症性肠病问卷(IBDQ)总分分别提高44.8%和32.5%;其中分别有22.7%和39.1%的改善是由于直肠出血得到缓解,而32.5%和28.4%的改善则是源自排便频率的缓解。另外,mirikizumab治疗UC儿科患者的Ⅱ期临床中期数据与LUCENT-1试验结果一致。
5.记忆样通用NK细胞疗法获批实体瘤临床。INmuneBio公司NK细胞免疫疗法INKmune™获FDA批准开展I/II期临床,评估用于肿瘤治疗的安全性与有效性。INKmune™是一种无复制能力的人类肿瘤细胞系,它与静息NK细胞结合并提供多种基本的启动信号。临床前研究显示,INKmune将患者的rNK细胞转化为记忆样NK细胞,该种细胞能够克服免疫微环境的免疫抑制和缺氧难题,直接靶向实体瘤并发挥杀伤作用。
6.苏庇医药约17亿美元收购CTI公司。苏庇医药(Swedish Orphan Biovitrum)宣布将以约17亿美元收购CTI BioPharma,并获其主导产品骨髓纤维化新药Vonjo(pacritinib)。pacritinib是一款能特异性抑制JAK2、IRAK1和CSF1R的口服激酶抑制剂,已于去年3月获FDA加速批准上市,用于治疗伴有严重血小板减少症的骨髓纤维化患者。交易完成后,CTI BioPharma将成为苏庇医药的全资子公司,并共同推进pacritinib在治疗骨髓增生性疾病方面的潜力。
医药热点
1.上海市胸科医院心胸疾病临床医学中心项目获批。据上海市发展改革委消息,上海市胸科医院心胸疾病临床医学中心项目已获得可行性研究批复,选址位于浦东新区唐镇,建设用地25523平方米,新建总建筑面积119953平方米,其中:地上80794平方米、地下39159平方米。项目总投资金额142523万元。该项目聚焦胸部肿瘤学和心血管病学,将打造集临床诊疗、临床研究、转化医学、基础研究为一体的产学研医发展中心和人才培养高地。
2.胡华忠任复旦上医党委副书记、纪委书记。5月8日上午,复旦大学上海医学院领导班子调整宣布会议举行。会议宣布了中共上海市委决定,胡华忠同志任复旦大学上海医学院党委副书记、纪委书记,免去复旦大学上海医学院党委副书记、纪委书记杨伟国同志的纪委书记职务。
3.郑州市阶段性降低职工医保缴费费率。为进一步减轻参保单位和灵活就业人员负担,郑州市本月起,在不降低参保人员医保待遇水平的前提下,将阶段性降低职工基本医疗保险缴费费率。新政规定,执行期限内, 郑州市职工基本医疗保险费率阶段性降低1个百分点,其中,职工医保缴费费率由原来的10%调整为9%,不含生育保险。具体来说,就是原来单位职工医保缴费费率率为8%、个人为2%,调整后,单位缴费率下调为7%、个人缴费率仍为2%。在此期间,郑州市灵活就业人员基本医疗保险费率阶段性也降低1个百分点,由原来的10%调整为9%。
评审动态
1. CDE新药受理情况(05月10日)
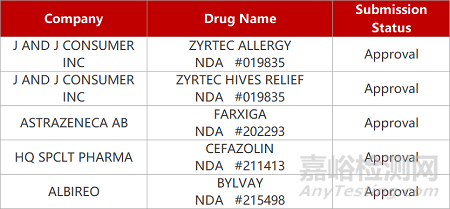
2. FDA新药获批情况(北美05月08日)