今日头条
先声USP1抑制剂获批实体瘤临床。先声药业自主研发的泛素特异性肽酶1(USP1)小分子抑制剂SIM0501获FDA临床许可,拟开展用于晚期实体瘤治疗的临床试验。在临床前研究中,SIM0501单药或与PARPi联合,均对HRD肿瘤有显著的抗增殖活性,且药物安全性良好。在中国,国家药监局已在10月受理了SIM0501的新药临床试验申请。
国内药讯
1.赛神Lp-PLA2抑制剂早期临床积极。赛神医药拟开发用于治疗阿尔茨海默病(AD)和其他神经退行性疾病的Lp-PLA2小分子抑制剂SNP318,在健康受试者中开展的Ⅰ期临床获积极结果。初步数据显示,SNP318在脑脊液(CSF)中有较好的分布,可完全抑制人体外周和中枢神经系统的靶点酶活性;药物耐受性良好,未观察到严重不良事件(SAEs)。赛神医药计划明年开展评估治疗AD的Ⅱ期临床。
2.甘李口服GLP-1R激动剂获批临床。甘李药业1类生物制品GZR18片获国家药监局临床试验默示许可,拟开发用于治疗2型糖尿病。GZR18是长效GLP-1R激动剂肽类药物,拟开发用于成年患者的2型糖尿病(T2DM)的治疗或肥胖/超重患者的体重管理。根据公开信息,该产品的注射制剂正在国内开展II期临床,评估与司美格鲁肽(诺和泰)对比,每周注射一次治疗2型糖尿病患者的效果。
3.贝达引进BiDAC降解剂获批肺癌临床。C4 Therapeutics公司1类化药CFT8919片获国家药监局临床试验默示许可,拟开发用于治疗携带EGFR突变的局晚期或晚期非小细胞肺癌(NSCLC)患者。CFT8919是一种BiDAC降解剂,已在临床前研究中显示出针对EGFR L858R驱动的NSCLC体内外模型的治疗潜力;同时对T790M或C797S突变的EGFR继发耐药突变有效。贝达药业拥有CFT8919在大中华区开发、制造和商业化权益。
4.和铂撤回引进FcRn抗体上市申请。和铂医药从HanAll Biopharma引进的FcRn抗体巴托利单抗(HBM9161)已在国内撤回用于治疗全身型重症肌无力(gMG)的上市申请。今年3月,HBM9161已在治疗gMG的关键III期临床达到主要终点及关键次要终点。基于临床试验方案,和铂医药正在进行III期临床的延期,并收集其他长期安全性数据。该公司计划将其他长期安全性数据纳入上市申请,并于明年上半年重新提交其上市申请。
5.和誉CSF-1R小分子抑制剂授权默克。和誉医药宣布已与德国默克就其临床后期CSF-1R小分子抑制剂pimicotinib(ABSK021)达成独家许可协议,授予后者在中国大陆、香港、澳门和台湾地区针对pimicotinib就所有适应症进行商业化的许可,和誉医药将保留在授权区域内独家开发pimicotinib的权利。根据协议,和誉医药将获得7000万美元首付款,如果德国默克行使全球商业化选择权,和誉医药还将获得额外款项,交易总额可能高达6.055亿美元。
国际药讯
1.NK-1受体拮抗剂美国报胃轻瘫NDA。Vanda公司神经激肽-1(NK-1)受体拮抗剂tradipitant的新药申请(NDA)获FDA受理,用于治疗胃轻瘫。PDUFA日期为明年9月18日。tradipitant可影响胃蠕动过程,并在负责恶心和呕吐的脑区域直接影响神经传递,从而起到治疗胃轻瘫症状的作用。今年5月,该新药也在治疗晕动症(尤指晕车)的III期Motion Syros研究获得积极结果。
2.长效VEGF眼科新药Ⅱ期临床成功。EyePoint公司VEGF受体阻断剂EYP-1901治疗湿性年龄相关性黄斑变性(AMD)的Ⅱ期临床DAVIO 2达到所有主要终点和次要终点。与aflibercept相比,EYP-1901(2mg和3mg)治疗患者的最佳矫正视力 (BCVA)(第28周和第32周合并)效果达到非劣效性标准(组间差为-0.3和-0.4个字母);患者治疗负担分别减少了89%和85%,近三分之二的眼睛在长达六个月的时间内无需额外治疗。药物安全性良好。贝达药业拥有EYP-1901的中国权益。
3.Arcturus公司CFTR靶向药获孤儿药资格。FDA授予Arcturus 公司开发拟用于治疗囊性纤维化(CF)的候选药物ARCT-032孤儿药资格。ARCT-032利用Arcturus的LUNAR®脂质气溶胶平台将囊性纤维化跨膜传导调节因子(CFTR)信使RNA输送到肺部,并在肺部表达CFTR mRNA的功能拷贝以恢复CFTR的活性,减轻导致进行性肺部疾病的下游效应。该公司将在明年上半年公布ARCT-032治疗CF的Ⅰb 期中期数据。
4.罗氏BTK抑制剂部分临床被FDA暂停。罗氏口服BTK抑制剂fenebrutinib在治疗复发性多发性硬化症(RMS)的III期FENhance研究中观察到药物性肝损伤事件。有两例患者接受治疗后出现肝转氨酶(肝酶)升高并伴有胆红素升高,两例患者均无症状,停药后指标恢复正常。目前,FDA已暂停针对RMS的III期FENhance I试验在美国的新入组工作。在美国以外国家/地区的入组工作仍在继续。
5.阿斯利康布局“不可成药”药物赛道。阿斯利康与Absci公司将利用后者创新生成性人工智能(AI)技术,为特定的肿瘤靶标开发治疗性候选抗体。Absci技术平台通过测量数百万个蛋白质-蛋白质相互作用来生成专有数据,以发现创新、“不可成药”药物靶点来提高药物成功开发的可能性。根据协议,Absci将获得预付款、研发经费和里程碑款项等,总金额高达2.47亿美元。
6.创新细胞递送基因药物公司完成A轮融资。Cytonus公司宣布完成金额达1170万美元的A轮融资,以用于开发一种全新的药物递送方式,通过改造细胞(cargocytes)作为脂质纳米颗粒的替代品,将编码抗癌蛋白的mRNA疗法递送到肿瘤中,治疗转移性癌症和中枢神经系统(CNS)疾病。该公司还计划将cargocytes应用于溶瘤病毒,开发出能通过系统性注射给药的溶瘤病毒疗法。
医药热点
1.上海“诞生” 脊柱健康个性化测量门诊。为持续推动脊柱健康管理的理念,上海市第十人民医院骨科探索性开设的脊柱健康个性化测量门诊正式开诊。在脊柱健康个性化测量门诊,医生将为就诊者测定与脊柱有关的数据并通过后台AI数据库测算,生成一张专属的健康报告。在诊断的基础上,根据患者的睡眠习惯、工作学习场景、脊柱病变情况等提出个体化方案(比如:要睡多硬的床垫、要枕多高的枕头、工作时的桌椅多高为宜等)。
2.中国医学科学院血液病医院互联网医院启动。11月25日,中国医学科学院血液病医院互联网医院在中国血液病专科交流工作会议上举办启动仪式。血液病医院互联网医院构建起覆盖诊前、诊中、诊后的线上线下一体化医疗服务模式,为全国患者提供包括预约挂号、预约取号、门诊缴费、检查检验报告查看、办理入院、住院押金缴费、每日清单、出院结算等服务,还有在线问诊、药品邮寄、专家咨询、随访管理等线上诊疗服务。患者可通过支付宝搜索【血液病医院互联网医院】小程序,登录后即可享受全病程的诊疗服务。
3.柳叶刀子刊:中国癌症死亡上升21.6%。近日,中国疾控中心殷鹏、齐金蕾、首都医科大学李梦龙等研究人员在《柳叶刀》子刊" The Lancet Public Health "上发表的一篇最新研究论文显示,2005-2020年,中国癌症相关总死亡人数增加21.6%,在男性和女性中,前三大致命癌症依次是:气管癌、支气管癌和肺癌;肝癌;胃癌。
4.广东省全面推进医疗设备租赁入院。近日,广东省政府发布《在我省教育科技、卫生健康等领域开展设备租赁试点工作方案的通知》,并且同步下发了《关于在我省教育领域开展设备租赁试点的工作方案》。这份文件明确为加快先进设备购置、缓解财政一次性支出压力,提升相关医疗服务能力并补齐短板,开展在医疗机构相关医疗设备租赁试点。
评审动态
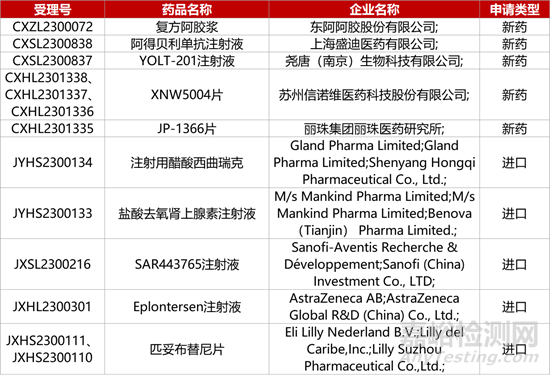
1. CDE新药受理情况(12月05日)
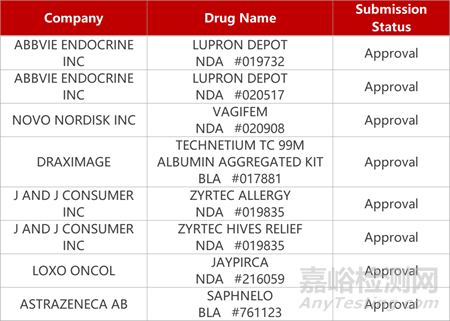
2. FDA新药获批情况(北美12月04日)