今日头条
捷思英达Aurora A抑制剂上肝癌临床。捷思英达小分子创新药Aurora A抑制剂VIC-1911联合仑伐替尼在治疗晚期肝癌的中国临床完成首例患者给药。该项试验由上海仁济医院夏强院士牵头发起,旨在评估VIC-1911联合用药治疗仑伐替尼耐药晚期肝癌的有效性与安全性。转化医学研究显示,VIC-1911与仑伐替尼联用有望克服其内源性和获得性耐药,提高疗效。
国内药讯
1.默沙东K药中国获批一线治疗胃癌。默沙东PD-1抑制剂帕博利珠单抗获国家药监局批准新适应症,联合含氟尿嘧啶类和铂类药物用于一线治疗局部晚期不可切除或转移性、HER2阴性胃或胃食管结合部腺癌患者。在Ⅲ期试验(KEYNOTE-859)中,Keytruda联合化疗较单独化疗降低患者死亡风险达22%,患者总生存期显著改善(中位OS:12.9vs11.5个月)。这是K药在中国获批的第12个适应症。
2.默沙东PCSK9抑制剂启动国际Ⅲ期临床。默沙东PCSK9抑制剂MK-0616(enlicitide)在中国登记启动一项针对动脉粥样硬化、高胆固醇血症适应症的国际Ⅲ期临床,拟在高心血管风险受试者中评价MK-0616减少主要心血管不良事件的有效性和安全性。该项研究中国部分由首都医科大学附属北京安贞医院马长生博士牵头开展。今年10月,该新药已在国内启动治疗高胆固醇血症的国际Ⅲ期研究。
3.益方KRAS G12C抑制剂拟纳入优先审评。益方生物KRAS G12C抑制剂格舒瑞昔片(D-1553片,Garsorasib)获CDE拟纳入优先审评,用于既往经一线系统治疗后疾病进展或不可耐受的、并且经检测确认存在KRAS G12C突变的局部晚期或转移性非小细胞肺癌的治疗。在I/II期研究中,D-1553确认的客观缓解率(ORR)为40.5%,疾病控制率(DCR)为91.9%。正大天晴拥有该新药在中国大陆地区开发、注册、生产和商业化的独家许可权。
4.恩瑞恺诺CAR-NK疗法红斑狼疮IIT临床积极。南京恩瑞恺诺公司开发的现货型CD19靶向CAR-NK细胞疗法KN5501,在上海长海医院开展用于治疗复发/难治的系统性红斑狼疮的临床试验(研究者发起)完成4例患者的CAR-NK回输治疗。根据国际SLEDAI-2K(轻度、中度、重度)三级病症评分标准,4例重度患者均实现深度缓解,由“重度”转为“轻度”,并表现出相应的持久性。这是利用CAR-NK治疗系统性红斑狼疮的首个临床报告。
5.圣诺mRNA疫苗获批RSV临床。圣诺医药旗下RNAimmune(达冕生物)创新型呼吸道合胞病毒(RSV)mRNA疫苗RV-1770获FDA批准开展Ⅰ期临床,评估用于预防成年人RSV感染的安全性与有效性。RV-1770具有独特的AI增强序列的骨架设计,并采用近期分离出的RSV临床毒株序列。在临床前的棉鼠模型研究中,该疫苗展示出同时针对RSV A亚型和B亚型菌株的免疫反应及中和作用。
国际药讯
1.新型CAR-T治疗重症肌无力获快速通道资格。Kyverna公司靶向CD19的自体CAR-T疗法KYV-101获FDA快速通道资格,用于治疗重症肌无力(MG)。KYV-101旨在深度诱导血液循环和组织实现B细胞完全耗竭,该新药拟开发用于治疗B细胞驱动的自身免疫性疾病(如狼疮性肾炎、系统性硬化症和炎性肌病)。今年6月,KYV-101用于治疗难治性狼疮肾炎(LN)已获得FDA快速通道指定。
2.创新口服GLP-1R激动剂Ⅱa期临床积极。Structure公司口服胰高血糖素样肽-1(GLP-1)受体激动剂GSBR-1290治疗2型糖尿病(T2DM)与肥胖患者的Ⅱa期临床结果积极。在T2DM队列中,第12周时两个剂量组患者HbA1c显著降低(分别降低1.01%和1.02%),体重也显著减轻(分别减轻3.51%和3.26%);在肥胖队列中,第8周时患者体重显著降低4.74%。临床中没有研究相关的严重不良事件(SAE)发生。
3.创新IL-17纳米抗体银屑病临床前研究积极。Scinai公司基于羊驼的纯重链抗体可变域开发的IL-17纳米抗体在治疗银屑病的临床前研究结果积极。与对照组相比,这款纳米抗体皮内注射一线治疗显著减少IL-17释放(p<0.001),类似于倍他米松和Cosentyx的作用;在减少炎症诱导方面,疗效比倍他米松更好,与Cosentyx单抗一样有效。此外,药物局部给药耐受性良好。
4.诺和诺德基金会启动疫苗开发项目。诺和诺德基金会宣布将在哥本哈根大学和丹麦国家血清研究所投入高达2.6亿美元启动一项疫苗研究和开发计划,旨在开发能在气道中产生强大的局部免疫力的新型疫苗,用于预防和治疗结核病(TB)、流感、A群链球菌(GAS)等呼吸道疾病。该项研究将并排比较不同的疫苗抗原、平台和递送方法,以增加疫苗成功开发的机会。
5.Checkpoint公司PD-L1单抗上市遭FDA拒绝。Checkpoint公司PD-L1抑制剂cosibelimab用于治疗转移性或局部晚期皮肤鳞状细胞癌(cSCC)的生物制剂许可申请(BLA)收到FDA发出的完整回复函(CRL)。FDA明确拒批是因为在检查中发现第三方合同生产组织的问题。关键研究最新数据显示,cosibelimabz在晚期cSCC患者中客观缓解率(ORR)达到55%,在转移性cSCC患者中ORR为50%。
6.PPARδ激动剂治疗PMM的Ⅱb期临床失败。Reneo公司PPARδ选择性激动剂mavodelpar(REN001)治疗原发性线粒体肌病(PMM)的IIb期STRIDE(NCT04535609) 研究未达到主要终点或次要终点。与安慰剂相比,REN001治疗24周时患者的12分钟步行测试步行距离与基线相比变化的统计不具统计学显著性;PROMIS F-SF 13a评分相对于基线的变化也未达到显著改善。受此影响,该公司股价暴跌82%。
医药热点
1.国家骨科医学中心保膝联盟成立。12月17日,国家骨科医学中心保膝联盟在京成立。保膝联盟依托国家骨科医学中心,充分发挥北京积水潭医院骨科优势,统筹优质资源,加强28家成员单位之间临床、教育、科研等方面合作,旨在将首批保膝联盟医院逐步打造成区域保膝中心,成为各地保膝的培训基地和治疗中心,进一步推动优质医疗资源下沉,带动周边保膝理念技术发展,惠及更多患者。
2.中山医院国家医学中心建设工程启动。12月18日,复旦大学附属中山医院国家医学中心建设项目的两个重点工程——上海国际医学科创中心工程、青浦新城院区一期工程同时启动。未来,上海国际医学科创中心将主要承担疫苗药物医疗器械研发攻关中心和医学研究转化中心两大核心功能。青浦新城院区作为长三角一体化示范区内的新型三甲医院,将承载高质量临床诊疗中心、国际医学交流合作中心、骨干人才培养中心、中西医协同创新中心和公共卫生中心等国家医学中心的功能布局,助力长三角医疗一体化进程。
3.美国Orchid Health公司推出人类胚胎基因筛查服务。据《科学》新闻(Science News)消息,近日,美国Orchid Health公司宣布推出针对人类胚胎的全基因组测序筛查服务,可检测出有潜在神经发育障碍、肥胖、精神疾病等风险的胚胎,费用为每个胚胎2500美元(约合人民币1.77万元)。此举遭到国际科学家组织——精神病学基因组学联盟(Psychiatric Genomics Consortium, PGC)的强烈反对,他们称该公司使用了他们长达十年来积累的数据并违反了将数据用于胚胎筛查的限制。
评审动态
1. CDE新药受理情况(12月19日)
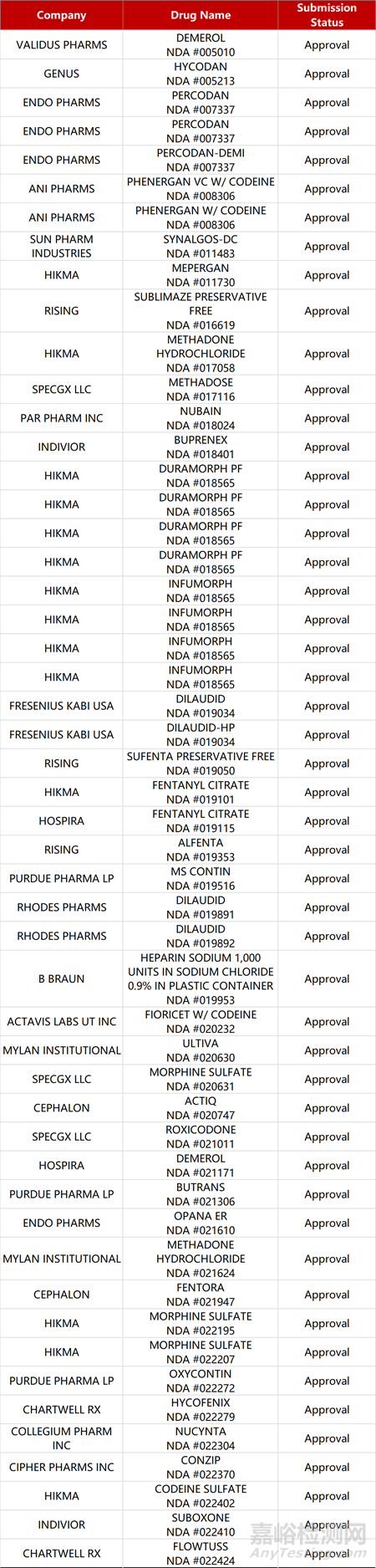
2. FDA新药获批情况(北美12月18日)