您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-08-27 12:16
1. 概 念
对床旁和自测的IVD产品,制造商必须开展可用性测试Usability Testing、可用性工程Usability Engineering,并通过可用性工程文件Usability Engineering File证明,以便通过公告机构批准。
可用性测试过程识别使用过程中的安全风险并予以记录,然后通过可用性工程重新设计产品,以确保尽可能安全地使用。
可用性测试对证明产品安全可用性而言至关重要,目的在于:测试特定用户是否能够在特定的使用环境中有效、高效、令人满意地使用制造商所提供的产品或服务,而且产品或服务不得对用户、患者或第三方造成任何伤害,由此证明该体外诊断产品符合IVDR的可用性要求。
形成性可用性测试(Formative usability testing)→允许将人为因素纳入医疗器械的设计和生产中。用户体验对产品性能有着巨大影响,产品开发过程中应当尽早且经常发现可用性问题,于潜在用户错误发生前阻断这些错误发生的机会。
总结性可用性测试(Summative usability testing)→专注于产品功能的定量研究,是对最终产品的有效性、效率和满意度的综合评估,评估产品最终版是否符合所有产品要求,并在形成性可用性测试中发现问题和加以解决后进行。通常评估各种使用特征,包括:错误率、完成任务的时间、总体客户满意度。
注意:与发现特定设计问题为中心的形成性可用性测试不同,总结性可用性测试根据特定、定义的性能预期对产品开展全面评估。
2. 步 骤
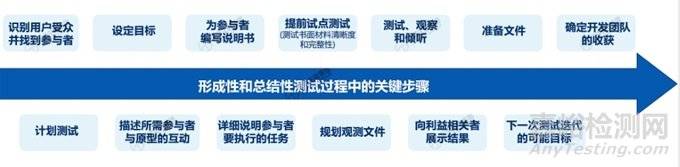
3. 要 点
√ 正确的准备
■ 必须已定义产品预期目的、预期使用人群、使用环境、使用方法。
■ 必须已完成产品性能评估测试。
■ 必须确保产品使用说明完整以开展总结性测试。
√ 正确的使用人群
为证明产品可被安全使用,制造商需证明指定使用人群能够在无严重错误情况下使用产品,参与者必须始终与产品的目标群体保持一致。
对于非专业人员(layperson),必须检验社会各阶层的代表性,因此往往需要大量可用性测试的参与者,有时候对参与者需要有所限制,例如:妊娠测试仅针对特定年龄段女性进行。
√ 正确的使用环境
制造商需要在可用性测试过程中模拟现实的使用环境,例如:制造商宣称其产品可在嘈杂场所使用,则必须模拟出使得测试参与者注意力易分散、不易集中的使用环境。
√ 真实的取样过程
为非专业使用而设计的体外诊断产品,必须由非专业人员进行取样和操作,可用性测试由此作为临床研究需要获得道德委员会的批准。
√ 说明书的可读性
即IFU readability,所有参与测试的非专业人员都必须能够借助说明书进行正确采样、操作、获得测试结果、正确解释所有可能的测试结果。

来源:久顺集团技术服务


