您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-11-11 12:05
摘要: 采用旋涂法在汽车用镁合金表面制备了4种改性涂层(不含有机改性硅酸盐涂层和有机改性硅酸盐涂层),对比分析了改性涂层的显微形貌以及在3.5% NaCl溶液中浸泡不同时间后的耐腐蚀性能。结果表明,相较镁合金基体,浸泡前的不含有机改性硅酸盐涂层A试样和浸泡1 d~9 d的涂层试样的腐蚀电位都正移,腐蚀电流密度明显减小,涂层A的耐腐蚀性能明显优于镁合金基体;4种改性涂层的腐蚀电位都相较镁合金基体发生正向移动,且有机改性硅酸盐涂层(涂层B、涂层C和涂层D)的腐蚀电位都比涂层A更正、腐蚀电流密度相较涂层A更小,腐蚀电流密度从小至大顺序为:涂层C<涂层D<涂层B<涂层A<基体。随着浸泡时间的延长,4种改性涂层的腐蚀电流密度都在增加,但相同浸泡时间下,涂层B和涂层C的腐蚀倾向相比涂层A更小、腐蚀速率相比涂层A较慢,且涂层C(KH-570/BTMSE=3/2)具有最佳的耐蚀性能。
关键词: 汽车;AZ31B镁合金;涂层;浸泡;耐腐蚀性能
AZ31B镁合金由于具有密度低、比强度高、良好的弯曲性能、较高的韧性和抗阻尼性能等,在汽车、电子等行业有着广泛应用[1],尤其是随着汽车轻量化的发展,用镁合金制作的汽车零部件(轮毂、发动机、车身等)也逐渐增多,这为镁合金带来巨大发展机遇的同时也对镁合金的使用性能提出了更高的要求[2],如汽车用镁合金除需要具备良好的强韧性外,还需要具有良好的耐腐蚀性能[3-5]。而镁合金的耐腐蚀性较差,一直是制约其更广泛应用的瓶颈,较为可行的方法是对镁合金进行表面改性处理[6],以在不改变原有镁合金基体的固有物性外,进一步提升其耐腐蚀性能。虽然目前对镁合金进行表面改性方面的报道较多,如表面激光处理、表面化学镀等[7-9],但是这些改性层的研究主要集中在无机涂层,而关于在镁合金表面制备有机改性涂层方面的报道较少。本文以化学结构相对比较对称、通过脱水缩聚获得更多交联点的KH-570硅烷偶联剂和1,2-双三甲氧基硅基乙烷(BTMSE)硅烷偶联剂为原料,采用旋涂法在镁合金表面制备4种改性涂层,对比分析了镁合金基体和4种改性层在3.5% NaCl溶液中浸泡不同时间后的显微形貌和耐蚀性能,以期优化改性层的制备工艺并推动有机改性涂层在汽车用镁合金中的应用。
1、 材料与方法
1.1 材料与方法
汽车用AZ31B镁合金的主要元素化学成分(质量分数,wt.%)为3.08Al、0.86Zn、0.48Mn、0.011Si、0.001Fe、0.001Cu、0.0006Ni,余量为Mg。改性剂为2.0 dl/g的聚三亚甲基碳酸酯-聚乳酸(共聚物P(TMC-DLLA),其中TMC/DLLA=70/30),KH-570硅烷偶联剂(C10H20O5Si)和1,2-双三甲氧基硅基乙烷(BTMSE)硅烷偶联剂(C8H22O6Si2)。
1.2 试样制备
采用线切割的方法加工20 mm×20 mm×4 mm镁合金试样,环氧树脂镶嵌后采用砂纸逐级打磨、金刚石研磨膏抛光、去离子水清洗和无水乙醇超声清洗后吹干备用。采用旋涂法在镁合金试样表面制备了4种改性涂层:(1)不含有机改性硅酸盐涂层,将2.0 dl/g的聚三亚甲基碳酸酯-聚乳酸溶解在四氢呋喃(THF)中,制备成质量分数6%的聚合物溶液,采用旋涂法在均胶机上制备涂层,然后置于48 ℃烘箱中干燥36 h,得到涂层A;(2)有机改性硅酸盐涂层,采用溶胶-凝胶法将x摩尔比的KH-570/BTMSE混合均匀,加入乙酸调节pH至5,加热至42 ℃并搅拌60 min,然后继续升温至75 ℃,搅拌120 min,空冷至室温并静置48 h。在均胶机上采用旋涂法在涂层A试样上制备有机改性硅酸盐涂层(复合涂层),然后置于烘箱中进行48 ℃/15 min+75 ℃/30 min+120 ℃/60 min的热固化处理,得到有机改性硅酸盐涂层,其中x=2∶1、3∶2和4∶1的涂层分别命名为涂层B、涂层C和涂层D。
预先配置3.5% NaCl溶液,分别将经过预处理的镁合金基体和涂层试样置于3.5% NaCl溶液中浸泡,每3 d换一次溶液,浸泡完成后用去离子水清洗和酒精超声清洗,吹干备用。
1.3 测试与表征
采用S-3400型扫描电子显微镜对涂层试样的显微形貌进行观察;极化曲线和电化学阻抗谱测试采用Reference 600型电化学工作站进行测试,测试温度为室温,腐蚀介质为3.5% NaCl溶液,标准三电极体系的工作电极为被测试样、铂片和饱和甘汞分别为辅助电极和参比电极[10],扫描速率为1 mV/s,测试频率为0.01 Hz~100 kHz。
2、 结果与讨论
2.1 不含有机改性硅酸盐涂层
图1为涂层A试样在3.5% NaCl溶液中浸泡不同时间后的显微形貌。浸泡前的涂层表面较为平整致密(图1(a)),未见异常裂纹或者微孔缺陷存在;当浸泡时间为3 d时,涂层表面可见鼓包,局部破裂产生微孔,这可能与浸泡过程中溶液透过涂层与基体接触并产生氢气而聚集在涂层与基体之间有关[11];延长浸泡时间至6 d时,涂层表面可见大面积的剥落,这主要与浸泡时间延长使得气体聚集程度增加并在鼓包处破裂有关[12];当浸泡时间延长至9 d时,剥落的涂层处已经发生明显腐蚀,局部可见腐蚀产物覆盖层。

图1 涂层A试样在3.5% NaCl溶液中浸泡不同时间后的显微形貌
Fig.1 Microscopic morphology of coating A sample soaked in 3.5% NaCl for different times
图2为镁合金基体和浸泡不同时间后涂层A的极化曲线,浸泡溶液为3.5% NaCl溶液,浸泡时间为1 d、3 d、6 d和9 d,表1中列出了相应的电化学参数。镁合金基体的腐蚀电位(Ecorr)和腐蚀电流密度(Jcorr)分别为-1.61 V和4.29×10-6 A/cm2;浸泡前涂层A试样的腐蚀电位和腐蚀电流密度分别为-1.57 V和3.06×10-8 A/cm2。相较镁合金基体,浸泡前的涂层A试样和浸泡1 d~9 d的涂层试样的腐蚀电位都正移,腐蚀电流密度明显减小。腐蚀电位正向移动表明材料的腐蚀倾向减小,而腐蚀电流密度减小则表明腐蚀速率变小[13-15],可见涂层A的耐腐蚀性能明显优于镁合金基体;随着浸泡时间延长,涂层A试样的腐蚀电流密度逐渐增大,浸泡9 d后的腐蚀电流密度仍然小于镁合金基体,表明浸泡0 d~9 d的涂层试样仍然具有优于镁合金基体的耐蚀性。
表1 镁合金基体和浸泡不同时间后涂层A的电化学参数
Tab. 1 Electrochemical parameters of magnesium alloy substrate and coating A after soaking for different times
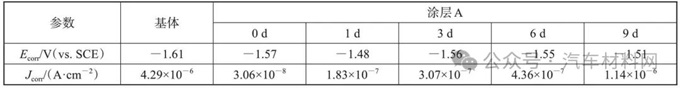
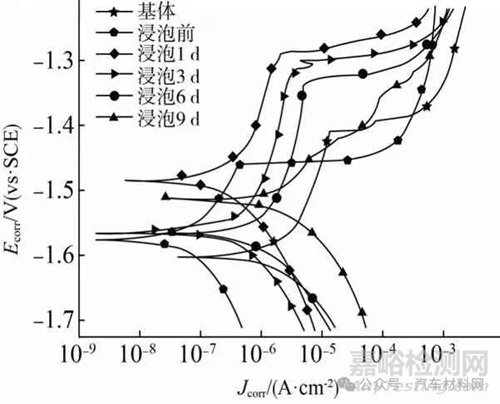
图2 镁合金基体和浸泡不同时间后涂层A试样的极化曲线
Fig.2 Polarization curves of magnesium alloy substrate and coating A sample after soaking for different times
图3为镁合金基体和浸泡不同时间后涂层A的电化学阻抗谱。对比分析可知,涂层A浸泡0 d~9 d试样的容抗弧半径都明显大于镁合金基体试样;对电荷转移电阻的拟合结果可知,镁合金基体试样的电荷转移电阻为3.60×104 Ω/cm2,而涂层A在浸泡0 d~9 d后的电荷转移电阻都高于镁合金基体,且电荷转移电阻从大至小顺序为:0 d>1 d>3 d>6 d>9 d>基体。这主要是因为表面涂层可以抑制电解质溶液对基体材料的腐蚀[16],而随着浸泡时间延长,涂层A的表面发生局部破损,对基体的保护作用减弱[17-18],电荷转移电阻会减小,涂层A试样的耐腐蚀性能降低。电化学阻抗谱的测试结果与极化曲线相吻合。
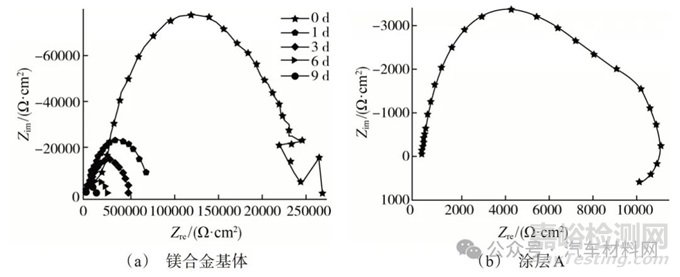
图3 镁合金基体和浸泡不同时间后涂层A的电化学阻抗谱
Fig.3 Electrochemical impedance spectra of magnesium alloy substrate and coating A after soaking for different times
2.2 有机改性硅酸盐涂层
图4为镁合金基体与涂层试样的极化曲线,表2为相应的电化学参数拟合结果。
表2 镁合金基体与涂层试样的电化学参数
Tab.2 Electrochemical parameters of magnesium alloy substrate and coating samples
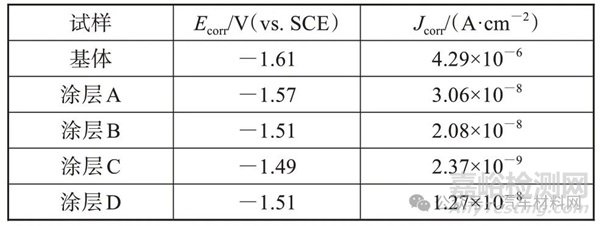
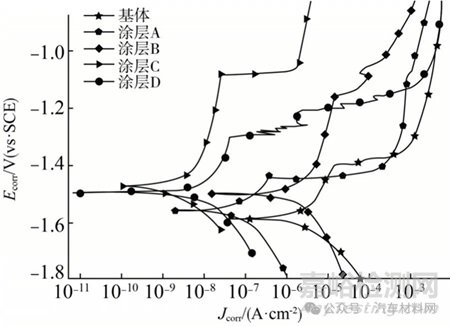
图4 镁合金基体与涂层试样的极化曲线
Fig.4 Polarization curve of magnesium alloy substrate and coating sample
对比分析可知,4种改性涂层的腐蚀电位都相较镁合金基体发生正向移动,且有机改性硅酸盐涂层(涂层B、涂层C和涂层D)的腐蚀电位都相较涂层A更正、腐蚀电流密度相较涂层A更小,腐蚀电流密度从小至大顺序为:涂层C<涂层D<涂层B<涂层A<基体。可见,4种改性涂层的耐腐蚀性能都由于镁合金基体,且耐腐蚀性由高至低顺序为:涂层C>涂层D>涂层B>涂层A>基体。
进一步对4种改性涂层在3.5%NaCl溶液中浸泡不同时间的试样进行电化学性能测试,其中,涂层A试样由于浸泡9 d后发生了较为严重腐蚀,所以只选择浸泡时间1 d~9 d的试样。图5为浸泡不同时间后镁合金表面改性涂层的极化曲线,表3列出了相应的极化曲线拟合结果。
表3 浸泡不同时间后镁合金表面改性涂层的极化曲线的电化学参数拟合结果
Tab.3 Electrochemical parameter fitting results of polarization curves of modified coatings on magnesium alloy surfaces after soaking for different times
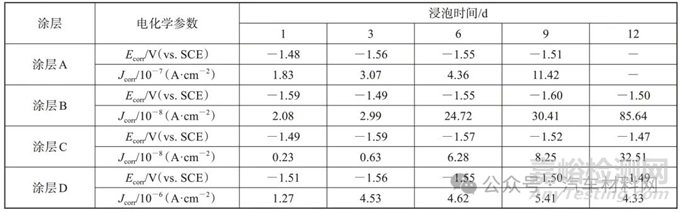
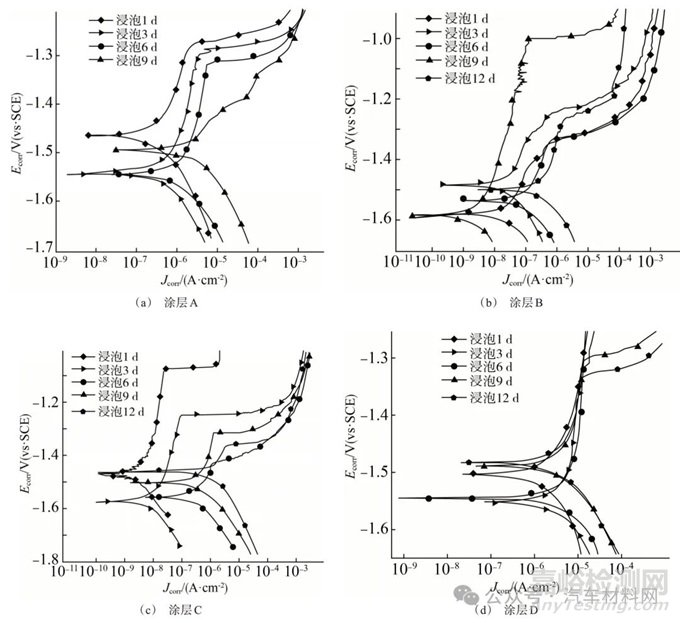
图5 浸泡不同时间后镁合金表面改性涂层的极化曲线
Fig.5 Polarization curve of modified coating on magnesium alloy surface after soaking for different times
对于涂层A试样,随着浸泡时间从1 d延长至9 d,腐蚀电位逐渐负移,腐蚀电流密度逐渐从1.83×10-7 A/cm2增加至11.42×10-7 A/cm2。对于有机改性硅酸盐涂层(涂层B、涂层C和涂层D)试样,随着浸泡时间从1 d延长至9 d,腐蚀电位整体呈现负向移动趋势,腐蚀电流密度增大;在相同浸泡时间下,涂层C的腐蚀电流密度最小,其次为涂层B,而涂层D的腐蚀电流密度最大。由此可见,随着浸泡时间的延长,4种改性涂层的腐蚀电流密度都在增加,耐腐蚀性能降低;但是相同浸泡时间下,涂层B和涂层C的腐蚀倾向相对涂层A更小、腐蚀速率相对涂层A较慢,且涂层C(KH-570/BTMSE=3∶2)具有最佳的耐蚀性能,这主要与涂层中两种前驱的摩尔比较为适宜,有助于基体与涂层形成良好结合,有效的阻挡了电解质溶液的渗透,更为有效保护镁合金基体有关。
表4为镁合金基体与表面涂层的电化学参数,分别列出了镁合金基体、涂层C和相关文献中PLLA涂层和MgZnMn-PLC涂层的腐蚀电位和腐蚀电流密度拟合结果。可见,涂层C以及文献报道的PLLA涂层[19]和MgZnMn-PLC涂层[20]的腐蚀电位都相较镁合金基体正向移动,而腐蚀电流密度都相对较小,且本文制备的涂层C的腐蚀电流密度最小,具有良好的耐腐蚀性能和应用前景,有望在汽车用镁合金的表面改性中应用。
表4 镁合金基体与表面涂层的电化学参数
Tab.4 Electrochemical parameters of magnesium alloy substrate and surface coating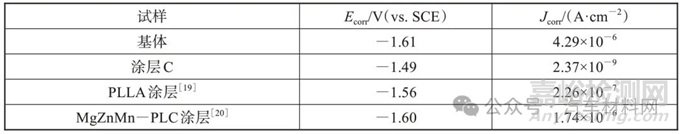
3、结 论
(1)相较镁合金基体,浸泡前的涂层A试样和浸泡1 d~9 d的涂层试样的腐蚀电位都正移,腐蚀电流密度明显减小,可见涂层A的耐腐蚀性能明显优于镁合金基体;随着浸泡时间延长,涂层A试样的腐蚀电流密度逐渐增大,浸泡9 d后的腐蚀电流密度仍然小于镁合金基体,表明浸泡1 d ~9 d的涂层试样仍然具有优于镁合金基体的耐蚀性。
(2)4种改性涂层的腐蚀电位都相较镁合金基体发生正向移动,且有机改性硅酸盐涂层(涂层B、涂层C和涂层D)的腐蚀电位都相较涂层A更正、腐蚀电流密度相较涂层A更小,且腐蚀电流密度从小至大顺序为:涂层C<涂层D<涂层B<涂层A<基体。
(3)随着浸泡时间的延长,4种改性涂层的腐蚀电流密度都在增加,耐腐蚀性能降低;但是相同浸泡时间下,涂层B和涂层C的腐蚀倾向相对涂层A更小、腐蚀速率相对涂层A较慢,且涂层C(KH-570/BTMSE=3∶2)具有最佳的耐蚀性能。
(4)本文制备的涂层C在防腐性能上优于文献报道的PLLA涂层和MgZnMn-PLC涂层
来源:期刊-《电镀与精饰》作者:钟志坚1*,刘 超2,李 畅3
(1.清远职业技术学院,广东 清远 511510;2.广东工业大学 材料与能源学院,广东 广州 510006;3.华南理工大学 材料科学与工程学院,广东 广州 510006)

来源:Internet


