您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-09-28 09:46
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
信达利妥昔单抗即将获批上市。信达与礼来共同开发的利妥昔单抗(IBI301)上市申请进入“在审批”阶段,有望近期获批上市,成为继复宏汉霖之后该品种国内第二家获批的生物类似药。利妥昔单抗是一款CD20靶向单抗,原研为罗氏的重磅药物美罗华,目前已获批的适应症包括非霍奇金淋巴瘤、慢性淋巴细胞白血病和类风湿性关节炎等,2019年销售额为64.77亿瑞士法郎。美罗华已于2008年获批进入中国,后经谈判进入国家医保。
国内药讯
1.昂科免疫CD24Fc新冠肺炎Ⅲ期研究结果积极。昂科免疫公司(OncoImmune)免疫调节剂SACCOVID (CD24Fc)治疗COVID-19重症和危重症患者的Ⅲ期临床SAC-COVID获积极结果。中期分析结果显示,CD24Fc联合标准护理治疗的患者比接受安慰剂+标准护理治疗的患者有多60%的机会实现临床康复(P=0.005);两个治疗组患者康复的中位时间分别为6天和10天CD24Fc联合标准护理将死亡或呼吸衰竭的风险降低了50%以上。
2.纽福斯眼科基因疗法获FDA孤儿药资格。纽福斯生物全资子公司Neurophth基于重组腺相关病毒的基因疗法NR082(NFS-01)获FDA孤儿药资格,用于治疗ND4突变引起的Leber’s遗传性视神经病变(LHON)。在一项9例ND4突变LHON患者参与的临床试验中,NR082使7例患者的视力得到明显改善,最佳视力恢复到0.8,9例患者平均最佳矫正视力提高0.39logMAR(即接近字母表四行的提高)。8例患者完成了近8年的长期随访,无严重不良反应事件。研究成果已发表于2020年的《眼科学》杂志上。
3.埃格林医药EG-009在美获批COVID-19 Ⅰ期临床。FDA在CTAP(加速批准计划)程序下批准埃格林医药口服胶囊EG-009用于治疗COVID-19的Ⅰ期临床试验申请。EG-009主要开发用于预防和治疗COVID-19引起的细胞因子风暴。目前对COVID-19的研究表明,重症患者之所以出现急性呼吸窘迫综合征等严重症状,除了病毒在组织中的增殖以外,人体免疫系统的过激反应导致的“细胞因子风暴”也是让患者病情加剧的重要因素。
4.GSK反义寡核苷酸乙肝药物首次在华获批临床。葛兰素史克(GSK)1类新药GSK3228836注射液获得一项临床试验默示许可,适应症为“慢性乙型肝炎”。GSK3228836是一款反义寡核苷酸(ASOs)药物,在全球范围内已进入Ⅱ期临床开发阶段。本次是该药首次在中国获批临床。一项公布在EASL2020年会上的Ⅱa期临床结果显示,在核苷酸类似物(NA)经治和NA初治的患者组中,300 mg GSK3228836治疗都能将患者的乙肝表面抗原水平降低,两组这一指标分别降低2.51 log10和1.56 log10。
5.百济神州Bcl-2抑制剂在中国申报临床。百济神州1类新药BGB-11417薄膜包衣片的临床试验申请获CDE受理。这是一款 “best-in-class”Bcl-2抑制剂,此次为该产品首次在中国申报临床。根据百济神州公开资料,该公司计划将BGB-11417作为单药以及联合BTK抑制剂泽布替尼进行开发。目前BGB-11417正在澳大利亚进行一项针对成熟B细胞恶性肿瘤患者的Ⅰa /Ⅰb期开放标签、剂量递增和扩展研究。
国际药讯
1.吉利德口服JAK1抑制剂在欧盟和日本同日获批。欧盟委员会批准吉利德与Galapagos联合开发的口服JAK1抑制剂Jyseleca(filgotinib)上市,用于单药或与甲氨蝶呤(MTX)联用,治疗对一种或多种疾病修饰性抗风湿药物反应不良或不耐受的中重度活动性类风湿性关节炎(RA)成年患者。吉利德和卫材同日也宣布日本厚生劳动省批准了Jyseleca上市。欧盟的批准是基于Ⅲ期临床FINCH和Ⅱ期临床DARWIN的数据支持。
2.阿斯利康/第一三共Enhertu首次获批治疗HER2阳性胃癌。日本厚生劳动省批准第一三共与阿斯利康联合开发的HER2靶向抗体偶联药物Enhertu扩展适应症,用于治疗化疗后疾病进展的HER2阳性无法切除的晚期胃癌患者。在一项Ⅱ期临床DESTINY-Gastric01中,Enhertu治疗组达到51.3%的客观缓解率(95% CI:41.9-60.5),化疗组为14.3%(95 CI:6.4-26.2);Enhertu将死亡风险降低了41%(p=0.0097),两组中位总生存期分别为12.5个月和8.4个月。这是Enhertu在全球范围内首次获批治疗HER2阳性胃癌。
3.百时美施贵宝PD-1辅助治疗Ⅲ期临床达终点。百时美施贵宝(BMS)宣布其重磅PD-1抑制剂Opdivo(nivolumab)在辅助治疗复发风险高的肌层浸润性尿路上皮癌患者的关键性Ⅲ期临床CheckMate-274中达主要终点。患者在根治性手术前接受了新辅助化疗治疗,试验结果表明,在意向治疗患者群,以及肿瘤PD-L1≥1%的患者亚群中,Opdivo都显著提高患者的无疾病生存期。目前该试验仍在进行中。分析数据将提交给监管部门,并于医学会议上公布。
4.两款药物获FDA授予罕见儿科疾病资格。FDA对两家公司旗下药物授予了罕见儿科疾病资格认定。一款是Spirovant Sciences公司用于治疗囊性纤维化(CF)的吸入性腺相关病毒(AAV)基因疗法SPIRO-2101,SPIRO-2101同时还获得了治疗CF的孤儿药称号;另一款是Mereo BioPharma用于治疗成骨不全(OI)的抗体药物setrusumab。该药物在美国和欧洲都获得了治疗OI的孤儿药称号,并被纳入EMA的适应途径计划和EMA的优先药物(PRIME)计划。
5.强生公布新冠疫苗JNJ-78436735Ⅰ/Ⅱa期临床结果。强生(Johnson & Johnson)新冠疫苗JNJ-78436735(Ad26.COV2.S)的Ⅰ/Ⅱa期临床结果公布在预印本网站medRxiv上。1次接种疫苗29天后,成人组(队列1a)和老年组(队列3)出现中和抗体血清转化的受试者比例分别为92%和11/12,队列1a中受试者中和抗体滴度超过100的比例分别为82%(5E10组)和94%(1E11组);两个队列大多数受试者可检测到Th1型CD4阳性T细胞反应,两队列均检测到S蛋白特异性CD8阳性T细胞反应;Ad26.COV2.S具良好的安全性和耐受性,老年人全身性不良事件发生率(36%)可能少于成年人。
6.NIH启动“ACTIV-4抗血栓药物”治疗COVID-19患者试验。美国国立卫生研究院(NIH)启动一项Ⅲ期临床“ACTIV-4抗血栓药物”研究。该项研究包括3项试验,将评估肝素与其它抗凝血药物用于治疗住院的COVID-19患者、无需住院的COVID-19患者,以及已出院的COVID-19患者的效果。住院患者将接受低剂量或高剂量的仿制药肝素,用于预防或减少血凝块形成;非住院患者将服用安慰剂、阿司匹林或低剂量阿哌沙班,评估这些药物减少可能致命的心脏或肺部疾病的疗效。出院的患者将检测尚未具体指定的抗凝血药,用于降低心脏病、卒中或其它并发症的风险。
医药热点
1.北京出台突发公卫事件应急条例。北京市表决通过了《北京市突发公共卫生事件应急条例》,规范了应对突发公卫事件的指挥处置、应急准备、监测预警、应急处置、应急保障、法律责任等。监测预警方面,《条例》明确,市、区人民政府应建立健全突发公卫事件监测预警系统,完善报告系统。执行职务的医卫人员发现发生或者可能发生事件线索的,应当依法向本单位和疾控机构报告。情况紧急时可以越级报告。任何人有权报告突发公共卫生事件隐患。
2.深圳先进院成立心血管健康联合实验室。日前,由广东省心血管病研究所、中国科学院深圳先进技术研究院(简称“深圳先进院”)、广东省介入性心脏病学会、澳门大湾区心脏研究学会联合组建的心血管健康联合实验室,在深圳先进院正式成立。该联合实验室旨在心血管疾病智能分析、慢病管理、医疗大数据、新型医疗仪器等领域建立长期合作平台,打造大湾区粤港澳区域级平台载体,共同推进心脏血管疾病领域的研究等。
3.青岛完成核酸检测近14万份,结果均为阴性。针对山东港口青岛港在对登临国际航行船舶作业人员和从事冷链物流进口作业人员进行定期例行核酸检测中发现2名装卸工人感染新冠病毒事件,青岛市已对151089名一般接触者、社区排查人群及相关从业人员开展核酸检测,已完成核酸检测139658份,结果全部为阴性。此外,青岛市采集冷链产品和环境样本26589份,已完成核酸检测21271份,仅在2名装卸工人装卸过的进口冷链产品中检出阳性样本51份。这批进口产品尚未进入市场,已被全部封存。
股市资讯
【复星医药】RT002获批III期临床试验(中重度眉间纹,颈部肌张力障碍)
【ST天圣】获得注射用盐酸头孢吡肟《药品注册证书》
【福安药业】巴氯芬片一致性评价受理(多发性硬化症)
审评动向
1. CDE最新受理情况(09月27日)
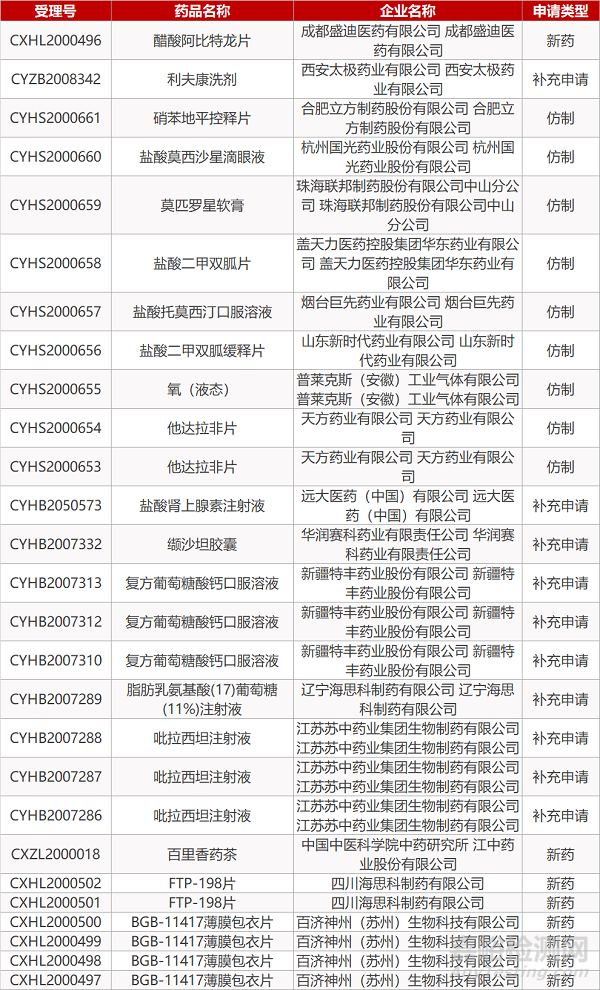
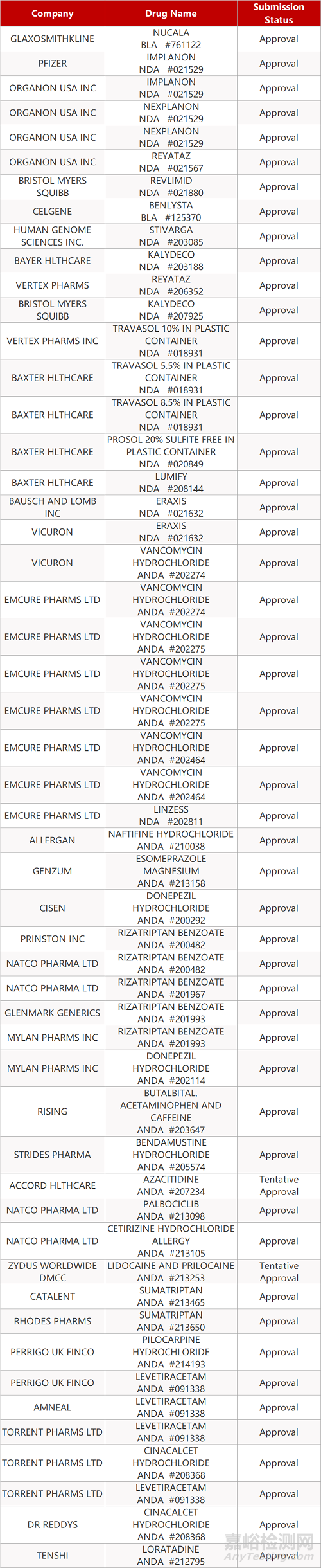
- The End -

来源:Internet


