2022.12.9,FDA发布“医疗器械上市前递交材料中人为因素信息的内容”的指南草案,以修订2016年发布的“人为因素审查最高优先级器械清单”指南草案。


该草案征求意见截止日期为2023.3.9。
该指南草案提供了一个基于风险的框架,以指导制造商和FDA工作人员关于人为因素的信息,这些信息应包括在上市前递交文档中,以提高FDA审查过程的效率。
【草案背景】
医疗器械的一个独特方面是器械-用户界面交互对其安全使用的关键作用。
在设备开发过程中,制造商通常会对人机界面进行人为因素评估。
2016年2月3日,FDA在《联邦公报》中公布了“人为因素审查最高优先级器械清单”指南草案。在考虑了利益相关方对2016年2月3日发布的指南草案的反馈后,FDA发布了一份修订版指南草案,现标题改为“医疗器械上市申请中人为因素信息的内容”。该指南草案提供了FDA关于提交人为因素信息的基于风险的政策,用于上市前审查,以回应利益相关者的反馈。
定稿后,该指南草案将用于补充FDA指南“将人为因素和可用性工程应用于医疗器械(以下简称为“人为因素指南”)。最终定稿后,FDA打算同时修订“人为因素指南”,主要修订包括如下四点:
1. 将“人为因素指南”第3节中的定义替换为本指南中包含的定义;
2. 修订“人为因素指南”第9节“文件”;
3. 将“人为因素指南”附录A“人为因素和可用性工程报告”替换为本指南第五节的交叉引用;
4. 酌情对“人为因素指南”进行任何其他修订。
FDA认识到并预计该机构和行业可能需要多达60天的时间来开展活动,以实施本指南中的政策。如果在最终指南发布前或发布后60天内,FDA收到的上市申请中没有关于上市申请中人为因素信息内容的新信息,CDRH工作人员一般不打算在审查申请时要求提供此类信息。然而,如果收到任何此类信息,CDRH确实打算进行审查。
FDA认识到并预计FDA和行业可能需要多达60天的时间来开展活动,以实施本指南中的政策。
如果在最终指南发布后60天内,FDA收到的上市申请中没有关于上市申请中人为因素信息内容的新信息,CDRH工作人员一般不打算在审查申请时要求提供此类信息。然而,如果收到任何此类信息,CDRH确实打算进行审查。
【人为因素评估的目标】
确保器械用户界面的设计能够消除或尽可能减少器械使用过程中可能导致伤害或降低医疗质量的使用错误。
在基于风险的人为因素评估方法中需要考虑的主要因素,包括识别已有或修改的关键任务,以及消除或减少与使用相关的危险。
【FDA目前对可用性信息的审核】
FDA关于器械上市前递交的决策是基于适用的法定和监管标准的安全性和有效性的合理保证。就相关程度而言,人为因素仅构成FDA评估的组成部分之一。
虽然FDA认为最大限度地降低使用相关的风险是最理想的,但消除所有使用相关的器械风险可能是不必要的,也是不实际的。
在适当的情况下,上市前递交信息应证明在器械设计中考虑了预期用户的需求,并且器械对于预期用户、用途和使用环境是安全有效的。
因此,在适当的情况下,上市任务应包括解释关键任务存在与否的信息、风险缓解策略的验证测试以及剩余风险的描述。包括适当的人为因素信息可以通过减少对AI问题来提高FDA审查的效率。
【适用范围】
本指南旨在帮助提交者和FDA工作人员确定哪些人为因素评估信息应包含在医疗器械的上市申请中,包括510(k)s、De Novo、PMA和HDE申请。
【可用性递交类别】
将人为因素工程信息包括在上市前递交文件中的目的是,通过证明器械的用户界面适合预期用户、用途和使用环境,帮助制造商满足适用的法律标准。
本草案中使用流程图、表格和文本来指导提交者通过基于风险的方法推荐提交者应在其上市前递交中包括哪些人为因素工程信息。FDA将这种基于风险的方法称为人为因素(HF)递交类别。提交者应使用图1中的流程图,并使用其配套文本来回答每个决策点提出的问题。确定哪种HF递交类别适合支持其上市前递交。
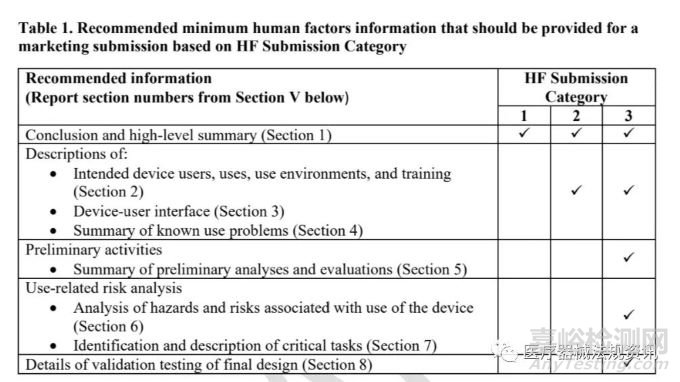
该流程图基于新器械和FDA已授予上市许可的器械的使用适应症和使用相关风险分析。FDA基于关键任务的存在或修改进行HF递交分类,考虑技术特征或使用说明的变化,如果相关。提交人应使用下述使用相关风险分析和决策点来帮助确定其上市提交的HF提交分类。提交者在使用图1确定其递交属于哪一类HF递交后,还应参考表1提交FDA推荐的人为因素工程信息。
通过上图的流程,可将人为因素(HF)递交类别分为:
• HF Submission Category 1
可用性递交类别1
• HF Submission Category 2
可用性递交类别2
• HF Submission Category 3
可用性递交类别3
【可用性递交信息】
• 对于HF递交类别1:提供HF评估的结论和高级摘要:
提交的文件应包括一份声明,证明器械的修改不会影响修改器械的人为因素考虑,并利用(如果适用)先前的人为因素工程评估来提供结论和高级摘要。对于属于HF提交类别1的器械,建议提交内容见表1。
• 对于HF提交类别2:提交理由:没有关键的任务(仅限新器械);或者没有引入新的关键任务和/或没有影响关键任务的变化(仅限于修改后的器械):
提交人应提交一份理由,清楚地描述他们却确定新器械没有关键任务,或修改后的器械没有影响关键任务的依据。这个基本原理应该基于第四节中提到的决策。关于属于HF提交类别2的器械的建议提交内容,请参见表1。
• 对于HF递交类别3:提供一份人因工程报告,包括验证测试,解决:
* 关键任务(仅限新器械;见表2);或
* 新的关键任务引入或现有的关键任务受变更影响(仅修改器械;见表3):
应在HF提交类别3中向FDA提交一份全面的人为因素工程报告,该报告包括本指南第IV节中描述的人为因素工程报告的所有要素。请注意,如果关键任务受到改良器械的影响,但现有的风险控制措施仍然可以接受,应在提交中提供理由,作为人为因素信息的一部分。

【人为因素信息的建议内容】
上市前递交制造商的风险管理、人为因素工程测试(如适用)和设计优化过程的内部文件有助于提供证据,在适当的情况下,证明在设计中考虑了预期用户的需求,且器械对于预期用户、用途和使用环境是安全有效的。
FDA建议人为因素信息应由制造商保存,不管是否提交给FDA。制造商必须在适用法律要求的范围内保存记录。
人为因素工程信息应总结所执行的评估。这种信息通常不包括来自人为因素确认测试的所有原始数据。
作为人因工程过程一部分的文件或分析应包含在上市前提交中提供的人因工程信息中。这包括风险分析,侧重于用户与器械的交互和特定的风险分析、过程、结果和结论。
人为因素工程信息的推荐结构如下:
• 第1部分: 结论和高级总结
提交者应该从结论开始,说明器械的用户界面是否被认为是为预期用户、用途和使用环境充分设计的,以及是否进行了新的人为因素测试来支持这一结论。FDA建议提交者从人因工程评估(例如,使用相关风险)的高级摘要开始,包括进行评估的基本原理,以及进行的人因工程过程的摘要(例如,人因工程分析和评估,器械-用户界面修改和验证测试)和结果的分析。适用时,本节应讨论人为因素确认试验后任何剩余的使用相关风险。提交者应说明为什么进一步降低风险不可行,这是基于对器械的效益风险分析。
• 第2部分:目标器械用户、用途、使用环境和培训的描述
应包括:
1. 目标用户群的描述
如果有一个以上不同的用户群体,应描述每个群体。描述应包括用户群之间在能力或使用责任方面有意义的差异,这些差异可能会影响他们与器械的交互。这包括可能使用同一器械执行不同任务的外行和医疗保健专业用户,或者可能在器械上执行不同任务的不同类型的专业人员。
2. 器械预期用途的概述
3. 器械使用的操作环境和设备操作的关键方面的总结,包括:
* 在使用器械之前,用户是否应该或必须接受医疗专业人员的培训
* 如何在临床应用中使用该器械
* 设置、维护、清理和再处理信息
4. 预期使用环境(例如医院、医疗救护车、家用)以及可能影响用户与设备交互的环境特征(例如强光、振动、环境噪音、高水平活动)的概述
5. 用户将接受的任何培训的描述
可以附上培训材料的样品,如视频、演示幻灯片或小册子。
• 第3部分:设备-用户界面的描述
如果适用,应包括:
1. 器械及其用户界面的图形表示(如照片、插图、线条画)
这应描述整个器械和用户将与之交互的用户界面的所有组件(例如,显示和功能屏幕、报警扬声器、控制装置、键盘、专用按钮、门、要连接的组件、固定夹)。
2. 器械用户界面的书面描述
将随器械提供给用户的标签副本(例如,使用适应症、用户手册、快速入门指南、包装)。
3. 器械操作顺序和用户预期
4. 与用户界面交互的概述
这应包括为使用该器械而执行的用户动作的序列,以及在适当时产生的器械响应;
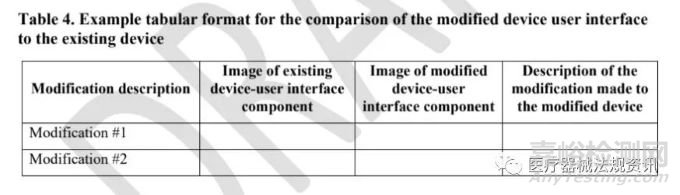
5. 对于改良的器械,考虑提供申请器械和现有器械的比较信息(格式示例见表4)。
•第4部分: 已知使用问题概述
应描述相同器械(如适用)或相似类型器械之前型号的所有已知使用问题。
FDA建议提交者声明没有已知的使用问题,如果适用。对于专门针对现场使用问题进行修改的器械,应讨论这些问题和器械修改。
• 第5部分: 初步分析和评估总结
应确定所使用的初步分析和评估方法(例如,特定的分析技术、形成性评估),总结这些分析和评估的关键结果,描述相应的用户界面设计的修改,并讨论构成人为因素验证试验方案开发的关键发现。
• 第6部分: 与器械使用相关的危险和风险分析
应包括与使用相关的风险分析文件和/或比较任务分析,如适用。这是综合风险分析的典型摘录,包含通过初步分析和评估确定的所有与使用相关的危险和风险,包括与潜在使用错误相关的危险和风险。
使用相关风险分析文件应是一份不断更新的文件;在整个器械设计过程中,应对已识别的风险和危害进行更新。
FDA认为以表格形式组织信息是有用的。表2提供了一个表格格式的例子。本示例提供了评估与您的设备相关的使用相关风险的最低建议信息。对于HF递交类别3中的改装器械,提交者应提供对比任务分析(见表3中的表格格式示例),将改装器械使用相关风险分析与现有器械使用相关风险分析进行比较。如果确定导致任务、相关危害、和/或风险缓解措施修改的器械变更不需要新的HF验证试验数据来支持器械的使用安全性,请提供理由。
• 第7部分:关键任务的识别和描述
1.应解释根据使用相关风险分析文件识别关键任务的过程
由于关键任务是由潜在危险的严重程度决定的,FDA建议提交者描述正在使用的严重程度,并在适当的时候用作参考。例如,如果提交者使用自愿共识标准中的定性五级严重性评级,则应包括一个严重性级别表,描述每个级别并引用适用的标准。
2. 列出并描述关键任务
对于HF提交类别3,如果相关的和合理的任务不需要新的HF验证测试数据来支持器械的使用安全,则提交者应提供单独的表格,突出显示新的关键任务。提交人还应描述人为因素验证测试中包含的每个使用场景,并列出构成每个使用场景的关键和非关键任务。
当修改现有器械时,FDA建议提交者将新器械用户界面与他们自己的现有器械进行比较。FDA建议以表格形式完成这一比较。表格格式示例如表4所示。
除了整个器械的使用相关风险分析文件外,提交者还应包括使用相关风险分析的子集。
FDA建议包括修改过的器械用户界面组件的照片,包括对标签的修改,如手册中的警告声明。
提交者应该列出受修改影响的任何关键任务。提交者还应讨论与修改相关的风险是否可接受,并评估提议的更改是否保证人为因素确认测试。
• 第8部分: 最终设计的HF验证测试的细节
应该总结所有进行的HF验证活动。除了测试结果之外,这一部分还应包含对所有使用错误和问题的综合分析,这些错误和问题可能会导致现实世界使用中的伤害,还应包含针对测试结果对用户界面进行的所有设计修改的描述,以及收益风险讨论。
应附上完整的测试方案和测试中使用的所有脚本和表格的样本。
提交者应提供剩余风险分析和现有缓解控制措施可接受的理由。尽管消除所有剩余风险可能不切实际,但提交者应具备对使用错误和使用相关风险缓解措施进行系统分析的证据。
当确定剩余风险不可接受时,提交者应评估风险控制和缓解措施,以确定降低风险的其他方法。
草案文末提供了3个假设的场景示例
旨在使用图1中的流程图及其配套文字说明FDA基于风险的方法来确定HF递交类别。基于HF递交类别,FDA推荐的支持上市提交的HF信息在每种情况下都有概述。这些例子并没有说明每种递交类型,也没有说明可能适合每种情况的人为因素信息。此外,描述对现有器械进行修改的示例是基于一个假设,即制造商已经决定它需要提交一份新的上市前递交材料。因此,这些示例并不是为了解释何时需要提交新的上市前递交材料。此外,这些示例并不旨在全面代表新器械或现有器械改进的上市子任务中应包含的内容。