您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2022-12-19 11:20
本文中所述的电针治疗仪产品,是指YY0780标准中3.1定义的通过电针给患者进行治疗和辅助治疗的仪器。在《医疗器械分类目录》中分类编码为20中医器械-02中医治疗设备-01穴位电刺激设备,管理类别Ⅱ类。
一.电针治疗仪结构组成和工作原理
1.产品通常包含主机和附件,若产品电源外置还包含外置的电源适配器。从输出形式上,产品可分为单通道和多通道,即一路输出和多路输出。
产品主机通常包含波形(信号)发生单元、信号控制和定时单元、输出幅度提升单元、输出强度调节单元、输出端子以及内部电源(若有)。产品结构示意图见图1。
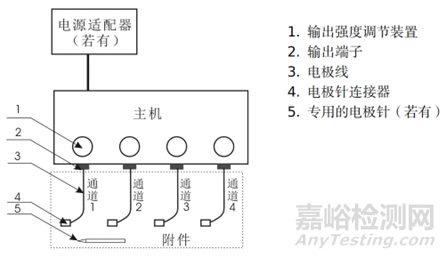
图1 电针治疗仪结构示意图
附件通常为电极线和电极针连接器,其中电极线和电极针连接器也可一体。若产品的电极针为专用针,则附件还包含有电极针。若产品附件不含电极针,还应明确可配用电极针的要求。
2.产品工作原理/作用原理
2.1工作原理
产品从内部功能原理来看,是一台单通道或多通道,带输出幅度调节装置的脉冲信号发生器,产品的功能原理框图见图2。
控制单元是产品的核心,控制单元产生基本的脉冲波形式、控制脉冲的频率和脉冲宽度、控制脉冲的输出模式、控制定时治疗的时间,同时接收保护取样单元反馈的信号,以判断是否出现异常而关断输出,控制单元可控制单一通道也可控制多个通道。
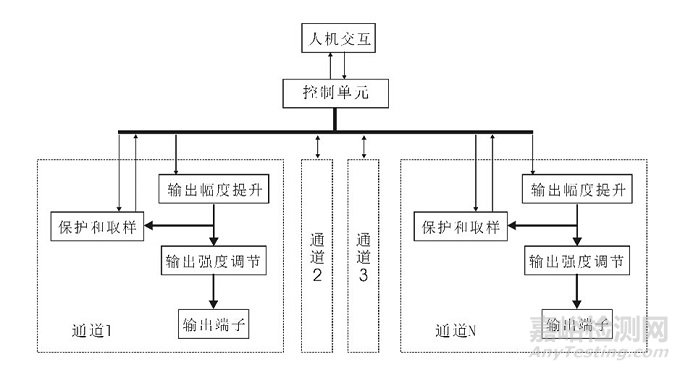
图2 产品的功能原理框图
人机交互单元包含输出端和输入端。输出端,可显示设备的输出状态和工作参数的状态,通常可由显示屏、数码管和指示灯组成。输入端,是对设备进行参数设定或调整以及工作或暂停的控制端,通常可由按键、旋钮和触摸屏组成。
输出幅度提升单元,其作用是将控制单元产生的仅有几伏的脉冲幅度电压提升至几十伏,此单元也可称之为功率放大单元。
输出强度调节单元,其作用是控制输出的强度,可以无级调节输出脉冲的幅度从最小到最大,也可有步长的分段调节。
取样保护电路的作用是获取输出短路、开路或意外输出的异常信号,将其发送给控制单元。
输出端子是主机连接电极线的装置。
产品可以单通道或多通道,各通道间相互独立,功能可相同,通道之间输出参数独立可控。
2.2主要作用机理
电针疗法即针刺穴位获得针感后,在针上通以微量电流,以针刺和电的双重刺激,疏通经络,治疗疾病的一种治疗方法。人体组织是由水、无机盐和带电生物胶体组织组成的复杂的电解体。当一种波形、频率不断变换的电流作用于人体时,组织中的粒子会发生定向运动,消除细胞膜极化状态,使离子浓度和分布发生显著变化,这是电针治疗的电生理基础。
选择不同治疗参数在对不同疾病的治疗或镇痛过程中有着因果关系。脉冲电刺激条件包括五个因素:波形的形态、频率、脉宽、幅度和组合模式。
常用的波形形态如下:(并不限于此二种波形)


有负向反冲的矩形波,负向反冲可视为尖波。
双向矩形波。
常用的脉冲组合模式见图3(并不限于以下模式)。
连续模式是连续按同一频率输出;断续模式是时有时无周期性输出、疏密模式是按两种不同频率周期性输出,除这三种基本模式以外,还有程序模式,程序模式是制造商对产品的输出脉冲按频率、脉宽、幅度等参数进行的周期性或非周期性组合的一种模式。
脉冲幅度与治疗效果直接关联,幅度太小起不到治疗作用,幅度太强则完全没有必要,还会引起患者的不适也存在发生电击伤害的风险[2]。
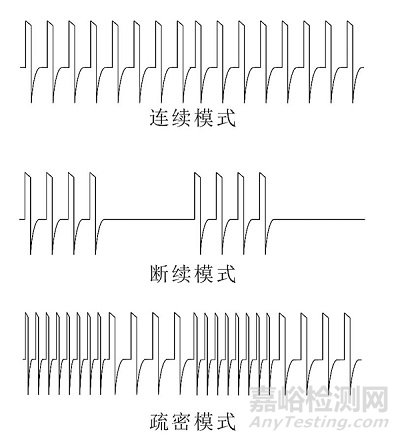
图3 常用的脉冲组合模式
二、电针治疗仪性能研究实验要求
1.化学和物理性能研究
应开展产品化学/材料表征、物理和/或机械性能指标的研究。比如,明确脉冲波形、频率、幅度等参数设计的依据。
如产品与普通针灸针联合使用时,应开展联合使用安全有效的研究。
该产品向患者提供电能,应开展量效关系和能量安全性研究,证明治疗参数设置的安全性、有效性、合理性,以及能量不会对正常组织造成不可接受的伤害。
2.电气系统安全性研究
应开展电气安全性、机械和环境保护以及电磁兼容性的研究。
3.软件研究
软件安全级别应为至少为B级,按照《医疗器械软件注册技术审查指导原则》的要求开展软件研究。
具有网络连接功能进行电子数据交换、远程监测或采用存储媒介以进行电子数据交换产品,应按照《医疗器械网络安全注册技术审查指导原则》的要求开展医疗器械网络安全研究。
4.生物学特性研究
对于与患者直接或间接接触的产品附件,应当按GB/T 16886.1规定的原则进行生物相容性评价。
电极针为短期接触患者组织,如需做生物学评价试验,应对其细胞毒性、致敏、皮内反应进行评价试验。
5.清洁、消毒、灭菌研究
5.1使用者清洁和消毒:应当明确清洗和消毒工艺(方法和参数)并进行相关验证。电极线和电极针连接器建议低水平消毒。
5.2电极针的灭菌研究
5.2.1生产企业灭菌:应明确灭菌工艺(方法和参数)和无菌保证水平(SAL),并开展灭菌验证及确认的相关研究。
5.2.2使用者灭菌:应明确灭菌工艺(方法和参数)并进行相关验证;对可耐受两次或多次灭菌的产品,应开展产品灭菌工艺耐受性的研究。
5.3 残留毒性:如灭菌使用的方法容易出现残留,应当明确残留物信息及采取的处理方法,并开展研究。
6.稳定性研究
6.1有效期
产品主机的有效期参见《有源医疗器械使用期限技术审查指导原则》的相关要求。
无菌有效期验证试验可采用加速稳定性试验和实时稳定性试验,企业需在试验方案中设定检测项目、检测方法及判定标准。产品附件无菌有效期验证可包括以下内容:产品附件原材料/组件、包装材料、生产工艺、灭菌方法、储存运输条件等基本信息,有效期相关影响因素的说明,稳定性试验的试验方案及试验报告等。
鉴于不良事件历史记录中显示电极针的重复使用容易导致断针。开发人应对电极针重复使用次数进行严格限定和充分得研究。对于多次重复使用的电极针,有效期验证除了考虑灭菌影响外,还应考虑电流热效应、使用手法等多重因素的影响。
6.2 使用和运输稳定性
建议按照GB/T14710的规定执行。
医用电器环境要求是评价产品在各种工作环境和模拟贮存、运输环境下的适应性,一般认为属于稳定性评价项目。可以制定不同的气候环境条件和机械环境条件来进行试验,或通过对关键部件的试验来评价整机的情况,也可以通过已上市同类产品比对方式进行判断。
7.一次性使用的医疗器械要求
对于一次性使用的电极针,应开展研究证明其无法重复使用。
三、电针治疗仪主要风险
依据YY/T 0316《医疗器械风险管理对医疗器械的应用》,从各方面列举了电针治疗仪产品的危险(源)分析,见表1。
表1 危险(源)、可预见事件序列、危险情况及伤害示例
|
危险(源) |
可预见的事件序列 |
危险情况 |
伤害 |
|---|---|---|---|
|
电磁能量(线电压) |
电极线无意地插入了网电源插座 |
网电压出现在针上 |
严重烧伤、心脏颤动、死亡 |
|
电磁能量(ESD) |
产品的信号发生和强度控制出现故障 |
产生了高能量的脉冲输出 |
造成电击伤害 |
|
机械能量 |
电极线过粗过硬 |
将针拉偏、拉断,造成与临近的针短路,造成能量意外叠加 |
针刺部位发生变化,造成无效或危险; 造成电击伤害 |
|
电极针连接器夹持力不足 |
电极针连接器脱落触碰其它针或患者身体其它部位 |
造成电击伤害; 治疗无效; |
|
|
化学的(电腐蚀) |
电针仪输出的直流分量使针发生电化学腐蚀 |
发生断针 |
针的断体部分留在患者体内 |
|
功能(不适当输出) |
新电池电压过高或充电后电池电压过高 |
产生了高能量的脉冲输出 |
造成电击伤害 |
|
使用错误 (不遵守规则) |
不适当的操作说明和产品维护保养 |
非专业医生使用;没有使用说明书和技术说明书,或其内容不全。如缺少必要的警告说明、缺少详细的使用方法、缺少必要的技术参数、缺少电路图和元器件清单、缺少运输和贮存环境条件的限制、缺少产品维护保养要求。设备在单一故障状态下运行 |
产生危险;产品损坏 |
|
产品附件(电极针)有效期标识不清晰 |
患者接触到过期有菌产品 |
感染,严重时导致死亡 |
|
|
一次性使用的针被意外的重复使用 |
表面氧化导电性差 |
治疗无效或疗效变差 |
|
|
发生断针 |
针的断体部分留在患者体内 |
||
|
输出短路或开路 |
电针的电刺激变强或者没有 |
造成刺激能量过大或者治疗无效 |
|
|
使用时未将所有输出幅度设定为最小值,输出幅度调节过快过大 |
突然的大能量输出(大脉冲幅度) |
造成刺激能量过大,患者不适,发生电击损伤。甚至引起患者肌肉强烈收缩,引发疼痛、弯针、断针或晕针等意外 |
|
|
不正确的产品贮存条件和产品维护保养。 |
器件老化、部件寿命降低 |
产品寿命降低 |
|
|
功能丧失或变坏 |
电极线老化 |
产品的输出无法加载至针上 |
无效治疗 |
|
电极针连接器老化 |
无法与针可靠导电连接 |

来源:嘉峪检测网


