您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-12-20 09:03
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:15条资讯,阅读时长约:3分钟 」
今日头条
再鼎医药尼拉帕利或将国内获批。再鼎医药1类新药PARP抑制剂尼拉帕利的上市申请审评状态已变更为"在审批",预计将于本月获批上市,适应症为对含铂化疗完全或部分缓解的复发性上皮性卵巢癌、输卵管癌或原发性腹膜卵巢癌成人患者维持治疗。尼拉帕利(则乐)是一种口服小分子聚(ADP-核糖)PARP1/2抑制剂,由TESARO公司开发,再鼎医药拥有其中国市场的独家研发和销售权。尼拉帕利于2017年3月在美国首次获批,同年11月在欧洲获批,用于对含铂化疗完全或部分缓解的复发性上皮卵巢癌、输卵管癌或原发性腹膜癌患者的维持治疗。
国内药讯
1.武田富马酸伏诺拉生片在华获批。武田全新机制抑酸药物沃克® (富马酸伏诺拉生片)获国家药监局批准上市,用于治疗反流性食管炎(RE)。沃克®是首款获批进入中国市场的钾离子竞争性酸阻滞剂(P-CAB),临床数据表明其具有首剂全效,持久抑酸和方便服用等特点。一项481例反流性食管炎患者参与的III临床phase结果显示,研究达到预设的主要终点,且沃克®治疗组的粘膜愈合率高达92.4%,安全性与兰索拉唑组相似。
2.罗欣药业卡托普利片通过一致性评价。罗欣药业卡托普利片(25mg)获国家药监局批准,通过仿制药一致性评价。卡托普利片一致性评价参比制剂由百时美施贵宝公司开发,为首个问世的竞争性血管紧张素转换酶抑制剂品种,通过阻止血管紧张素亚型转化以降低外周血管阻力,用于治疗高血压和心力衰竭,口服后1-1.5小时即可达到体内血药浓度峰值。目前国内已有多家制药企业生产的卡托普利片获批上市,该药属于甲类医保药物。
3.罗欣借壳上市获批。东音股份重大资产置换及发行股份购买资产暨关联交易事项获国家证监会有条件通过。本次重大资产重组拟置入资产为罗欣药业99.65476%的股权。拟置出资产(东音股份)最终作价为9.0亿元,拟置入资产(罗欣药业)的最终作价为75.4亿元,上述差额66.4亿元由上市公司以发行股份的方式向交易对方购买。拟置入资产中价格不足一股部分对应的资产,由交易对方无偿赠与上市公司。本次交易完成后,上市公司的控股股东变更为罗欣控股,其将持有上市公司36.1779%股份。
4.再鼎医药合作抗癌产品在美国提交上市申请。Deciphera公司已向FDA提交其广谱KIT/PDGFRα抑制剂Ripretinib的新药上市申请,用于治疗既往接受过伊马替尼、舒尼替尼和瑞戈非尼治疗的晚期胃肠道间质瘤(GIST)患者。再鼎医药拥有该新药在大中华区的开发和商业化独家授权。一项关键性III期研究INVICTUS结果显示,与安慰剂相比,Ripretinib能够改善四线及四线以上GIST患者的无进展生存期,达主要终点指标。Ripretinib此前已获FDA授予快速审批资格和突破性疗法认定,以及FDA和欧洲EMA授予的治疗GIST的孤儿药资格。
国际药讯
1.FDA加速批准创新安斯泰来ADC上市。Seattle Genetics/安斯泰来Nectin-4靶向抗体偶联药物Padcev(enfortumab vedotin-ejfv)获FDA批准上市,治疗曾接受过铂基化疗和PD-1/PD-L1抑制剂治疗的局部晚期或转移性尿路上皮癌患者。这款疗法曾获FDA授予的突破性疗法认定和优先审评资格。一项125例患者参与的临床结果显示,在已接受过铂基化疗和PD-1/PD-L1抑制剂的治疗患者中,Padcev的总缓解率达到44%,其中完全缓解率为12%,部分缓解率为32%。中位缓解持续时间为7.6个月。
2.首款EZH2抑制剂明年初有望上市。Epizyme公司的“first-in-class”EZH2抑制剂tazemetostat获FDA肿瘤学药物咨询委员会推荐,用于治疗不适合手术治疗的转移性/局部晚期上皮样肉瘤(ES)。Tazemetostat的新药申请已获FDA的优先审评资格,预计明年1月23日之前得到回复。在一项Ⅱ期临床中,24例初治和38例复发/难治性ES患者接受tazemetostat的治疗,截至2018年9月,tazemetosta的客观缓解率为15%,疾病控制率达到26%,中位总生存期尚未达到。
3.Keytruda有望治疗特定高危膀胱癌患者。FDA肿瘤学药物咨询委员会以9:4的投票结果,支持默沙东重磅PD-1抑制剂Keytruda治疗特定高风险非肌肉浸润性膀胱癌(NMIBC)患者。Keytruda治疗高风险NMIBC患者的sBLA已获FDA授予的优先审评资格,预计FDA将在明年1月作出回复。Keytruda目前获批治疗20多项适应症,其中包括治疗晚期或转移性尿路上皮癌患者。一项Ⅱ期临床KEYNOTE-057结果显示,Keytruda在高风险NMIBC患者中的完全缓解率(CR)达到40.2%(n=102)。而且,在完全缓解的患者中,58.5%的患者在中位随访时间达到16.7个月时仍然维持完全缓解。
4.奥拉帕利有望年底获批治疗胰腺癌患者。FDA肿瘤学药物咨询委员会以7:5的投票结果,支持阿斯利康和默沙东联合开发的PARP抑制剂奥拉帕利(olaparib,Lynparza)作为一线维持疗法,治疗携带生殖系BRCA基因突变并在铂基化疗后疾病没有进展的转移性胰腺癌患者。今年8月,FDA已接受奥拉帕利的补充新药申请并授予其优先审评资格,预计年底作出回复。一项Ⅲ期临床POLO结果表明,与安慰剂组相比,奥拉帕利一线维持治疗能够将患者的PFS从3.8个月提高到7.4个月(HR: 0.53, 95% CI, 0.35-0.82, p=0.004);但两组的中位OS的差异不具统计学意义。
5.辉瑞BRAF/EGFR抑制剂组合获优先审评资格。辉瑞宣布,FDA已受理BRAF抑制剂Braftovi(encorafenib)和EGFR抑制剂Erbitux(cetuximab)构成的组合疗法的补充新药申请,用于治疗携带BRAF V600E突变的转移性结直肠癌患者。FDA同时授予其优先审评资格,预计明年4月前作出回复。一项Ⅲ期临床BEACON CRC结果显示,与Erbitux+化疗对照组相比,Braftovi联合Erbitux显著提高患者的总生存期(OS)和客观缓解率(ORR)。Braftovi+Erbitux组中位OS为9.4个月,对照组为5.4个月(p=0.0003)。Braftovi+Erbitux组中位ORR为20%,显著优于对照组的2%(p<0.0001)。
6.GSK红斑狼疮疗法达到Ⅲ期终点。葛兰素史克抗体药物Benlysta(belimumab)在治疗狼疮性肾炎(LN)的Ⅲ期试验BLISS-LN中,达主要终点和所有次要终点。与安慰剂+标准疗法组相比,Benlysta联合标准疗法显著提高达到初级肾脏缓解(PERR)标准的患者比例(43%vs32%,p=0.0311);Benlysta治疗组中的患者还在关键性次要终点中显示出统计学意义上的优势,包括治疗两年后达到完全肾脏缓解(CRR)和序贯肾脏缓解,以及治疗一年后达到PERR的患者比例等。GSK计划明年上半年递交该适应症的监管申请。Benlysta是目前唯一一款获批治疗红斑狼疮的生物制品。
7.礼来启动偏头痛新药Emgality真实世界研究。礼来(Eli Lilly)宣布启动偏头痛新药Emgality (galcanezumab-gnlm)一项代号为TRIUMPH的长期真实世界研究。该研究计划在美国、欧洲、亚洲的多个中心招募大约2850例患者,在2年的时间内跟踪偏头痛预防性治疗的临床处方行为和治疗选择,包括Emgality、其他CGRP抗体药物、口服偏头痛预防药物等药物的转换使用情况和中止治疗情况,评估患者自己报告的偏头痛负担缓解情况、生活质量和总体的治疗满意度,同时评估患者每月偏头痛发作天数的减少情况。galcanezumab去年9月已获批,是全球第3个上市的靶向降钙素基因相关肽(CGRP)单抗类偏头痛新药。
医药热点
1.法国660名医生联名发公开信。据外媒消息,近日,法国各地医院的660名医生在一封公开信中表示,如果法国政府不增加医疗经费,罢工医生将再次在全法各地游行。公开信中指出,医疗预算削减、床位数削减和医务人员短缺使法国的医疗系统濒临崩溃的边缘,也使患者的生命处于危险之中。据了解,2019年3月法国各公立医院急诊部开始罢工,罢工浪潮逐渐扩散到小儿科、精神科等各个科室,12月家庭医生也开始加入。到现在,法国医院罢工已经持续了9个月,不但没有结束,且有愈演愈烈的趋势。
2.跨省异地就医直接结算人次达395万。国家医保局12月18日发布消息称,截至2019年11月底,跨省异地就医定点医疗机构数量为25057家,二级及以下定点医疗机构22233家,国家平台备案人数523万,累计结算人次395万。2019年11月,跨省异地就医定点医疗机构数量新增1487家;二级及以下定点医疗机构新增1448家。当月跨省异地就医直接结算27.9万人次,环比上升17.0%;医疗费用66.0亿元人民币,环比上升20.1%;基金支付39.5亿元,环比上升19.6%,基金支付比例59.8%;日均直接结算9297人次。
3.内蒙古:加强不明原因发热患者的鼠疫排查。内蒙古自治区卫健委近日发布《关于进一步加强医疗机构重点传染病管理工作的通知》。通知要求内蒙古全区各级各类医疗机构要加强门、急诊及发热门诊管理,强化医务人员识别传染病疑似病例的意识和能力。强化医生首诊负责制,首诊医生接诊发热患者时,要注重询问是否来自疫源地,有无接触具有发烧、淋巴结肿大、咳嗽咳痰、痰中带血等症状,对鼠疫疑似患者开展早期排查和识别,疑似和确诊鼠疫病例按照就地、就近原则,转入当地定点医院进行隔离治疗。
股市资讯
【赛隆药业】全资子公司湖南赛隆药业有限公司向国家药监局提交的“阿加曲班注射液”、“注射用胸腺法新”国产药品注册申请处于“审批完毕-待制证”状态,“注射用替加环素”国产药品注册申请处于“制证完毕-待发批件”状态。
【上海医药】公司2019年股票期权激励计划规定的股票期权授予条件已经成就,公司确定股票期权的授予日为2019年12月19日,向符合授予条件的211名激励对象授予2,568万份股票期权,行权价格18.41元/A股。
审评动向
1. CDE最新受理情况(12月19日)
2. FDA最新获批情况(北美12月18日)

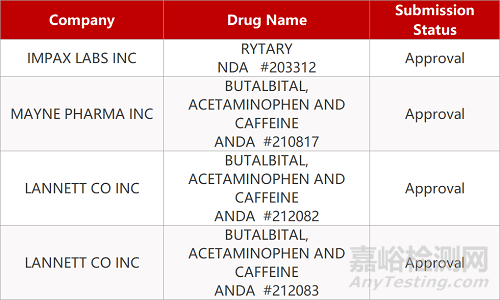

来源:药研发


