您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-05-14 08:55
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:15条资讯,阅读时长约:3分钟 」
今日头条
云顶药业Trop-2 ADC拟纳入优先审评。云顶药业Trop-2 ADC新药注射用戈沙妥组单抗的上市申请获CDE拟纳入优先审评,用于既往接受过至少2种疗法的转移性三阴性乳腺癌成人患者。注射用戈沙妥组单抗是一款“First in class”Trop-2靶向抗体药物偶联物(ADC),已获FDA批准上市(商品名:Trodelvy® ),用于上述适应症。在一项国际III期临床试验ASCENT(NCT02574455)中,Trodelvy与化疗相比,将患者中位总生存期延长至11.8个月(vs6.9个月,p<0.0001),将死亡风险降低了49%。
国内药讯
1.豪森「阿美替尼」新适应症拟纳入优先审评。豪森药业第三代EGFR抑制剂阿美替尼(阿美乐®)新适应症上市申请获CDE拟纳入优先审评,用于一线治疗具有表皮生长因子受体外显子19缺失或外显子21(L858R)置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)。阿美替尼是全球范围内第二款获批的第三代EGFR抑制剂,也是国产首款获批上市的第三代EGFR抑制剂。去年3月,阿美替尼获NMPA批准上市,用于EGFR突变阳性NSCLC的二线治疗。
2.德琪SINE抑制剂获批国际III期临床。德琪医药SINE抑制剂塞利尼索(XPOVIO®)获NMPA临床试验默示许可,即将开展用于治疗晚期或复发性子宫内膜癌的III期临床(SIENDO)。这是一项国际III期临床,正在北美、欧洲及亚洲同步开展。塞利尼索是首款获FDA批准的口服SINE化合物,用于治疗多发性骨髓瘤和弥漫性大B细胞淋巴瘤。德琪医药拥有该新药在亚太地区的开发和推广权益。在中国,塞利尼索的上市申请已获CDE纳入优先审评。
3.百奥赛图CD40单抗在澳洲获批II期临床。百奥赛图集团旗下祐和医药CD40单抗YH003获得澳洲监管机构批准,即将联合君实生物PD-1单抗(特瑞普利单抗)开展II期临床,评估这一组合疗法在胰腺癌和PD1耐药黑色素瘤患者中的疗效和安全性。在多种肿瘤小鼠模型中,无论是单药还是与PD-1单抗联用,YH003均显示出强大的抗肿瘤效果;在小鼠药效学研究中,YH003显著增加了肿瘤浸润细胞中的抗肿瘤T细胞的比例。
4.恒瑞哮喘新药SHR-1905获批临床。恒瑞1类新药SHR-1905注射液获国家药监局临床试验默示许可,拟开发用于治疗哮喘。根据恒瑞已布局该领域专利,推测SHR-1905可能为靶向胸腺基质淋巴细胞生成素(TSLP)的单抗。目前全球范围尚无同靶点抗体获批上市;全球进展最快的同类产品为安进/阿斯利康的Tezepelumab,本月10日,该新药已向FDA提交了生物制剂许可申请(BLA),用于治疗重度哮喘。
5.瑞创RC1012注射液上I期临床。瑞创生物通用型DNT细胞治疗产品RC1012注射液治疗复发/难治急性髓系白血病(AML)的I期临床首例受试者给药。该项研究旨在评估RC1012的安全性和耐受性;确定最大耐受剂量和/或II期临床推荐剂量;药代动力学以及初步疗效,主要研究者由浙江大学医学院附属第一医院血液病骨髓移植中心蔡真教授担任。RC1012是国内首个获批临床的通用型免疫细胞新药。
国际药讯
1.安斯泰来前列腺癌新药在英获批。英国药品和健康产品管理局(MHRA)批准安斯泰来前列腺癌药物Xtandi(enzalutamide,恩扎卢胺)上市,用于治疗转移性激素敏感性前列腺癌(mHSPC)成年男性患者。随着这项批准,Xtandi成为了MHRA批准的唯一一种可治疗3种晚期前列腺癌的口服疗法,包括:高危非转移性和转移性去势抵抗性前列腺癌(nmCRPC,mCRPC)以及mHSPC。Xtandi已成为晚期前列腺癌患者的标准护理疗法。
2.VBI公司新型乙肝疫苗关键性Ⅲ期临床结果积极。VBI Vaccines公司第三代乙肝病毒(HBV)候选疫苗Sci-B-Vac在成人中的关键性Ⅲ期临床数据在The Lancet Infectious Diseases上发表。与20µg单抗原乙肝疫苗相比,10µg三抗原Sci-B-Vac接种后受试者获得的血清保护率(SPR)更高:Sci-B-Vac接种2次(第168天)后的SPR为87.2%,与单抗原疫苗接种3次(第196天)后的SPR相当(91.1%)。而且Sci-B-Vac受试者的抗体几何平均浓度(GMC)是活性对照组的5-8倍。目前,这款新型疫苗正在接受FDA和EMA的审评。
3.强生角膜塑形隐形眼镜在美获批。FDA批准强生旗下Johnson & Johnson Vision公司开发的角膜塑形隐形眼镜ACUVUE Abiliti上市。这是一款针对患者角膜形状个体化设计的治疗近视的隐形眼镜,用于患者晚上睡觉时佩戴以控制近视。在近视儿童中进行的临床研究表明,ACUVUE Abiliti在为期两年的时间里,让近视儿童的眼轴伸长幅度缩小了0.28毫米。ACUVUE Abiliti也是FDA批准的首款用于控制近视的角膜塑形隐形眼镜。
4.Danon病基因疗法RP-A501遭FDA叫停。FDA暂停Rocket公司Danon病基因疗法RP-A501的一项早期试验。Danon病是一种罕见的神经肌肉和心血管疾病,该病将导致认知障碍、心肌病、骨骼肌病,往往需要心脏移植。目前,RP-A501已在早期临床中显示出将一小部分年轻成人患者的心力衰竭指标降低的治疗潜力。FDA要求Rocket将“额外的风险缓解方法”纳入RP-A501临床项目。在去年,1例接受高剂量RP-A501治疗的患者曾出现过免疫反应。
5.渤健购入新型溶栓药。渤健宣布将行使选择权,从TMS公司收购一款拟用于治疗急性缺血性中风(AIS)的小分子纤溶酶原激活剂TMS-007。TMS-007在分解血凝块方面具有潜在的全新作用机制,在一项Ⅱa期临床中达到安全性的主要终点:与安慰剂相比,TMS-007治疗患者的安全性事件发生率为0%(vs3%);而且TMS-007治疗组90天后有40%的患者达到独立生活并且没有明显中风遗留症状或显著残疾的标准,安慰剂组这一数值仅为18%(p<0.05)。
6.渤健联手Capsigen开发新型AAV基因疗法。渤健宣布与Capsigen公司达成一项战略合作,利用Capsigen专利的TRADE™平台和衣壳工程相关技术开发新型AAV衣壳,用于中枢神经系统(CNS)和神经肌肉疾病治疗的基因疗法。根据协议,Capsigen将负责设计和筛选新的AAV衣壳;渤健将享有新型AAV衣壳的独家许可,用于未知数量的中枢神经系统和神经肌肉疾病基因疗法;Capsigen将获得1500万美元的预付款,可能高达12.92亿美元的潜在里程碑付款以及产品的销售分成。
医药热点
1.全国注册护士人数超470万。国家卫健委网站5月11日发布的相关数据显示,2020年年底,全国注册护士总数为470多万,较2015年的324万,增幅达45%。每千人口注册护士数从2015年的2.37增加到2020年的3.35,全国医护比由2015年的1∶1.07提高到1∶1.15,具有大专以上学历的护士超70%,护士队伍学历素质和专业服务能力不断提升。下一步,国家卫生健康委将从4个方面开启护理工作高质量发展新征程。
2.上海推广七大“便捷就医”场景。上海市卫健委牵头于2021年1月组建“便捷就医服务”数字化转型工作专班,目前选择11家市级医疗机构和4个区卫生健康委开展试点,将于6月底完成此项工作,实现7个“便捷就医”重点推广场景,包括精准预约、智能预问诊、互联互通互认、医疗付费“一件事”、电子病历卡、查询核酸检测、智慧急救上车即入院。除了智慧急救上车即入院外,其他6个场景将于今年年底实现全市全覆盖。
3.印度第二代新冠突变株急速蔓延。世卫组织5月10日将印度发现的新冠突变株B.1.617上升为重点关注的突变株(VOC)。Fred Hutch研究所日前公布的一组数据显示,第二代突变株B.1.617.2在印度正以0.59的速度极速上升(而B.1.617、B.1.617.1和B.1.617.3比例都在下降),目前在所检测样本中已接近60%。值得一提的是,上周英国报道了B.1.617.2导致15位接种阿斯利康疫苗的老人出现了突破感染。
审评动向
1. CDE新药受理情况(05月13日)
申请临床:
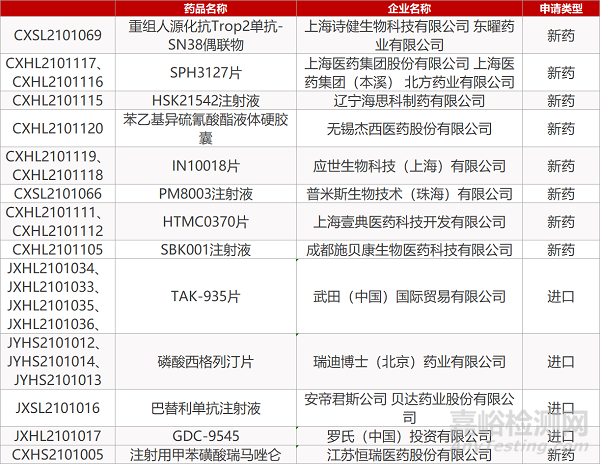
上海诗健/东曜药业的重组人源化抗Trop、上海医药的SPH3127片(2个规格)、辽宁海思科的HSK21542注射液、无锡杰西的苯乙基异硫氰酸酯液体硬胶囊、应世生物的IN10018片(2个规格)、普米斯生物的PM8003注射液、上海壹典的HTMC0370片(2个规格)、成都施贝康的SBK001注射液、武田的TAK-935片(4个规格)、安帝君斯公司/贝达药业的巴替利单抗注射液、罗氏的GDC-9545。
申请生产:
江苏恒瑞的注射用甲苯磺酸瑞马唑仑、瑞迪博士的磷酸西格列汀片(3个规格)。
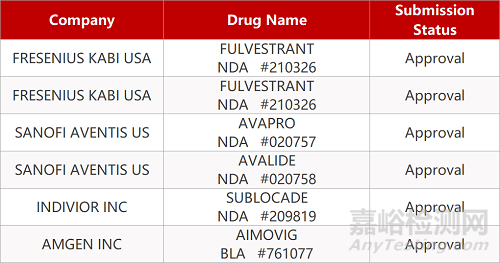
2. FDA新药获批情况(北美05月12日)

来源:药研发


