您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-14 23:11
引 子
“听说做制剂的做饭都不错”
对啊!确实如此!对于我们摇粉青年来说,so easy.......
主药就是主菜;
辅料就是配菜和佐料;
选好加工方法煎(粉末直压)、炒(干法)、炖(湿法)、炸.......
控制好温度、时长等“参数”。
出锅!
对于摇粉青年来说,普通菜已经拦不住我们的脚步~~~
多做研究那不是我们基本的"职业道德"么?
所以,你有没有因为放错一种"辅料"而毁掉一锅菜。
本文从三个部分阐述了原辅料相容性的内容:
1.各国对原辅料相容性研究的要求
2.常见原辅料不相容情形
3.原辅料相容性筛选试验
一、各国对原辅料相容性研究的要求
做处方不像做饭那样,没有严格的规定,大家可以随意的做一些搭配,不好大不了下次不做了,出现问题的可能性很小。但是,做处方却关系到了人的生命,我们总是要慎之又慎,避免一些出现问题的环节,而针对这些各国也对原辅料相容性做了一些要求,下面我们就一起看一下各国的要求。
1.中国
在《化学药物制剂研究基本技术指导原则》中有明确的要求(第6页),具体内容如下:
(一) 原料药
1.相容性研究
本相容性研究指药物与辅料间及药物与药物间相互作用研究。前者将在下面辅料部分进行阐述。后者主要是复方制剂研究中需要考虑的问题,实验可参照药物稳定性指导原则中影响因素的试验方法进行。
(二) 辅料
相容性研究药物与辅料相容性研究为处方中辅料的选择提供了有益的信息和参考。药品申请人可以通过前期调研,了解辅料与辅料间、辅料与药物间相互作用情况,以避免处方设计时选择不宜的辅料。
对于缺乏相关研究数据的,可考虑进行相容性研究。例如口服固体制剂,可选若干种辅料,若辅料用量较大的(如稀释剂等),可按主药:辅料=1:5的比例混合,若用量较小的(如润滑剂等),可按主药:辅料=20:1的比例混合,取一定量,参照药物稳定性指导原则中影响因素的实验方法或其他适宜的实验方法,重点考察性状、含量、有关物质等等,必要时,可用原料药和辅料分别做平行对照实验,以判别是原料药本身的变化还是辅料的影响。
如处方中使用了与药物有相互作用的辅料,需要用实验数据证明处方的合理性。
2.ICH
在ICH 药品研发Q8(R2)2.1.2 Excipients部分中也有明确要求(第3页),具体内容如下:
2.1.2 辅料
申报者应针对各种辅料的作用,详述其选择过程,配比以及可能影响的药物制剂性能(如稳定性、生物利用度)或可生产性。处方中应包括药物制剂生产中所用到的所有物质,不论其是否出现在成品中(如:工艺辅助剂)。必要时,应建立辅料之间的相容性(比如双重防腐系统中防腐剂的组合)。同时,应阐述辅料(如抗氧剂、渗透促进剂、崩解剂、控释剂)是否能实现预期的作用,是否能在预期的有效期内发挥作用。可能的情况下,可以利用有关辅料性能的资料,来论证辅料的选择和质量属性,并支持证明药物制剂质量标准的合理性(3.2.P.5.6)。
有关辅料安全性方面的资料,可以被交叉引用(3.2.P.4.6)。
3.美国
虽未搜索到FDA相关的法规性文件中有对原辅料相容性研究的硬性要求,但在FDA<Chemistry Review of Question-based Review (QbR) Submissions>和FDA发布的药物研发QbD实例模板中具有相关体现。具体信息如下:
3.1 Chemistry Review of QbR Submissions
ATTACHMENT2: QbR QUESTIONS - DRUG PRODUCT (CHEMISTRY)What evidence supports excipient-drug substance compatibility and if applicable, excipient-excipient compatibility?
3.2 QbD for ANDAs: Example for IR
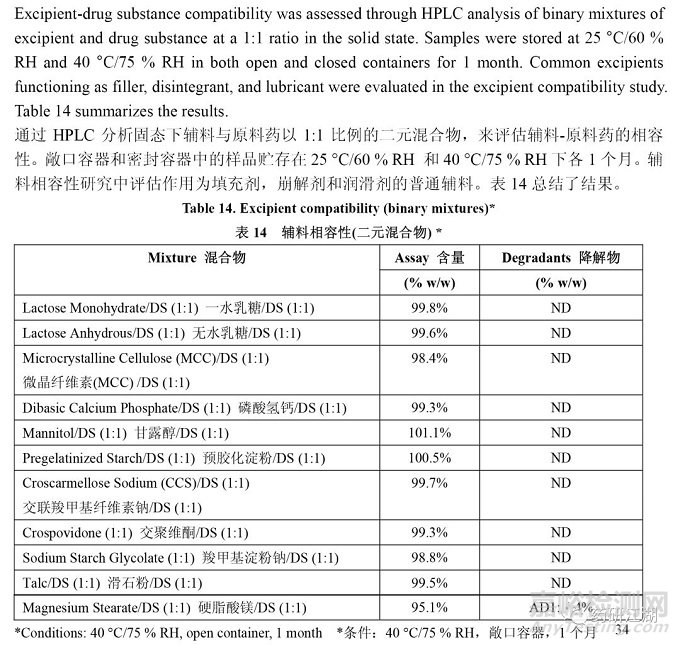
图片来源:Quality by Design for ANDAs: An Example for Immediate-Release Dosage Forms,FDA,2012.
3.3 QbD for ANDAs: An Example for MR
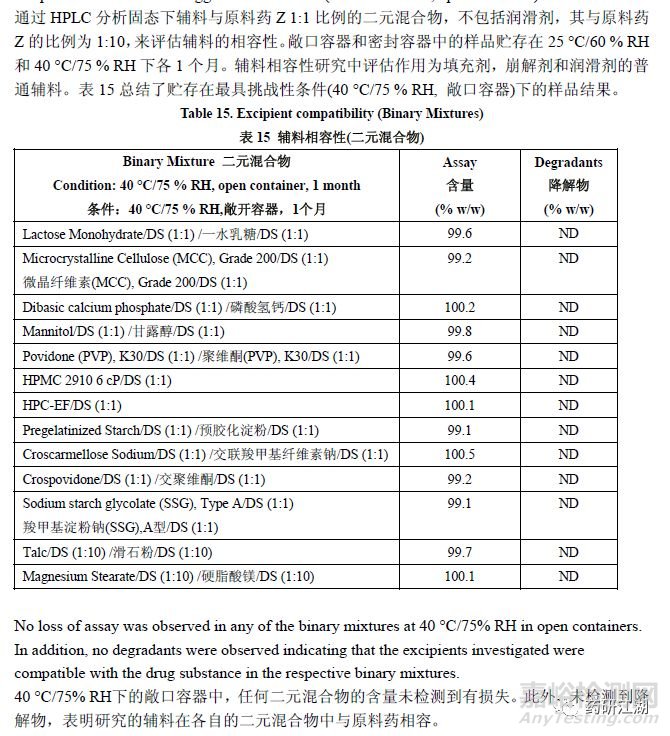
图片来源:Quality by Design for ANDAs: An Example for Modified-Release Dosage Forms,FDA,2012.
通过检索的信息发现,只有中国对原辅料相容性试验操作进行了较为详细的描述,而ICH、FDA虽有对原辅料相容性部分的研究有要求,但并未给出统一的规定。而原辅料相容性研究是制剂产品研发开始阶段不可或缺的一环,不仅有利于快速高效选择适宜于产品处方的合适药用辅料,而且还对产品的关键质量特性(critical quality attributes,CQA)和质量控制策略的制定具有指导意义。
二、常见原辅料不相容情形
不像做菜那样,不太合适的搭配显而易见,做药物研发的处方研究过程中的原辅料不相容的情况就不太容易判断了,不过这里小编搜集整理了部分原辅料不相容的情形
药用辅料本身不具备有效性,但可以形成有利于药物保持质量稳定的制剂微环境。按照原料与药用辅料的相互作用,原辅料不相容的情况大体可分为物理不相容、化学不相容、生物不相容。
2.1物理不相容
2.1.1物理吸附
吸附作用是常见的原辅料物理不相容的原因。在产品制备过程中,药物可通过范德华力或静电吸附作用附着在辅料表面,若吸附作用过强,药物不能较好的从辅料表面解吸附,表现为药物不能很好的分散和释放。
经典案例
抗菌药西吡氯铵与硬脂酸镁配伍使用导致其生物利用度降低。在产品制备过程中,硬脂酸镁作为润滑剂使用,硬脂酸镁的硬脂酸阴离子与药物阳离子静电吸附但药物难以解吸附,导致西吡氯铵的抗菌活性下降。
2.1.2包埋
药物小分子通过物理力与辅料表面大分子结合,可得到药物分布均匀的混合物,是改善难溶性药物溶出的有效手段之一。预胶化淀粉具有较好的膨胀系数,可显著提高难溶性药物(如塞来昔布)的溶出速度。但当其凝胶化速度大于膨胀速度时,药物将会被包埋其中而延迟释放从而导致药物的体内生物利用度降低。
2.1.3低共熔作用
处方中两种或两种以上组分在制备过程中出现润湿或液化现象。如非那西丁与咖啡因,对乙酰氨基酚与阿司匹林都会产生低共熔物导致复方对乙酰氨基酚片粘冲严重。颗粒中药物熔融,不仅引起外观物理变化,而且会出现崩解不合格、粘冲等各种质量问题。冰片与薄荷脑在一定比例下常温研磨可以形成二元低共熔混合物,能显著促进药物透皮吸收,并且冰片-薄荷脑二元低共熔混合物在常温条件下长期存放,其物化性质保持稳定。
2.1.4形成复合物
Masuda等研究发现,阿昔洛韦可以和酒石酸形成阿昔洛韦-酒石酸共晶体,和枸橼酸形成阿昔洛韦-枸橼酸无定型复合物,形成复合物后阿昔洛韦的溶解速度明显快于无水阿昔洛韦,无定型复合物在采用 PEG 为基质的乳膏中透皮率明显高于结晶型。
2.1.5其他
混悬液中产生絮凝、乳剂的分层、注射剂中的配伍反应产生不溶性微粒等。
2.2化学不相容
药用辅料来源广泛,多为天然产物、半合成或合成的物质,药用辅料结构各异,自身所带功能基团也各不相同,因而原辅料间极可能发生一些简单或复杂的化学反应。
2.2.1美拉德反应
常见于含有还原糖的辅料(如乳糖、葡萄糖、麦芽糖等)与含胺类基团(伯胺、仲胺)的原辅料(如蛋白类药物、肽类药物、阿昔洛韦、盐酸氟西汀等)配伍使用时。伯胺类药物生成糖基化中间体后还可发生阿姆德瑞分子重排,使药物杂质增加。影响美拉德反应的因素很多,美拉德反应除了受到糖类和胺类的影响,还受到温度、时间、pH、水分活度的影响,前者主要影响反应产物的种类,后者主要影响反应的动力学。
2.2.2水解反应
水分是影响药物稳定性的重要因素之一。无论是外围环境中的水分还是原辅料自身含有水分均可引起药物的水解。有文献报道,阿司匹林与聚乙烯比咯烷酮、微晶纤维素等辅料混合制备产品时,若不控制辅料中水分,阿司匹林容易发生水解反应,与硬脂酸镁合用时,可加速阿司匹林的水解。
2.2.3降解反应
多见于pH敏感的药物和酸性/碱性辅料的混合物。辅料本身含有的酸性/碱性基团可以调整原辅料混合的微观环境pH值,因而对药物的稳定性产生影响。磷酸氢钙二水合物(DCPD)为片剂处方中常用的填充剂,由于其本身具有碱性,已证明其与许多酸性药物不相容。抗癌药β-拉杷醌与DCPD配方使用,药物可促进DCPD在较低温度下脱水,形成碱性微环境,β-拉杷醌部分溶于DCPD的结晶水中发生化学降解。
盐酸度洛西汀为Eli Lilly公司开发的5-羟色胺和去甲肾上腺素再摄取抑制剂,结构中含有仲胺。度洛西汀为酸不稳定化合物,可降解为剧毒化合物 1-萘酚。因此需对其进行肠溶包衣。而常用的肠溶型包衣聚合物HPMCAS和HPMCP结构中均含有游离酸,度洛西汀与聚合物发生降解反应产生琥珀酰胺和邻苯二甲酰胺杂质。
2.2.4酸碱反应
氧化镁因其碱性可作为pH调节剂,也可用作抗酸药。有文献报道,布洛芬与氧化镁的1:1和2:1二元固体混合物在55℃时发生了化学反应,镁(二布洛芬)为该反应的产物。使用碱性氧化物(氧化钙)和氢氧化物(氢氧化镁)与布洛芬配伍,也出现类似化学反应。
2.2.5氧化反应
某些辅料如聚维酮和聚乙二醇(PEGs)含有合成副产物的有机过氧化物,气相二氧化硅和气相二氧化钛含气相金属氧化物,虽然符合药典相关的过氧化标准限度,但仍可能引起药物氧化降解。聚维酮(PVP)是以过氧化氢为引发剂,通过N-乙烯吡咯烷酮自由基聚合而制备所得。因此市售PVP通常含有微量未反应的过氧化物。Hartauer等人研究发现,采用聚维酮制备盐酸雷洛昔芬片,聚维酮中的过氧化物杂质可导致盐酸雷洛昔芬N-氧化物衍生物的产生。
2.2.6氢键反应
药物分子与辅料分子间以氢键结合,可提高或阻滞药物的释放。Sibel 等研究发现塞来昔布的氨苯磺胺基可与硬脂酸镁的羧基或胶体二氧化硅的硅烷醇基发生氢键结合,抑制药物的有效释放。氢键作用还常见与含胺基和含羟基的原辅料混合物中。
2.2.7其他
除上述几种常见的化学反应外,原辅料之间还可发生络合反应、包合反应、氧化还原、转移反应、裂解反应、异构化反应、合成反应等等。原辅料间的化学反应与原料及其杂质、辅料本身的化学结构、功能基团及其所含的杂质以及外围环境因素有关。
常见原辅料功能基团的化学不相容情况
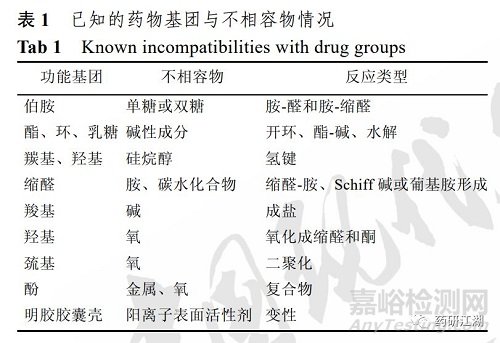
图片来源:口服固体制剂原辅料相容性研究进展
辅料中带入的杂质及可能的不相容反应
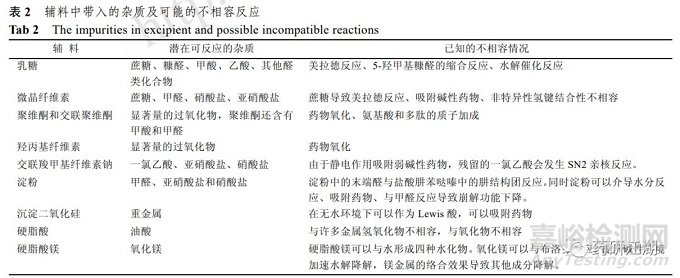
2.3生物不相容
原辅料的生物不相容通常以有效性、安全性为评价指标,主要表现为体内ADME方面的不相容和药物治疗方面的不相容。
2.3.1体内ADME方面的不相容
2002年罗氏召回VERSED 糖浆剂(盐酸咪达唑仑糖浆剂),原因即为咪达唑仑和处方中糖精形成不溶性复合结晶沉淀物,该沉淀物导致产品给药时剂量不均一,进而导致过量或低剂量给药,产生给药安全性和有效性问题。含有四环素的产品可与处方中碳酸钙形成难溶性复合物、苯巴比妥可与PEG400形成难溶性复合物,这些都会导致主药溶解度和口服生物利用度下降。
2.3.2治疗方面的不相容
如降糖药物处方使用的大量的蔗糖作为辅料,降血压的药物采用含钠离子的辅料,外用药使用对皮肤有强烈刺激的辅料等。
三、原辅料相容性筛选试验
写到这,小编都有点饿了,写了这么多很消耗脑力的!不过,估计你们也有点看累了,不过再坚持一下,下面内容也是重点。
鉴于目前尚无统一的原辅料相容性试验操作指南,因此在设计原辅料相容性试验时应充分考虑原料、辅料的理化性质及其可能存在的潜在杂质以及制剂产品的剂型特点以及产品制备、贮存过程中潜在的影响因素。
原辅料相容性试验的设计以在了解原料药和其杂质,辅料和其杂质,制剂生产的降解途径和潜在加工条件的机理。科学合理的方法应用于构造相容性研究中。在研究时,应适当关注同名称辅料的来源、类型等信息,以考察因辅料自身差异可能带来的产品质量差异。
3.1辅料种类及比例:二元或多元体系
产品开发的处方可能涉及到药物与一种或多种辅料。一般,原辅料相容性试验设计是将原料与辅料配制成二元混合物,同时采用药物和辅料的单独样品作对照研究。二元混合物的混合比例尚无明确标准。不同辅料在处方中功能不同,因此处方用量也各异,一般原辅料相容性研究中辅料配比皆高于处方量,目的是考察辅料在高用量的情况下,原辅料混合物的稳定性。一般,对于辅料用量较大的(如稀释剂等),可按主药:辅料=1:5的比例混合,若用量较小的(如润滑剂等),可按主药:辅料=20:1的比例混合。
也可根据实际情况自行设定混合比例,如在FDA发布的仿制药研发(QbD)实例中,原辅料相容性研究采用的是药物与辅料比例为1:1的二元固体混合体系。
原则上,原辅料相容性试验为一种原料对应一种辅料。但在已知某些类别的化合物与特定辅料不相容,而原型处方同时存在有利于其稳定的辅料的情况下,需要重新设计实验。此种情况下,可考虑将试验设计为三元原辅料混合物体系,多元原辅料混合迷你处方体系或采用N-1试验设计。
例如,在FDA发布的仿制药研发(QbD)实例中,为进一步评估原辅料的潜在交互作用是否会引起药物的不稳定性,,采用N-1设计,制备了药物与辅料的几种不同混合无,除包括代表成品比例的药物和所有辅料的混合物外,其与的混合物样品,每次去掉一种辅料。
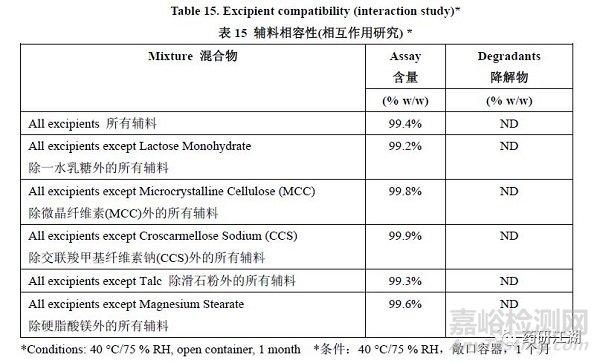
图片来源:Quality by Design for ANDAs: An Example for Immediate-Release Dosage Forms,FDA,2012.
除此之外,原辅料相容性试验设计还应考虑到原料和辅料的来源或者型号,特别是一些生产工艺不同、聚合物纯度等级有差别的原辅料。
3.2制备方式
通常,用于相容性考察的原辅料混合物样品多为直接物理混合所得。但从原辅料到终产品的过程中,其他非物料因素也会对产品质量或稳定性产生影响。如果忽略这些因素,相容性结果则不能正确反映原辅料间的潜在不相容,对辅料选择做出错误性指导。
大多数的药物不稳定性反应是经水解、氧化、美拉德反应等发生的。机械应力(研磨、压制、搅拌切碎)、温度和水分在加速反应发生中起着重要作用。而产品在制备过程中极易引入这些变量。
因此在制备或考察原辅料相容性样品过程中,可模拟制剂产品的制备工艺,主动引入这些变量,以全面考察原辅料的相容性。相容性研究中,可通过球磨机研磨、原辅料共同研磨模拟机械应力,通过卡弗(Carver)试验验证混合组分的可压性。
在药物辅料混合物中添加不同浓度的氧化剂(如过氧化氢)、不同抗氧化剂、不同批次和纯度的辅料(如PVP)等,考察原辅料混合体系的氧化敏感度。制备样品的混悬液或在封闭的混合物体系中加入5%~20%的水,考察水分对样品稳定性的影响。
3.3考察条件
通常是参照中国药典“原料药与制剂稳定性试验指导原则”和《化学药物(原料药和制剂)稳定性研究技术指导原则》中影响因素的实验方法或其他适宜的试验方法,同时采用原料药和辅料分别做平行对照实验。
影响因素实验一般包括高温、高湿、强光照实验。高温试验一般高于加速试验温度10℃以上(如50℃、60℃等),高湿试验通常采用相对湿度75%或更高(如92.5% RH等),光照试验的总照度不低于1.2×106Lux•hr、近紫外能量不低于200w•hr/m2。考察时间点通常可设定为0天、5天、10天、30天等。
若考察药物长期稳定性,宜选择恒温加速试验(isothermal stress testing,IST)。该实验将有一定湿度(加5%~20%的水)或无湿度的药物辅料混合物放置在高于一般贮存温度条件(>50℃)若干时间(通常3~4周甚至6个月),然后根据试验目的和要求选择适宜的检测方法分析加速样品。该实验时间较长且需借助其他仪器如HPLC来定量分析。虽然操作较复杂,但IST试验特别适用于研究药物降解途径和药物与辅料的交互作用。
3.4评价指标
原辅料相容性的考察项目通常包括:性状(外观)、杂质(有关物质)、水分和含量等。除此之外,还可根据剂型的特点和实际情况自行设计能够反映其质量特性的指标,如原料的晶型、熔点等。
对于需要测定含量和水分的样品,建议分别单次包装,以避免取样不均匀引入的测定误差,配制的样品含量尽量均匀,以避免测定结果的分散性;药物颗粒的大小对结果也有影响,故样品药用一定规格的筛号过筛并测定其粒度,固体表面是微粉的重要性质,必要时可用BET方法测定。
原辅料相容性实验的原辅料配比、制备方法、考察条件不能完全模拟制剂产品的生产、贮存过程,因此原辅料相容性试验的结果并不能作为辅料选择和评价工艺的金标准。大多数的美拉德反应,可通过减少制剂中水分活度并使用适当的包装来避免。有时即使相容性试验显示原辅料存在不相容问题,但并不影响产品开发继续选择使用该辅料。
如FDA发布的仿制药研发(QbD)实例中,主药与硬脂酸镁的二元混合物有相互作用,但产品处方开发仍然选择使用硬脂酸镁,通过外加硬脂酸镁的制备工艺来限制主药与硬脂酸镁的接触,鉴定和定量主药与硬脂酸镁的加合物杂质AD1,通过控制该杂质限度来保证产品的稳定性。
四、结语
生活中的很多事情都是想通的,从做菜想到做处方,从菜品搭配想到辅料相容性,只要想做好一件事情,用心才是关键。做菜前要选好主菜、配菜、佐料,而在做处方前要做好原辅料相容性。这也是做好一道菜,研究好一个处方前,一个重要的部分。
回到处方设计上看,评估药物和不同辅料间可能的不相容性是保证制剂产品质量的基础,是保证制剂产品良好稳定性的关键。原辅料相容性试验也体现了质量源于设计(QbD)的思想,对产品研发中质量风险控制策略的制定具有重要参考意义。
参考文献
1. 胡士高,孙备. 口服固体制剂原辅料相容性研究进展[J]. 中国现代应用药学,2012,29(9):789-793.
2. 曹筱琛,贾飞,陶巧凤.药物与辅料相容性研究进展[J]. 中国现代应用药学,2013,30(2):223-228.
3. FDA:Quality by Design for ANDAs: An Example for Immediate-Release Dosage Forms,2012.
4. FDA:Quality by Design for ANDAs: An Example for Modified-Release Dosage Forms,2012.
5. Bharate SS, Bharate SB, Bajaj AN. Interactions and incompatibilities of pharmaceutical excipients with active pharmaceutical ingredients: a comprehensive review[J]. J Excipients and Food Chem,2010, 1:3–26.
6. 大咖手把手教你原辅料相容性试验,丁香园论坛
7.《化学药物制剂研究基本技术指导原则》

来源:Internet


