您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-13 23:24
恶性肿瘤是人类健康的杀手之一,其中乳腺癌在全球范围内均呈现出随年递增的高发病率。免疫原性细胞死亡(ICD)的概念作为抗肿瘤免疫治疗的重要理论基础,可以通过逆转肿瘤免疫原性差的状况,提高抗癌疗法免疫应答率。然而,针对恶性程度较高,且原发灶较深的三阴性乳腺癌(TNBC)而言,单纯应用ICD相关治疗的疗效并不如人意,且抗癌治疗所引起的癌细胞免疫逃逸,以及癌转移及复发率高等问题,仍然是临床抗癌治疗的难点。
磁热疗法是一种微创的肿瘤消融方式,其利用交变磁场(AMF)下磁性介质产生的热量来局部消融肿瘤以及作为热源驱动化合物引发剂分解作用,不仅克服了传统热疗法的循环热损失和穿透深度限制,还可以与免疫检查点阻断相结合,以提高抗癌疗效。
重庆医科大学基础医学院梁冰团队在水凝胶生物材料临床应用转化领域展开了多年的研究,研究范围涉及肿瘤靶向治疗,骨肿瘤治疗及骨缺损修复等(ACS Appl. Mater. Inter. 2022; J. Magnes. Alloy 2021; Theranostics, 2019等)。PLGA是FDA认证的医用高分子聚合物,具有良好的生物相容性,可作为微创植入型生物材料注射到原位肿瘤部位达到治疗肿瘤的目的。基于以上思考,曹友德/梁冰团队在国际知名期刊Materials Today Bio发表文章《Injectable versatile liquid-solid transformation implants alliance checkpoint blockade for magnetothermal dynamic-immunotherapy》 (IF=10.76)。
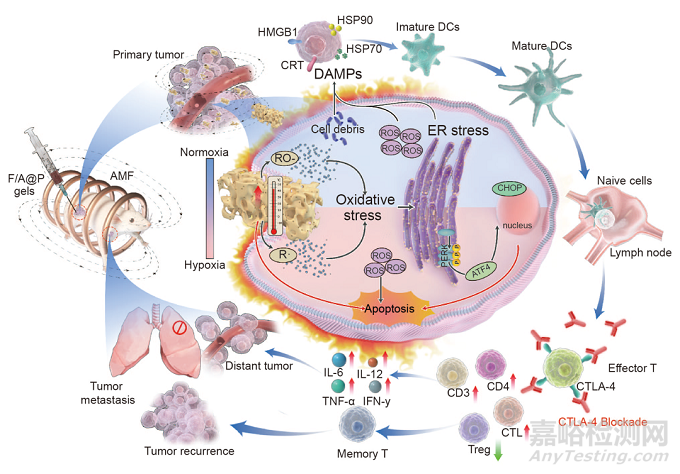
图1: 基于F/A@P凝胶的抗TNBC免疫治疗方案:磁热效应与ROS双重诱导ICD有效改善肿瘤免疫原性,联合免疫检查点阻断以提高TNBC免疫治疗效果
该团队设计了液固转换多孔多功能植入免疫凝胶,用于三阴性乳腺癌的磁热动态免疫治疗(图1)。研究显示该水凝胶(F/A@P)具有良好的液固相变性能,在磁热驱动下具有丰富的多孔结构,Fe3O4纳米粒负载稳定,大大提高了磁热能转换效率。(图2)
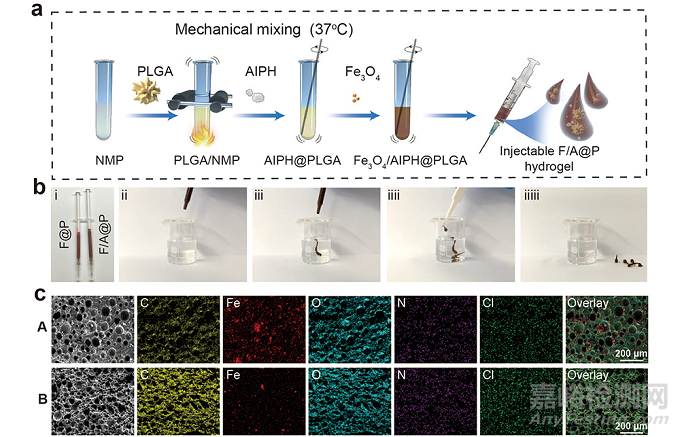
图2.F/A@P水凝胶的合成示意图,液固相变过程及SEM图及相应元素图。
同时,AIPH被热分解为大量与氧无关的的自由基并随即辐散至肿瘤环境中,不仅可以精准的杀死癌细胞而减少对周围正常组织的损坏,而且这些丰富的氧化应激损伤的积累打破了内质网平衡稳态,通过激活PERK信号通路诱导内质网应激的产生(图3)。F/A@P介导的磁热效应协同双重内源性应激诱导癌细胞发生大规模ICD,增强了癌细胞免疫原性,随后表达在癌细胞表面的损伤相关分子模式(DAMPs)等,促使树突状细胞成熟,提高了抗原识别和呈递的功能。
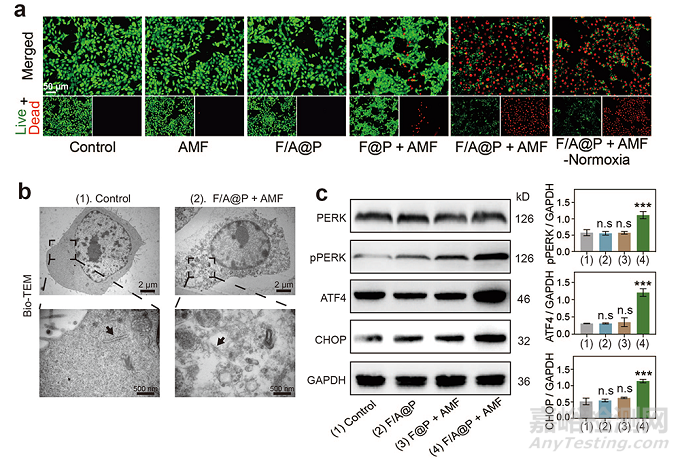
图3. F/A@P水凝胶的体外杀伤效应以及激活PERK信号通路诱导内质网应激的产生。
此外团队还通过建立转移双侧原位TNBC小鼠模型来评估F/A@P免疫凝胶的体内抗癌效应,结果如图4所示:
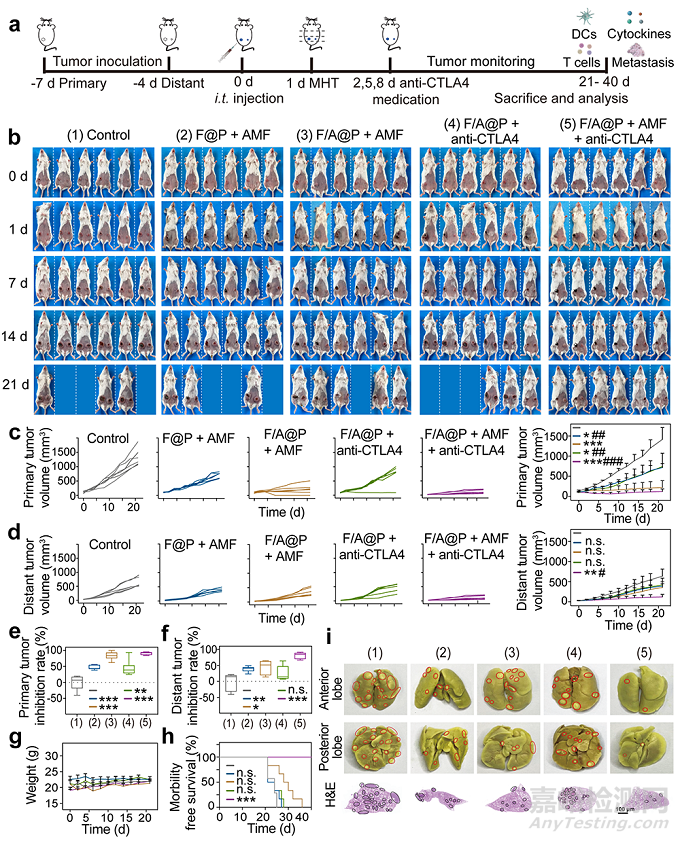
图4: F/A@P介导的MDT联合CTLA4阻断治疗对小鼠原位4T1荷瘤模型的抗肿瘤作用。
当原发肿瘤接受F/A@P的磁热治疗后的小鼠联合接受CTLA4检查点阻断用药时,其21天的原发和远处肿瘤抑制率均达到90%。免疫流式检测证实了这种磁热动态免疫策略在模型体内应用后所引起的肿瘤免疫抑制性微环境的重新编程(图5),包括CD8+ T细胞浸润,Treg T细胞抑制、记忆T细胞的激活,以防止肿瘤复发。
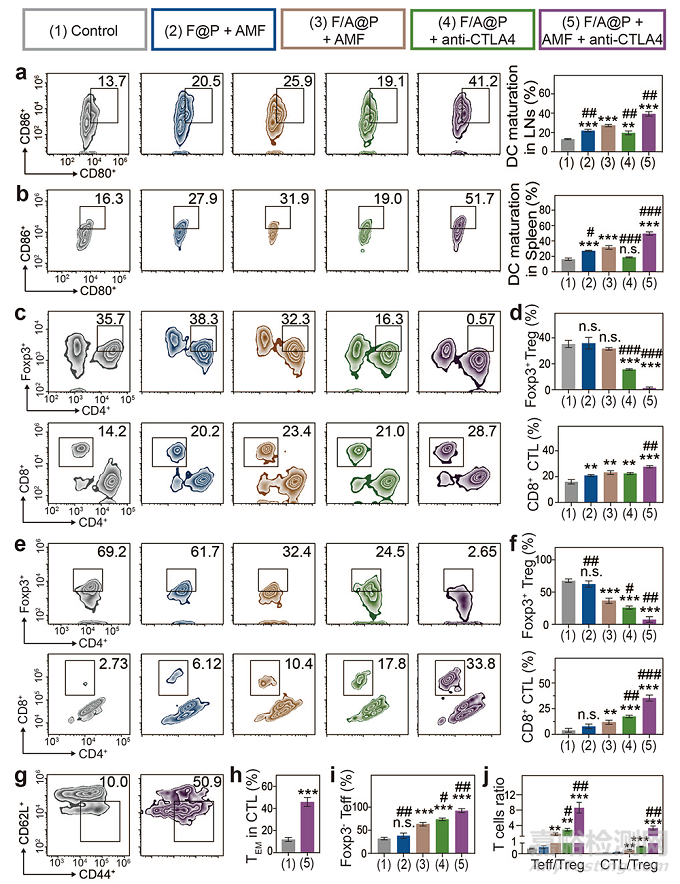
图5.免疫流式检测证实了肿瘤免疫抑制性微环境的重新编程。
这种显著的治疗效果为抗肿瘤免疫治疗提供了新的思路,基于液固转换多孔多功能的F/A@P凝胶的磁热动力免疫疗法,用于恶性肿瘤的微创治疗。基于F/A@P免疫凝胶中所有成分都是FDA批准的,以及磁热疗法及其应用前景引起的广泛关注,该项研究有望产生进一步的临床转化。
重庆医科大学基础医学院硕士生王孟娜为该论文的第一作者。重庆医科大学基础医学院病理教研室曹友德教授、梁冰助理研究员,重庆市中医院副主任医师余柯晓,为该论文的共同通讯作者。本研究得到了国家自然科学基金(82102909)、国家博士后基金(2021M693754)、重庆市博士后特别资助(2021XM2023)等基金项目的大力支持。

来源:高分子科技


